解题方法
1 . 某化学兴趣小组探究不同条件下化学能转化为电能的装置如图所示。
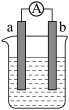
回答下列问题:
(1)若电极a为 ,b为
,b为 ,且a、b质量相等,电解质溶液为
,且a、b质量相等,电解质溶液为 溶液,电路中通过
溶液,电路中通过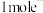 时,a、b的质量差为
时,a、b的质量差为_______ g。
(2)若电极a为 ,b为
,b为 ,电解质溶液为氢氧化钠溶液,则该电池的负极反应式为
,电解质溶液为氢氧化钠溶液,则该电池的负极反应式为_______ 。
(3)若该电池为 燃料电池,氢氧化钠溶液为电解质溶液,电子由a移向b,则
燃料电池,氢氧化钠溶液为电解质溶液,电子由a移向b,则 应通入
应通入_______ 极(填“a”或“b”),该电极反应式为_______ ,电解质溶液中 向
向_______ 极移动(填“a”或“b”)。
(4)理论上能自发进行的氧化还原反应可以设计成原电池。请利用反应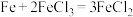 设计一个原电池,并在方框内画出简单原电池实验装置图
设计一个原电池,并在方框内画出简单原电池实验装置图______ ,注明电极材料和电解质溶液。


回答下列问题:
(1)若电极a为
 ,b为
,b为 ,且a、b质量相等,电解质溶液为
,且a、b质量相等,电解质溶液为 溶液,电路中通过
溶液,电路中通过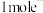 时,a、b的质量差为
时,a、b的质量差为(2)若电极a为
 ,b为
,b为 ,电解质溶液为氢氧化钠溶液,则该电池的负极反应式为
,电解质溶液为氢氧化钠溶液,则该电池的负极反应式为(3)若该电池为
 燃料电池,氢氧化钠溶液为电解质溶液,电子由a移向b,则
燃料电池,氢氧化钠溶液为电解质溶液,电子由a移向b,则 应通入
应通入 向
向(4)理论上能自发进行的氧化还原反应可以设计成原电池。请利用反应
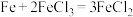 设计一个原电池,并在方框内画出简单原电池实验装置图
设计一个原电池,并在方框内画出简单原电池实验装置图
您最近一年使用:0次
2 . 2023年全国政府工作报告指出,推动重点领域节能降碳减污。一种太空生命保障系统利用电解水供氧,生成的氢气与宇航员呼出的二氧化碳在催化剂作用下生成水和甲烷,水可循环使用。
(1)已知 与
与 的燃烧热分别为
的燃烧热分别为 ,
, ,
,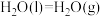
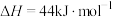 ,写出
,写出 与
与 反应生成
反应生成 和
和 的热化学方程式
的热化学方程式______ 。
(2)一定温度下,在恒容密闭容器中 与
与 反应生成
反应生成 和
和 。
。
①能说明该反应达到平衡状态的是___________ (填字母)。
A. B.容器内压强一定 C.气体平均相对分子质量一定
B.容器内压强一定 C.气体平均相对分子质量一定
D.气体密度一定 E. 的体积分数一定
的体积分数一定
②已知容器的容积为5 L,初始加入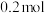
 和
和
 ,反应平衡后测得
,反应平衡后测得 的转化率为50%,则该反应的平衡常数为
的转化率为50%,则该反应的平衡常数为___________ 。
③温度不变,再加入 、
、 、
、 、
、 各
各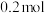 ,则
,则
___________ (填“>”“<”或“=”) 。
。
(3)工业上在一定条件下利用 与
与 可直接合成有机中间体二甲醚:
可直接合成有机中间体二甲醚: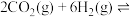
 。当
。当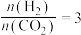 时,实验测得
时,实验测得 的平衡转化率随温度及压强变化如图所示。
的平衡转化率随温度及压强变化如图所示。

①该反应的
___________ (填“>”或“<”)0。
②图中压强(p)由大到小的顺序是___________ 。
(4)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。

①系统工作时,a极为___________ 极,b极区的电极反应式为___________ 。
②系统工作时b极区有少量固体析出,可能的原因是___________ 。
(1)已知
 与
与 的燃烧热分别为
的燃烧热分别为 ,
, ,
,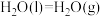
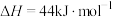 ,写出
,写出 与
与 反应生成
反应生成 和
和 的热化学方程式
的热化学方程式(2)一定温度下,在恒容密闭容器中
 与
与 反应生成
反应生成 和
和 。
。①能说明该反应达到平衡状态的是
A.
 B.容器内压强一定 C.气体平均相对分子质量一定
B.容器内压强一定 C.气体平均相对分子质量一定 D.气体密度一定 E.
 的体积分数一定
的体积分数一定②已知容器的容积为5 L,初始加入
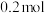
 和
和
 ,反应平衡后测得
,反应平衡后测得 的转化率为50%,则该反应的平衡常数为
的转化率为50%,则该反应的平衡常数为③温度不变,再加入
 、
、 、
、 、
、 各
各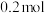 ,则
,则
 。
。(3)工业上在一定条件下利用
 与
与 可直接合成有机中间体二甲醚:
可直接合成有机中间体二甲醚: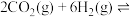
 。当
。当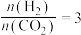 时,实验测得
时,实验测得 的平衡转化率随温度及压强变化如图所示。
的平衡转化率随温度及压强变化如图所示。
①该反应的

②图中压强(p)由大到小的顺序是
(4)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。

①系统工作时,a极为
②系统工作时b极区有少量固体析出,可能的原因是
您最近一年使用:0次
名校
3 . 海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。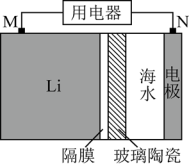
(1)N极为该电池的___________ 极。该电池的总反应为:___________
(2)N极上发生的电极反应为:___________ 、___________
(3)玻璃陶瓷的作用是___________

(1)N极为该电池的
(2)N极上发生的电极反应为:
(3)玻璃陶瓷的作用是
您最近一年使用:0次
4 . 某小组学生研究常见的金属腐蚀现象,分析其原理.按要求回答下列问题.
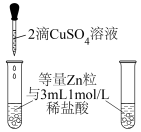
(1)甲同学设计如图所示对比实验。
当a中滴入CuSO4溶液后,观察到其中产生气泡的速率较b中的________ 。其原因是________________ 。
(2)乙同学将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的铁粉和碳粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化,如图所示。
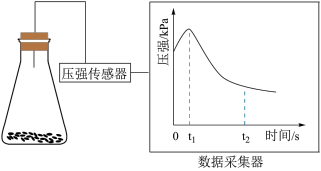
① 时,碳粉表面生成的气体为
时,碳粉表面生成的气体为________ 。
② 时,碳粉表面发生的电极反应式为
时,碳粉表面发生的电极反应式为________________ 。
③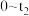 电化学腐蚀过程中,铁极的电极反应式为
电化学腐蚀过程中,铁极的电极反应式为________________ 。
(3)丙同学研读如下一次性保暖贴说明书,并分析暖贴工作原理。
①暖贴工作时,铁粉发生的反应为________ (填“氧化反应”或“还原反应”)。
②写出使用暖贴时的注意事项:________________ 。
③暖贴发热时,正极材料为________ ;食盐的作用为________ 。
④当暖贴放热结束时,铁粉转化成的物质中可能含有________ 。

(1)甲同学设计如图所示对比实验。
当a中滴入CuSO4溶液后,观察到其中产生气泡的速率较b中的
(2)乙同学将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的铁粉和碳粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化,如图所示。

①
 时,碳粉表面生成的气体为
时,碳粉表面生成的气体为②
 时,碳粉表面发生的电极反应式为
时,碳粉表面发生的电极反应式为③
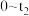 电化学腐蚀过程中,铁极的电极反应式为
电化学腐蚀过程中,铁极的电极反应式为(3)丙同学研读如下一次性保暖贴说明书,并分析暖贴工作原理。
| 品名:一次性保暖贴 主要成分:铁粉、水、食盐、活性炭、蛭石、吸水性树脂 产品性能:平均温度 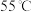 ,最高温度 ,最高温度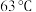 ,发热时间12小时以上 ,发热时间12小时以上 |
②写出使用暖贴时的注意事项:
③暖贴发热时,正极材料为
④当暖贴放热结束时,铁粉转化成的物质中可能含有
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
5 . 某化学学习小组同学利用Fe3+与I-发生的氧化还原反应设计一个原电池,并进行有关实验探究。请回答相关问题:
(1)画出简单的示意图,并标明所使用的用品。供选择的实验用品:KCl溶液,FeCl3溶液,FeCl2溶液,KI溶液,铜片,锌片,铁片,石墨棒,烧杯,盐桥,导线,灵敏电流计______ 。
(2)利用(1)中设计好的装置,控制适合的条件对反应2Fe3++2I- 2Fe2++I2进行实验探究:
2Fe2++I2进行实验探究:
①反应开始时,右池中电极上发生氧化反应,电极反应式为______ ,盐桥中的_____ (填“阳”或“阴”)离子向右池移动。
②电流计指针不发生偏转时,反应达到化学平衡状态,在左池中加入FeCl2固体,右池的电极作______ (填“正”“负”)极。
(1)画出简单的示意图,并标明所使用的用品。供选择的实验用品:KCl溶液,FeCl3溶液,FeCl2溶液,KI溶液,铜片,锌片,铁片,石墨棒,烧杯,盐桥,导线,灵敏电流计
(2)利用(1)中设计好的装置,控制适合的条件对反应2Fe3++2I-
 2Fe2++I2进行实验探究:
2Fe2++I2进行实验探究:①反应开始时,右池中电极上发生氧化反应,电极反应式为
②电流计指针不发生偏转时,反应达到化学平衡状态,在左池中加入FeCl2固体,右池的电极作
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
6 . 回答下列问题:
(1)镍镉(Ni-Cd)可充电电池在现代生活中有广泛的应用。已知某镍镉电池的电解质溶液为 溶液,其充、放电按下式进行:
溶液,其充、放电按下式进行: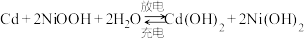 。
。
负极:_______ 。
阳极:_______ 。
(2)某电动汽车配载一种可充放电的锂离子电池,放电时电池总反应为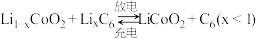 。则:
。则:
负极:_______ 。
正极:_______ 。
(1)镍镉(Ni-Cd)可充电电池在现代生活中有广泛的应用。已知某镍镉电池的电解质溶液为
 溶液,其充、放电按下式进行:
溶液,其充、放电按下式进行: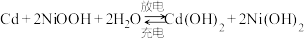 。
。负极:
阳极:
(2)某电动汽车配载一种可充放电的锂离子电池,放电时电池总反应为
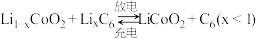 。则:
。则:负极:
正极:
您最近一年使用:0次
22-23高一·全国·课时练习
解题方法
7 . 人们应用原电池原理制作了多种电池以满足不同的需要,同时废弃的电池随便丢弃也会对环境造成污染。请回答下列问题:
(1)电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2。
①工作时电流从_______ 极流向_______ 极(填“Ag2O”或“Zn”)。
②电极反应式:正极:_______ ,负极:_______ 。
③工作时电池正极区的pH_______ (填“增大”“减小”或“不变”)。
(2)氢镍电池是近年来开发出来的可充电电池,它可以取代会产生镉污染的镉镍电池。氢镍电池的总反应式为 H2+NiO(OH)
H2+NiO(OH) Ni(OH)2。电池放电时,负极反应式为
Ni(OH)2。电池放电时,负极反应式为_______ ,正极反应式为_______ ,正极附近溶液的pH_______ (填“增大”“减小”或“不变”)。
(1)电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2。
①工作时电流从
②电极反应式:正极:
③工作时电池正极区的pH
(2)氢镍电池是近年来开发出来的可充电电池,它可以取代会产生镉污染的镉镍电池。氢镍电池的总反应式为
 H2+NiO(OH)
H2+NiO(OH) Ni(OH)2。电池放电时,负极反应式为
Ni(OH)2。电池放电时,负极反应式为
您最近一年使用:0次
22-23高一·全国·课时练习
8 . 利用反应Zn+CuSO4=Cu+ZnSO4,设计一个原电池。
(1)选用_______ 为负极材料,_______ 为正极材料,电解质溶液为_______ 。
(2)写出电极反应式:负极_______ ,正极_______ 。
(3)试画出上述装置图_______ 。
(1)选用
(2)写出电极反应式:负极
(3)试画出上述装置图
您最近一年使用:0次
解题方法
9 . 目前,第三代混合动力车已经投入市场,成为能源改革的典范。
(1)混合动力车一般使用镍氢电池,碱液(主要为KOH溶液)为电解质溶液。镍氢电池的充放电反应式为H2+2NiOOH 2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:
2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:_____ 。
(2)为实现电池的安全性,科技工作者开发出利用稀土金属氧化物作为固体电解质的氢气—空气燃料电池。这种稀土金属氧化物在高温下能传导O2-。写出该电池放电时的负极反应方程式:_____ 。
(1)混合动力车一般使用镍氢电池,碱液(主要为KOH溶液)为电解质溶液。镍氢电池的充放电反应式为H2+2NiOOH
 2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:
2Ni(OH)2。请写出该电池放电时正极的电极反应方程式:(2)为实现电池的安全性,科技工作者开发出利用稀土金属氧化物作为固体电解质的氢气—空气燃料电池。这种稀土金属氧化物在高温下能传导O2-。写出该电池放电时的负极反应方程式:
您最近一年使用:0次
解题方法
10 . 电化学技术在处理污染气体领域的应用广泛。
(1)利用反应 构成电池的方法,既能实现有效消除氮氧化物的排放,又能提供电能,装置如图所示。
构成电池的方法,既能实现有效消除氮氧化物的排放,又能提供电能,装置如图所示。

①A电极的电极反应式为___________ 。
②下列关于该电池的说法正确的是___________ 。
A.电子从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电池工作一段时间,溶液的 不变
不变
D.当有 被处理时,转移电子物质的量为
被处理时,转移电子物质的量为
(2)以含 废气为原料,用电化学方法制取硫酸。装置如图。
废气为原料,用电化学方法制取硫酸。装置如图。

写出负极电极反应式___________ 。若发电厂利用上述装置处理含 废气,电池输出电压为
废气,电池输出电压为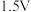 ,每天处理废气约为
,每天处理废气约为 (标准状况),废气中
(标准状况),废气中 体积分数为2.24%。则该电池每天提供
体积分数为2.24%。则该电池每天提供___________  电能。(
电能。( 的电量为
的电量为 )
)
(1)利用反应
 构成电池的方法,既能实现有效消除氮氧化物的排放,又能提供电能,装置如图所示。
构成电池的方法,既能实现有效消除氮氧化物的排放,又能提供电能,装置如图所示。
①A电极的电极反应式为
②下列关于该电池的说法正确的是
A.电子从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电池工作一段时间,溶液的
 不变
不变D.当有
 被处理时,转移电子物质的量为
被处理时,转移电子物质的量为
(2)以含
 废气为原料,用电化学方法制取硫酸。装置如图。
废气为原料,用电化学方法制取硫酸。装置如图。
写出负极电极反应式
 废气,电池输出电压为
废气,电池输出电压为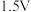 ,每天处理废气约为
,每天处理废气约为 (标准状况),废气中
(标准状况),废气中 体积分数为2.24%。则该电池每天提供
体积分数为2.24%。则该电池每天提供 电能。(
电能。( 的电量为
的电量为 )
)
您最近一年使用:0次



