解题方法
1 . 磷酸锌常用作氯化橡胶合成高分子材料的阻燃剂。工业上利用烧渣灰( 主要含ZnO,还含少量FeO、Al2O3、 CuO 及SiO2)为原料制取磷酸锌的工艺流程如图所示:
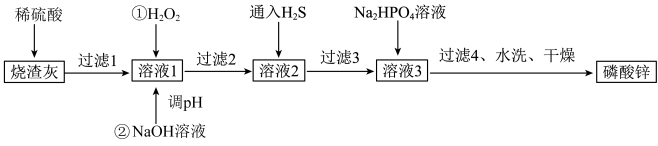
已知:①Zn3(PO4)2在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶液1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
回答下列问题:
(1)基态锌原子的价电子排布式为_____________ 。
(2)加入H2O2的作用是___________________________ 。
(3)经过滤2得到滤渣的主要成分是Fe( OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是___________ 。
(4)通入H2S的目的是除去Cu2+,写出该反应的离子方程式:_________________ 。
(5)洗涤磷酸锌沉淀时应选用________ (填“冷水”或“热水”),洗涤沉淀的操作是________________ 。
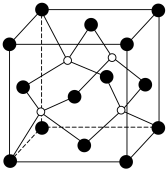
(6)图是碳化硅的晶胞结构,其晶体类型属于___________ 晶体。若碳化硅晶胞边长为a pm,阿伏加德罗常数的值为NA,则碳化硅晶体的密度为______________ g·cm-3 (列出计算式即可)。

已知:①Zn3(PO4)2在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶液1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.0 | 2.2 | 5.4. | 6.5 |
| 完全沉淀的pH | 5.0 | 3.6 | 6.7 | 8.5 |
(1)基态锌原子的价电子排布式为
(2)加入H2O2的作用是
(3)经过滤2得到滤渣的主要成分是Fe( OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是
(4)通入H2S的目的是除去Cu2+,写出该反应的离子方程式:
(5)洗涤磷酸锌沉淀时应选用
(6)图是碳化硅的晶胞结构,其晶体类型属于

您最近一年使用:0次
2 . 氮及其化合物在工农业生产中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一
Ⅰ.一定条件下,用 催化还原可消除NO污染。
催化还原可消除NO污染。
已知:
①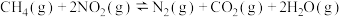
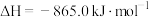
②
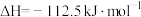
(1) 和
和 完全反应,每生成2.24L(标准状况)NO时,吸收8.9kJ的热量,则
完全反应,每生成2.24L(标准状况)NO时,吸收8.9kJ的热量,则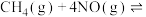
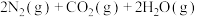

___________  ;一定温度下,往一体积不变的密闭容器中加入适量的
;一定温度下,往一体积不变的密闭容器中加入适量的 和NO,下列条件能判断该反应到达平衡状态的有
和NO,下列条件能判断该反应到达平衡状态的有___________ (填序号)。
A.混合气体的平均相对分子质量不变
B.
C.单位时间里有4n mol C—H断开同时有4n mol O—H断开
D.混合气体的压强不变
E.混合气体的密度不变
(2)将2mol NO(g)、1mol (g)和2mol He(g)通入反应器,在温度T、压强p条件下进行反应②和
(g)和2mol He(g)通入反应器,在温度T、压强p条件下进行反应②和 。平衡时,若
。平衡时,若 、
、 与
与 三者的物质的量相等,则NO转化率为
三者的物质的量相等,则NO转化率为___________ ,反应②平衡常数
___________ (用含p的代数式表示)。
Ⅱ.利用如图所示原理去除NO:
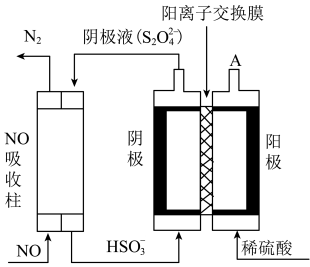
(3)基态N原子中,电子占据的最高能级为___________ 能级,该能级轨道的形状为___________ ;电解池中阴极反应式为___________ 。
(4)A口每产生224mL (体积已换算成标准状况,不考虑
(体积已换算成标准状况,不考虑 的溶解),可处理NO的物质的量为
的溶解),可处理NO的物质的量为___________ mol。
Ⅰ.一定条件下,用
 催化还原可消除NO污染。
催化还原可消除NO污染。已知:
①
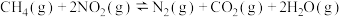
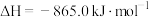
②

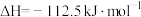
(1)
 和
和 完全反应,每生成2.24L(标准状况)NO时,吸收8.9kJ的热量,则
完全反应,每生成2.24L(标准状况)NO时,吸收8.9kJ的热量,则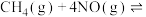
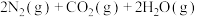

 ;一定温度下,往一体积不变的密闭容器中加入适量的
;一定温度下,往一体积不变的密闭容器中加入适量的 和NO,下列条件能判断该反应到达平衡状态的有
和NO,下列条件能判断该反应到达平衡状态的有A.混合气体的平均相对分子质量不变
B.

C.单位时间里有4n mol C—H断开同时有4n mol O—H断开
D.混合气体的压强不变
E.混合气体的密度不变
(2)将2mol NO(g)、1mol
 (g)和2mol He(g)通入反应器,在温度T、压强p条件下进行反应②和
(g)和2mol He(g)通入反应器,在温度T、压强p条件下进行反应②和 。平衡时,若
。平衡时,若 、
、 与
与 三者的物质的量相等,则NO转化率为
三者的物质的量相等,则NO转化率为
Ⅱ.利用如图所示原理去除NO:

(3)基态N原子中,电子占据的最高能级为
(4)A口每产生224mL
 (体积已换算成标准状况,不考虑
(体积已换算成标准状况,不考虑 的溶解),可处理NO的物质的量为
的溶解),可处理NO的物质的量为
您最近一年使用:0次
2023-09-20更新
|
327次组卷
|
2卷引用:云南大理市辖区2023-2024学年高三上学期毕业生区域性规模化统一检测理综化学试题
3 . 金属铜、铁在日常生活中应用广泛,根据下列说法回答下列问题。
(1) 的制备反应为
的制备反应为 。
。
上述氧化过程中, (II)
(II)_____ (答简化电子排布式)变为 III)
III)_____ (答外围电子排布图),基态 (III)电子占据
(III)电子占据_____ 个不同轨道。
(2)对上述反应式中的短周期元素按照电负性由小到大排序为_____
(3)配合物 的配位数为6,其配体
的配位数为6,其配体 中的
中的 的杂化方式为
的杂化方式为_____ 杂化。
(4)铜原子与氯原子形成化合物的晶胞如图所示(黑球代表铜原子,白球表示氯原子)。
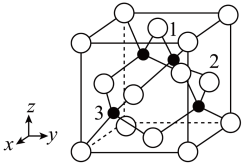
①已知铜和氯的电负性分别为1.9和3.0,则铜与氯形成的化合物属于_____ (填“离子”或“共价”)化合物。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子1的坐标为( ,
, ,1),则原子2和3的坐标分别为
,1),则原子2和3的坐标分别为_____ 、_____ 。
③已知该晶体的密度为 ,阿伏加德罗常数为NA,则该晶体中铜原子和氯原子的最短距离为
,阿伏加德罗常数为NA,则该晶体中铜原子和氯原子的最短距离为_____ pm(只写计算式)。
(1)
 的制备反应为
的制备反应为 。
。上述氧化过程中,
 (II)
(II) III)
III) (III)电子占据
(III)电子占据(2)对上述反应式中的短周期元素按照电负性由小到大排序为
(3)配合物
 的配位数为6,其配体
的配位数为6,其配体 中的
中的 的杂化方式为
的杂化方式为(4)铜原子与氯原子形成化合物的晶胞如图所示(黑球代表铜原子,白球表示氯原子)。

①已知铜和氯的电负性分别为1.9和3.0,则铜与氯形成的化合物属于
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子1的坐标为(
 ,
, ,1),则原子2和3的坐标分别为
,1),则原子2和3的坐标分别为③已知该晶体的密度为
 ,阿伏加德罗常数为NA,则该晶体中铜原子和氯原子的最短距离为
,阿伏加德罗常数为NA,则该晶体中铜原子和氯原子的最短距离为
您最近一年使用:0次
名校
解题方法
4 . DF-31洲际弹道导弹是我国大国地位和国防实力的象征,其制作材料包含了 等多种元素。回答下列问题:
等多种元素。回答下列问题:
(1)基态铁原子的电子排布式为_______ , 具有较强的还原性,原因是
具有较强的还原性,原因是_______ 。
(2) 的第二电离能
的第二电离能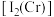 和
和 的第二电离能
的第二电离能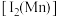 分别为
分别为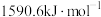 、
、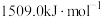 ,
, 的原因是
的原因是_______ ;过氧化铬 中
中 的化合价为
的化合价为 ,则分子中
,则分子中 键、π键的数目之比为
键、π键的数目之比为_______ 。
(3)下图中表示的碳原子能量最高的是_______(填字母)。
(4)超临界流体是物质介于气态和液态之间的新状态,目前应用最广泛的是超临界 。超临界
。超临界 流体是一种具有和水相似能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。
流体是一种具有和水相似能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。 中C原子的杂化方式为
中C原子的杂化方式为_______ ,分子中的化学键为_______ (填“极性键”或“非极性键”),分子属于_______ (填“极性”或“非极性”)分子。
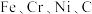 等多种元素。回答下列问题:
等多种元素。回答下列问题:(1)基态铁原子的电子排布式为
 具有较强的还原性,原因是
具有较强的还原性,原因是(2)
 的第二电离能
的第二电离能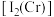 和
和 的第二电离能
的第二电离能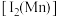 分别为
分别为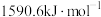 、
、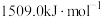 ,
, 的原因是
的原因是 中
中 的化合价为
的化合价为 ,则分子中
,则分子中 键、π键的数目之比为
键、π键的数目之比为(3)下图中表示的碳原子能量最高的是_______(填字母)。
A. | B.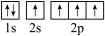 |
C.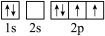 | D.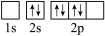 |
 。超临界
。超临界 流体是一种具有和水相似能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。
流体是一种具有和水相似能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。 中C原子的杂化方式为
中C原子的杂化方式为
您最近一年使用:0次
名校
解题方法
5 . 氯吡苯脲是一种常用的膨大剂,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害。其结构简式如下:
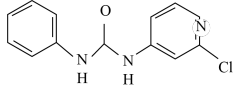
回答下列问题:
(1)基态氯原子价电子排布式为_______ 。
(2)氯吡苯脲的晶体中,氮原子的杂化轨道类型为_______ ,该物质易溶于水的原因是_______ 。
(3)氯吡苯脲晶体中,微粒间的作用力类型有_______ (填字母)。
A.离子键 B.极性键 C.非极性键 D.π键 E.氢键
(4)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。

反应过程中,每生成 氯吡苯脲,形成
氯吡苯脲,形成_______ 个 键、断裂
键、断裂_______ 个π键。
(5)膨大剂能在动物体内代谢,其产物较为复杂,其中有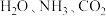 等,请用共价键理论解释
等,请用共价键理论解释 分子比
分子比 分子稳定的原因:
分子稳定的原因:_______ 。

回答下列问题:
(1)基态氯原子价电子排布式为
(2)氯吡苯脲的晶体中,氮原子的杂化轨道类型为
(3)氯吡苯脲晶体中,微粒间的作用力类型有
A.离子键 B.极性键 C.非极性键 D.π键 E.氢键
(4)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。

反应过程中,每生成
 氯吡苯脲,形成
氯吡苯脲,形成 键、断裂
键、断裂(5)膨大剂能在动物体内代谢,其产物较为复杂,其中有
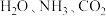 等,请用共价键理论解释
等,请用共价键理论解释 分子比
分子比 分子稳定的原因:
分子稳定的原因:
您最近一年使用:0次
6 . 铜是重要的战略资源,云南是我国铜资源储量较高的省份之一,回答下列问题:
(1)铜在周期表中位于第______ 族(填族序数),属于______ 区。
(2)铜可以形成多种配合物。
① 的核外电子排布式是
的核外电子排布式是______ ,过渡金属离子与水分子形成配合物时,若d轨道全空或全满时,化合物无颜色,否则有颜色。据此判断,
______ (填“有”或“无”)颜色。
② 可形成多种配合物,如
可形成多种配合物,如 ,若其中两个
,若其中两个 被
被 替换,得到的配合物只有两种结构,则
替换,得到的配合物只有两种结构,则 的空间构型是
的空间构型是______ , 中N原子的杂化方式是
中N原子的杂化方式是______ ,空间构型是______ 。
(3)铜与金等金属及合金可用于生产石墨烯的催化剂,如图是一种铜金合金的晶胞示意图:

①Cu原子的配位数是______ 。
②原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为______ 。
(1)铜在周期表中位于第
(2)铜可以形成多种配合物。
①
 的核外电子排布式是
的核外电子排布式是
②
 可形成多种配合物,如
可形成多种配合物,如 ,若其中两个
,若其中两个 被
被 替换,得到的配合物只有两种结构,则
替换,得到的配合物只有两种结构,则 的空间构型是
的空间构型是 中N原子的杂化方式是
中N原子的杂化方式是(3)铜与金等金属及合金可用于生产石墨烯的催化剂,如图是一种铜金合金的晶胞示意图:

①Cu原子的配位数是
②原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为
 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为
您最近一年使用:0次
名校
解题方法
7 . (Ⅰ)瑞德西韦是一种核苷类似物,具有抗病毒活性,对新型冠状病毒病例展现出较好的疗效。其结构如图所示:
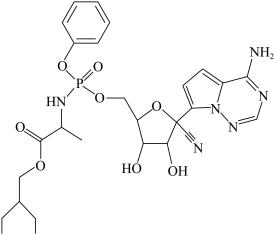
回答下列问题:
(1)该结构中基态P原子价电子的轨道表示式为___________ ,核外电子占据最高能级的电子云轮廓图形状为___________ 。
(2)瑞德西韦组成元素中位于第二周期元素的第一电离能从大到小的顺序为___________ ,分子中氮原子的杂化类型有___________ 。
(3)苯酚(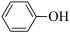 )是合成瑞德西韦的原料之一,其熔点为43℃,苯酚的晶体类型是
)是合成瑞德西韦的原料之一,其熔点为43℃,苯酚的晶体类型是________ 。苯酚与甲苯(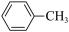 ,熔点℃)的相对分子质量相近,但苯酚的熔、沸点高于甲苯,原因是
,熔点℃)的相对分子质量相近,但苯酚的熔、沸点高于甲苯,原因是___________ 。
(Ⅱ)大力推广磷酸亚铁锂电池新能源汽车对实现“碳达峰”和“碳中和”具有重要意义。电极材料以硫铁矿(主要成分 ,含少量
,含少量 、
、 和
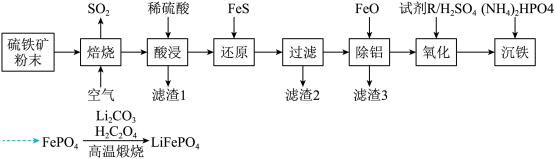
和 )为原料制备,工业流程如图所示。回答下列问题:
)为原料制备,工业流程如图所示。回答下列问题:
(4) 分子的空间结构名称为
分子的空间结构名称为___________ ,试剂R是一种绿色氧化剂,其中心原子杂化方式是___________ 。
(5)从平衡的角度解释加FeO除铝的原因(结合离子方程式说明)___________ 。
(6)若“沉铁”时溶液中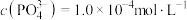 ,则“沉铁”时pH不能高于
,则“沉铁”时pH不能高于___________ ,[已知:常温下,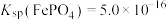 、
、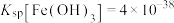 、
、 ,溶液体积变化忽略不计]。
,溶液体积变化忽略不计]。
(7)磷酸亚铁锂( )的晶胞结构如图所示:
)的晶胞结构如图所示:
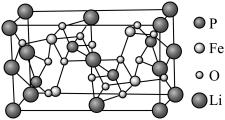
长方体晶胞的长和宽均为 ,高为
,高为 ,
, 为阿伏加德罗常数的值,晶体的密度为
为阿伏加德罗常数的值,晶体的密度为___________  。
。

回答下列问题:
(1)该结构中基态P原子价电子的轨道表示式为
(2)瑞德西韦组成元素中位于第二周期元素的第一电离能从大到小的顺序为
(3)苯酚(
 )是合成瑞德西韦的原料之一,其熔点为43℃,苯酚的晶体类型是
)是合成瑞德西韦的原料之一,其熔点为43℃,苯酚的晶体类型是 ,熔点℃)的相对分子质量相近,但苯酚的熔、沸点高于甲苯,原因是
,熔点℃)的相对分子质量相近,但苯酚的熔、沸点高于甲苯,原因是(Ⅱ)大力推广磷酸亚铁锂电池新能源汽车对实现“碳达峰”和“碳中和”具有重要意义。电极材料以硫铁矿(主要成分
 ,含少量
,含少量 、
、 和
和 )为原料制备,工业流程如图所示。回答下列问题:
)为原料制备,工业流程如图所示。回答下列问题:
(4)
 分子的空间结构名称为
分子的空间结构名称为(5)从平衡的角度解释加FeO除铝的原因(结合离子方程式说明)
(6)若“沉铁”时溶液中
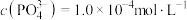 ,则“沉铁”时pH不能高于
,则“沉铁”时pH不能高于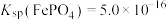 、
、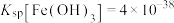 、
、 ,溶液体积变化忽略不计]。
,溶液体积变化忽略不计]。(7)磷酸亚铁锂(
 )的晶胞结构如图所示:
)的晶胞结构如图所示:
长方体晶胞的长和宽均为
 ,高为
,高为 ,
, 为阿伏加德罗常数的值,晶体的密度为
为阿伏加德罗常数的值,晶体的密度为 。
。
您最近一年使用:0次
名校
解题方法
8 . 硫及其化合物用途非常广泛。回答下列问题:
(1)基态S原子的电子占据最高能级的电子云轮廓图为_______ 形。
(2)O和S处于同一主族。 及
及 中,中心原子的杂化方式相同,键长及键角如图1所示。
中,中心原子的杂化方式相同,键长及键角如图1所示。
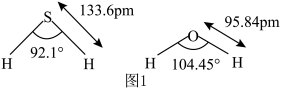
① 分子中的键长比
分子中的键长比 中的键长短,其原因是
中的键长短,其原因是_______ 。
② 分子中的键角
分子中的键角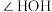 比
比 分子中的键角
分子中的键角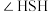 大,其原因是
大,其原因是_______ 。
(3)①单质硫与热的 浓溶液反应的产物之一为
浓溶液反应的产物之一为 。
。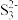 的空间构型为
的空间构型为_______ 。
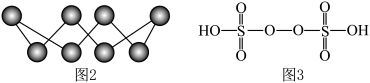
②S单质的常见形式为 ,其环状结构如图2所示,S原子采用的轨道杂化方式是
,其环状结构如图2所示,S原子采用的轨道杂化方式是_______ 。
③钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为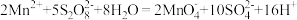 。已知
。已知 的结构如图3所示,上述反应每生成
的结构如图3所示,上述反应每生成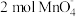 ,
, 层断裂的共价键数目为
层断裂的共价键数目为_______  。
。
(4)噻吩( )广泛应用于合成医药、农药、染料工业。每个噻吩分子中含有
)广泛应用于合成医药、农药、染料工业。每个噻吩分子中含有_______ 个 键。噻吩的沸点为
键。噻吩的沸点为 ,吡咯(
,吡咯(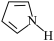 )的沸点在
)的沸点在 之间,后者沸点较高,其原因
之间,后者沸点较高,其原因_______ 。
(1)基态S原子的电子占据最高能级的电子云轮廓图为
(2)O和S处于同一主族。
 及
及 中,中心原子的杂化方式相同,键长及键角如图1所示。
中,中心原子的杂化方式相同,键长及键角如图1所示。
①
 分子中的键长比
分子中的键长比 中的键长短,其原因是
中的键长短,其原因是②
 分子中的键角
分子中的键角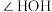 比
比 分子中的键角
分子中的键角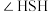 大,其原因是
大,其原因是(3)①单质硫与热的
 浓溶液反应的产物之一为
浓溶液反应的产物之一为 。
。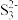 的空间构型为
的空间构型为②S单质的常见形式为
 ,其环状结构如图2所示,S原子采用的轨道杂化方式是
,其环状结构如图2所示,S原子采用的轨道杂化方式是③钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为
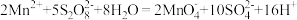 。已知
。已知 的结构如图3所示,上述反应每生成
的结构如图3所示,上述反应每生成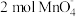 ,
, 层断裂的共价键数目为
层断裂的共价键数目为 。
。
(4)噻吩(
 )广泛应用于合成医药、农药、染料工业。每个噻吩分子中含有
)广泛应用于合成医药、农药、染料工业。每个噻吩分子中含有 键。噻吩的沸点为
键。噻吩的沸点为 ,吡咯(
,吡咯( )的沸点在
)的沸点在 之间,后者沸点较高,其原因
之间,后者沸点较高,其原因
您最近一年使用:0次
9 . 草酸钴在化学中应用广泛,可以用于制取催化剂和指示剂。用水钴矿(主要成分为Co2O3,还含有少量SiO2、Al2O3、CuO、FeO及MnO2杂质)制取草酸钴晶体(CoC2O4·2H2O)的工艺流程如图所示:

常温下,有关沉淀数据如下表(“完全沉淀”时,金属离子浓度≤1.0×10-5mol·L-1)。
回答下列问题:
(1)下列状态的钴中,电离最外层一个电子所需能量最大的是 (填序号)。
(2)“酸浸”时Co2O3发生反应的化学方程式为___________________ 。
(3)“氧化”时发生反应的离子方程式为___________________________ 。
(4)滤渣②的主要成分有_______________________ ,常温下,若“调节pH”后,溶液中c(Co2+)=0.1 mol·L-1,则需调节溶液pH的范围是______________________ ( 忽略溶液的体积变化)。
(5)“提纯”分为萃取和反萃取两步进行,先向除杂后的溶液中加入某有机酸萃取剂(HA)2,发生反应:Co2++n(HA)2 CoA2·(n-1)(HA)2+2H+。当溶液pH处于4.5到6.5之间时,Co2+萃取率随着溶液pH增大而增大,其原因是
CoA2·(n-1)(HA)2+2H+。当溶液pH处于4.5到6.5之间时,Co2+萃取率随着溶液pH增大而增大,其原因是_________________________ ;反萃取时,应加入的物质是_____ ( 填溶液名称)。
(6)某含钴配合物的组成为CoCl3·5NH3·H2O,该配合物中钴离子的配位数是6。1 mol该配合物可以与足量的硝酸银反应生成3 mol AgCl沉淀,则该配合物的配体是________ ,若NH3分子与钴离子形成配合物后,H-N- H键角会____________ (填“变大”“变小”或“不变”),并说明理由:_______________ 。

常温下,有关沉淀数据如下表(“完全沉淀”时,金属离子浓度≤1.0×10-5mol·L-1)。
| 沉淀 | Mn(OH)2 | Co(OH)2 | Cu(OH)2 | Fe(OH)3 | Al(OH)3 |
| 恰好完全沉淀时pH | 10.1 | 9.4 | 6.7 | 2.8 | 5.2 |
(1)下列状态的钴中,电离最外层一个电子所需能量最大的是 (填序号)。
| A.[Ar]3d74s1 | B.[ Ar]3d74s2 |
| C.[Ar]3d74s14p1 | D.[Ar]3d74p1 |
(3)“氧化”时发生反应的离子方程式为
(4)滤渣②的主要成分有
(5)“提纯”分为萃取和反萃取两步进行,先向除杂后的溶液中加入某有机酸萃取剂(HA)2,发生反应:Co2++n(HA)2
 CoA2·(n-1)(HA)2+2H+。当溶液pH处于4.5到6.5之间时,Co2+萃取率随着溶液pH增大而增大,其原因是
CoA2·(n-1)(HA)2+2H+。当溶液pH处于4.5到6.5之间时,Co2+萃取率随着溶液pH增大而增大,其原因是(6)某含钴配合物的组成为CoCl3·5NH3·H2O,该配合物中钴离子的配位数是6。1 mol该配合物可以与足量的硝酸银反应生成3 mol AgCl沉淀,则该配合物的配体是
您最近一年使用:0次
名校
解题方法
10 . 元素周期表是元素周期律的具体表现,是学习和研究化学的一种重要工具。下图是元素周期表的一部分,回答下列问题:
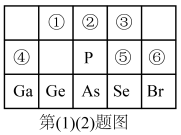

(1)元素①最简单的气态氢化物分子的空间构型是___________ 。请用一个方程式比较元素①和元素②的非金属性强弱:___________ 。
(2)元素⑤、⑥非金属性更强的是:___________ (用元素符号表示),请从原子结构的角度解释:___________ 。
电离能是指由气态原子失去电子形成阳离子需要的能量。从中性原子中失去第一个电子所需要的能量为第一电离能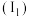 ,失去第二个电子所需要的能量为第二电离能
,失去第二个电子所需要的能量为第二电离能 ,依次类推。上图为1-19号元素第一电离能
,依次类推。上图为1-19号元素第一电离能 。回答下列问题:
。回答下列问题:
(3)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常,预测下列关系式中正确的是___________(填编号)。
(4)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
锰元素位于第四周期第VIIB族。请写出基态 的价层电子排布式:
的价层电子排布式:___________ ,比较两元素的 、
、 ,可知,气态
,可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是___________ 。
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:___________ 。


(1)元素①最简单的气态氢化物分子的空间构型是
(2)元素⑤、⑥非金属性更强的是:
电离能是指由气态原子失去电子形成阳离子需要的能量。从中性原子中失去第一个电子所需要的能量为第一电离能
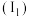 ,失去第二个电子所需要的能量为第二电离能
,失去第二个电子所需要的能量为第二电离能 ,依次类推。上图为1-19号元素第一电离能
,依次类推。上图为1-19号元素第一电离能 。回答下列问题:
。回答下列问题:(3)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常,预测下列关系式中正确的是___________(填编号)。
A.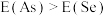 | B. |
C. | D.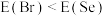 |
| 元素 | Mn | Fe | |
电离能 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
 的价层电子排布式:
的价层电子排布式: 、
、 ,可知,气态
,可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出
 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:
您最近一年使用:0次



