1 . 下表是元素周期表的一部分,用化学用语回答:
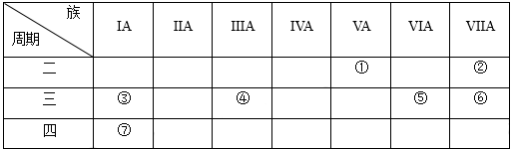
(1)②的元素符号为_________ 。
(2)比较元素③和⑦的原子半径大小:③_____ ⑦(填“>”或“<”)。
(3)绘出元素⑤的离子结构示意图_________________ 。
(4)元素①的氢化物的电子式为____________ ,将该氢化物通入④和⑥形成的化合物的水溶液中,发生反应的离子方程式为___________________________________ 。

(1)②的元素符号为
(2)比较元素③和⑦的原子半径大小:③
(3)绘出元素⑤的离子结构示意图
(4)元素①的氢化物的电子式为
您最近一年使用:0次
名校
解题方法
2 . 下表列出了①~⑥六种元素在周期表中的位置。
请按要求回答下列问题:
(1)写出①的元素符号___________________ 。
(2)⑥的原子结构示意图是_______________ 。
(3)写出③与⑤的单质反应的化学方程式__________________________ 。
(4)③和④中金属性较弱的是_______________ (填化学式)。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||
(1)写出①的元素符号
(2)⑥的原子结构示意图是
(3)写出③与⑤的单质反应的化学方程式
(4)③和④中金属性较弱的是
您最近一年使用:0次
2017-07-01更新
|
97次组卷
|
3卷引用:湖南省郴州市永兴县童星学校2020-2021学年高二下学期期中考试化学试题
名校
解题方法
3 . 元素周期表的第三周期共有______ 种元素;在第三周期元素中,最高价氧化物对应的水化物碱性最强的是__________ (填化学式,下同);最高价氧化物对应的水化物酸性最强的是________ 。
您最近一年使用:0次
2017-05-04更新
|
608次组卷
|
2卷引用:湖南省长沙市长郡中学2016-2017学年高一下学期期中考试化学试题
4 . 下表是元素周期表的一部分,回答下列有关问题:
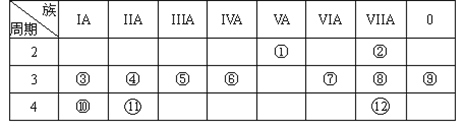
(1)写出元素符号:⑨________ (填化学式,下同)
(2)在这些元素中,最活泼的金属元素是________ 。
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是________ ,呈两性的氢氧化物是________ 。

(1)写出元素符号:⑨
(2)在这些元素中,最活泼的金属元素是
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是
您最近一年使用:0次
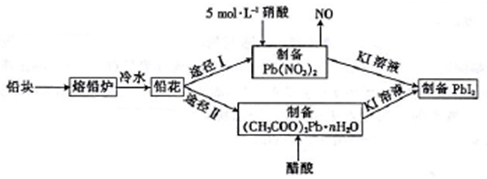
5 . 铅及并化合物在工业生产中具有非常广泛的用途,根据以下流程回答相关问题。
(1)铅是碳的同族元素,且比碳多4个电子层,则铅位于元素周期表第___ 周期__ 族。
(2)反位条件的控制在工业生产中有着极其重要的作用。把铅块制成铅花的目的是_______ 。途径I中不用14 mol·L-1的浓硝酸制备硝酸铅的原因是______________________ 。
(3)写出(CH3COO)2Pb溶液[(CH3COO)2Pb 为弱电解质]与KI溶液反应的离子方程式:_________ 。
(4)取75.8 g (CH3COO)2Pb • nH2O样品在N2气氛中加热,测得剩余固体质量随温度的变化如图所示(样品在75℃时已完全失去结晶水)。
①(CH3COO)2Pb • nH2O中n=______ 。
②150~200℃间分解产物为PbO和一种有机物M,M能与水反应生成乙酸,则该温度区间内分解反应的化学方程式为________________________________ 。
(5)T℃时,取一定量的PbI2固体,用蒸馏水配制成饱和溶液。准确移取25.00mL PbI2饱和溶液,分次加入阳离子交换树脂RH(发生反应:2RH+Pb2+==R2Pb+2H+)中,用250 mL洁净的锥形瓶接受流出液,用蒸馏水淋洗树脂至流出液呈中性。将洗涤液一并盛放到锥形瓶中,加入酚酞,用0.0025 mol·L-1的NaOH溶液滴定,重复上述操作2次,当达到滴定终点时,平均消耗氢氧化钠溶液20.00 mL。则T℃时PbI2的Ksp=_______________________ 。
(1)铅是碳的同族元素,且比碳多4个电子层,则铅位于元素周期表第
(2)反位条件的控制在工业生产中有着极其重要的作用。把铅块制成铅花的目的是
(3)写出(CH3COO)2Pb溶液[(CH3COO)2Pb 为弱电解质]与KI溶液反应的离子方程式:
(4)取75.8 g (CH3COO)2Pb • nH2O样品在N2气氛中加热,测得剩余固体质量随温度的变化如图所示(样品在75℃时已完全失去结晶水)。
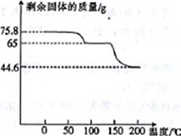
①(CH3COO)2Pb • nH2O中n=
②150~200℃间分解产物为PbO和一种有机物M,M能与水反应生成乙酸,则该温度区间内分解反应的化学方程式为
(5)T℃时,取一定量的PbI2固体,用蒸馏水配制成饱和溶液。准确移取25.00mL PbI2饱和溶液,分次加入阳离子交换树脂RH(发生反应:2RH+Pb2+==R2Pb+2H+)中,用250 mL洁净的锥形瓶接受流出液,用蒸馏水淋洗树脂至流出液呈中性。将洗涤液一并盛放到锥形瓶中,加入酚酞,用0.0025 mol·L-1的NaOH溶液滴定,重复上述操作2次,当达到滴定终点时,平均消耗氢氧化钠溶液20.00 mL。则T℃时PbI2的Ksp=
您最近一年使用:0次
2017-04-20更新
|
460次组卷
|
3卷引用:2017届湖南省郴州市高三第四次质量检测理科综合化学试卷
名校
6 . 下表列出了 A〜R 9种元系在周期表中的位置
(1) 这9中元素中金属性最强的是_________________ ;(填元素符号)
(2) 化学性质最不活泼的元素是_________________ ;(填元素符号)
(3) G的最高价含氧酸的化学式是_________________ ;
(4) 写出一个化学方程式证明G和H的非金属性强弱____________________ 。
族 周期 | IA | IIA | ⅢA | IVA | VA | VIA | ⅦA | 0 |
2 | E | F | ||||||
3 | A | C | D | G | R | |||
4 | B | H |
(1) 这9中元素中金属性最强的是
(2) 化学性质最不活泼的元素是
(3) G的最高价含氧酸的化学式是
(4) 写出一个化学方程式证明G和H的非金属性强弱
您最近一年使用:0次
7 . 下表是元素周期表短周期的一部分

(1)①~⑦元素中金属性最强的元素在元素周期表中的位置是___________ 。
(2)表中元素⑥的原子结构示意图为___________ 。
(3)④与⑤形成的化合物的化学键类型为_______ ,该化合物的电子式为____________ 。
(4)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是___________ (填化学式,下同);④所在主族的前四种元素的单质分别与氢气化合形成的气态氢化物的稳定性由强到弱的顺序是_________ 。
(5)表中元素②的单质与③的最高价含氧酸反应的化学方程式为___________________ 。

(1)①~⑦元素中金属性最强的元素在元素周期表中的位置是
(2)表中元素⑥的原子结构示意图为
(3)④与⑤形成的化合物的化学键类型为
(4)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是
(5)表中元素②的单质与③的最高价含氧酸反应的化学方程式为
您最近一年使用:0次
名校
8 . 元素周期表的形式多种多样,下图是扇形元素周期表的一部分(前四周期的元素),对比中学常见元素周期表,回答下列问题:
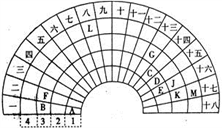
(1)E代表的元素处于常见周期表的位置是___________ 。G的离子结构示意图_____________ 。
(2)CE2的电子式是__________________ 。
(3)元素A和M形成的化合物的水溶液与元素K的单质反应的离子方程式为:__________________ 。反应后,向溶液中加入CK4溶剂,振荡后现象为____________________ 。

(1)E代表的元素处于常见周期表的位置是
(2)CE2的电子式是
(3)元素A和M形成的化合物的水溶液与元素K的单质反应的离子方程式为:
您最近一年使用:0次
名校
9 . 某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式。如果将它们按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“.”代表一种元素,其中P点代表氢元素。
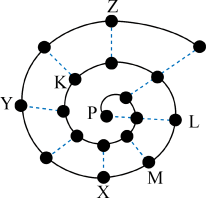
(1)X元素符号为__________________ 。
(2)M与Z两种元素形成的化合物含有的化学键为________________ 。
(3)下列说法正确的是__________________ 。
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L +>K 2﹘
d.由K、L两种元素组成的化合物中可能含有共价键

(1)X元素符号为
(2)M与Z两种元素形成的化合物含有的化学键为
(3)下列说法正确的是
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L +>K 2﹘
d.由K、L两种元素组成的化合物中可能含有共价键
您最近一年使用:0次
2017-03-27更新
|
223次组卷
|
2卷引用:2016-2017学年湖南省益阳市箴言中学高一下学期3月月考化学试卷
解题方法
10 . 如表列出了①~⑥六种元素在元素周期表中的位置.
请回答下列问题:
(1)①、②、③三种元素相比较,非金属性最强的是____ (填写元素符号);
(2)元素①③⑥的氢化物的分子式分别是_____ ;_______ ;_____ .
(3)④、⑤两种元素的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是______________________________ .
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ |
请回答下列问题:
(1)①、②、③三种元素相比较,非金属性最强的是
(2)元素①③⑥的氢化物的分子式分别是
(3)④、⑤两种元素的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是
您最近一年使用:0次
2016-12-09更新
|
313次组卷
|
2卷引用:湖南省2016-2017学年高二普通高中学业水平考试信息模拟卷(四)化学试题



