解题方法
1 . 如图为元素周期表的一部分。回答下列问题:
(1)O的原子序数是___________ 。
(2)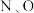 和F三种元素中,非金属性最强的是
和F三种元素中,非金属性最强的是___________ (填元素符号)。
(3)F和 的原子半径大小:F
的原子半径大小:F___________  (填“
(填“ ”或“
”或“ ”)。
”)。
(4) 在氢气中燃烧的化学方程式为
在氢气中燃烧的化学方程式为___________ 。
| N | O | F |
| Cl |
(2)
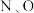 和F三种元素中,非金属性最强的是
和F三种元素中,非金属性最强的是(3)F和
 的原子半径大小:F
的原子半径大小:F (填“
(填“ ”或“
”或“ ”)。
”)。(4)
 在氢气中燃烧的化学方程式为
在氢气中燃烧的化学方程式为
您最近一年使用:0次
名校
解题方法
2 . 下表列出了A~R9种元素在周期表中的位置。请回答下列问题。
(1)在这9种元素中,最外层电子数为1的元素为_____ (填元素符号),化学性质最不活泼的是_____ (填元素符号)。
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应水化物反应的离子方程式是_____ 。
(3)F、A、D三种元素的离子半径由大到小的顺序排列为_____ (填离子符号)。
(4)用电子式表示由C和H组成的化合物的形成过程:_____ 。
(5)由E和F形成的氧化物通入足量的B的氢氧化物中,其离子反应方程式为_____ 。
(6)由E和G所形成的化合物中所含有的化学键为_____ 。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应水化物反应的离子方程式是
(3)F、A、D三种元素的离子半径由大到小的顺序排列为
(4)用电子式表示由C和H组成的化合物的形成过程:
(5)由E和F形成的氧化物通入足量的B的氢氧化物中,其离子反应方程式为
(6)由E和G所形成的化合物中所含有的化学键为
您最近一年使用:0次
2023-12-24更新
|
432次组卷
|
2卷引用:湖南省长郡中学2023-2024学年高一上学期选科适应性调研检测化学试题
解题方法
3 . 如表为元素周期表中的一部分,请回答下列问题:
(1)写出⑤元素的名称_______ 。
(2)写出③元素的离子结构示意图_______ 。
(3)④单质与水发生反应的离子方程式_______ 。
(4)写出⑥元素在周期表中的位置_______ 。
(5)比较单质氧化性的强弱⑤_______ ⑦(填”>”、”<”或”=”)。
| 项目 | I A | II A | III A | IV A | V A | VI A | VII A |
| 二 | ① | ② | ③ | ||||
| 三 | ④ | ⑤ | |||||
| 四 | ⑥ | ⑦ |
(1)写出⑤元素的名称
(2)写出③元素的离子结构示意图
(3)④单质与水发生反应的离子方程式
(4)写出⑥元素在周期表中的位置
(5)比较单质氧化性的强弱⑤
您最近一年使用:0次
名校
4 . 下表是元素周期表的一部分,回答相关问题。
(1)元素①和⑦形成的化合物的化学式为___________ 。
(2)元素⑥的过氧化物的电子式___________ ,其最高价氧化物对应的水化物中含有的化学键类型为___________ 。
(3)元素⑥、⑦、⑧、⑨的简单离子半径由大到小的顺序为___________ (用离子符号表示);元素④、⑤、⑧、⑨的最简单氢化物中稳定性最强的是___________ (填化学式)。
(4)最近,德国科学家实现了铷原子气体超流体态与绝缘体态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。关于铷的下列说法不正确的是___________ (填序号)。
a.与水反应比钠反应更剧烈
b.单质具有很强的氧化性
c.Rb2O在空气中不会吸收水和二氧化碳
d.Rb2O2能与水剧烈反应并释放氧气
e.RbOH的碱性比同浓度的NaOH溶液弱
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(2)元素⑥的过氧化物的电子式
(3)元素⑥、⑦、⑧、⑨的简单离子半径由大到小的顺序为
(4)最近,德国科学家实现了铷原子气体超流体态与绝缘体态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。关于铷的下列说法不正确的是
a.与水反应比钠反应更剧烈
b.单质具有很强的氧化性
c.Rb2O在空气中不会吸收水和二氧化碳
d.Rb2O2能与水剧烈反应并释放氧气
e.RbOH的碱性比同浓度的NaOH溶液弱
您最近一年使用:0次
2023-06-15更新
|
112次组卷
|
2卷引用:湖南省湘潭县一中2022-2023学年高一下学期期末考试化学试题
5 . 根据元素周期表中1~20号元素的性质和递变规律,回答下列问题:
(1)原子序数为8的元素名称是______ ;
(2)硫化氢的电子式是______ ;
(3)氟(F)和氯(Cl)均为第ⅦA族元素,则两种元素的非金属性强弱是F______ (填“>”或“<”)Cl;
(4)钾和硫两种元素的最高价氧化物对应的水化物相互反应的离子方程式为____________ 。
(1)原子序数为8的元素名称是
(2)硫化氢的电子式是
(3)氟(F)和氯(Cl)均为第ⅦA族元素,则两种元素的非金属性强弱是F
(4)钾和硫两种元素的最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
6 . 化学是一门实用性很强的科学。请根据题意填空:
(1)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。据此他判断汤汁中含有______ (填“钠”或“钾”)元素;
(2)在金属元素中,有一类金属既可单独使用,也可用于生产合金。在合金中加入该类金属,能大大改善合金的性能,因而,该类金属又被称为“冶金工业的维生素”。则该类金属是______ (填“稀土金属”或“碱土金属”);
(3)中国古代最早的指南针“司南”,其具有磁性作用是因为主要含有______ (填“Fe2O3”或“Fe3O4”)。
(1)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。据此他判断汤汁中含有
(2)在金属元素中,有一类金属既可单独使用,也可用于生产合金。在合金中加入该类金属,能大大改善合金的性能,因而,该类金属又被称为“冶金工业的维生素”。则该类金属是
(3)中国古代最早的指南针“司南”,其具有磁性作用是因为主要含有
您最近一年使用:0次
名校
7 . 根据元素周期表中1~18号元素的性质和递变规律,回答下列问题。
(1)原子序数为17的元素符号是___________ ;
(2)二氧化碳中所含两种元素的原子半径大小:C___________ O(填“>”或“<”);
(3)硫和氯均为第三周期元素,则两种元素的气态氢化物的稳定性强弱:
___________ HCl(填“>”或“<”);
(4)氮元素的简单气态氢化物与其最高价氧化物对应的水化物相互反应的离子方程式为___________ 。
(1)原子序数为17的元素符号是
(2)二氧化碳中所含两种元素的原子半径大小:C
(3)硫和氯均为第三周期元素,则两种元素的气态氢化物的稳定性强弱:

(4)氮元素的简单气态氢化物与其最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
名校
8 . 下表是元素周期表的一部分。
(1) 和
和 互为
互为___________ ,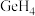 分子的空间结构为
分子的空间结构为___________ 。
(2) 为
为___________ (填“共价”或“离子”)化合物,该物质可作为野外工作的应急燃料,其与水反应的化学方程式为___________ 。
(3)能作为氯、溴、碘元素非金属性递变规律的判断依据是___________。
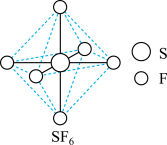
(4) 分子的空间结构为正八面体形,如图所示。
分子的空间结构为正八面体形,如图所示。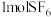 中含有
中含有___________ 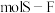 键,它的一氯代物
键,它的一氯代物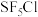 有
有___________ 种。
(5)研究发现,给小鼠喂食适量硒酸钠 可减轻重金属铊引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为
可减轻重金属铊引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | H | ||||||
| 二 | C | O | F | ||||
| 三 | Na | Si | S | Cl | |||
| 四 | Ca | Ge | Se | Br |
 和
和 互为
互为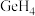 分子的空间结构为
分子的空间结构为(2)
 为
为(3)能作为氯、溴、碘元素非金属性递变规律的判断依据是___________。
A. , , , , 的熔点 的熔点 | B. , , , , 的氧化性 的氧化性 |
C. 、 、 、 、 的热稳定性 的热稳定性 | D. 、 、 、 、 的酸性 的酸性 |
 分子的空间结构为正八面体形,如图所示。
分子的空间结构为正八面体形,如图所示。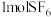 中含有
中含有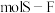 键,它的一氯代物
键,它的一氯代物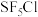 有
有
(5)研究发现,给小鼠喂食适量硒酸钠
 可减轻重金属铊引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为
可减轻重金属铊引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为
您最近一年使用:0次
名校
9 . 如图是元素周期表的一部分,表中列出了八种元素的位置:
请回答下列问题:
(1)①元素的简单氢化物的电子式为______ 。
(2)在元素①-⑧中,金属性最强的元素是______ (填元素符号),最高价含氧酸酸性最强的是_____ (填化学式)。
(3)②、③、④三种元素的原子半径由大到小的顺序是_____ (填元素符号),③和⑦的简单氢化物的稳定性较强的是_____ (填化学式)。
(4)④和⑤所形成的化合物属于_____ (填“离子”或“共价”)化合物。
(5)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为_____ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ||||||||
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①元素的简单氢化物的电子式为
(2)在元素①-⑧中,金属性最强的元素是
(3)②、③、④三种元素的原子半径由大到小的顺序是
(4)④和⑤所形成的化合物属于
(5)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为
您最近一年使用:0次
2023-04-09更新
|
478次组卷
|
2卷引用:湖南省岳阳教研联盟2022-2023学年高一下学期联考联评化学试题
名校
10 . 下图为元素周期表的一部分,请参照① ⑨在表中的位置,回答下列问题:
⑨在表中的位置,回答下列问题:
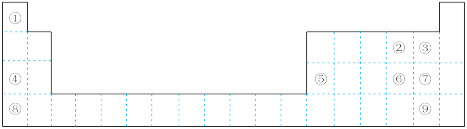
(1)最高价氧化物对应水化物碱性最强的是_______ (填化学式),氢化物热稳定性最强的是_______ (填电子式)。
(2)②③④的原子半径从大到小的顺序是_______ (填元素符号)。④⑤⑧的阳离子中氧化性最强的是_______ (填离子符号)。
(3)元素⑥的非金属性比⑦_______ (填“强”或“弱”),请从原子结构的角度解释:_______ 。
(4)现在含有元素硒( )的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多
)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多 个电子层,硒在周期表中的位置为
个电子层,硒在周期表中的位置为_______ ,则下列叙述中正确的是_______ 。
A.原子序数为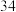
B.气态氢化物的稳定性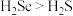
C. 不能与氢氧化钠反应
不能与氢氧化钠反应
D. 既有氧化性又有还原性
既有氧化性又有还原性
(5)①和④可形成 型离子化合物,该离子化合物的电子式为
型离子化合物,该离子化合物的电子式为_______ ,其与水反应放出气体的化学方程式为_______ 。
 ⑨在表中的位置,回答下列问题:
⑨在表中的位置,回答下列问题:
(1)最高价氧化物对应水化物碱性最强的是
(2)②③④的原子半径从大到小的顺序是
(3)元素⑥的非金属性比⑦
(4)现在含有元素硒(
 )的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多
)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多 个电子层,硒在周期表中的位置为
个电子层,硒在周期表中的位置为A.原子序数为
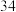
B.气态氢化物的稳定性
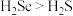
C.
 不能与氢氧化钠反应
不能与氢氧化钠反应D.
 既有氧化性又有还原性
既有氧化性又有还原性(5)①和④可形成
 型离子化合物,该离子化合物的电子式为
型离子化合物,该离子化合物的电子式为
您最近一年使用:0次
2023-02-05更新
|
278次组卷
|
2卷引用:湖南省郴州市苏仙区多校2022-2023学年高一上学期期末线上联考化学试题



