解题方法
1 . 下表列出了9种元素在元素周期表中的位置示意图。
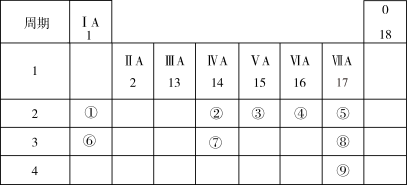
请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_______________ 。
(2)画出元素⑧形成的简单离子的结构示意图_______________ 。
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_______________ 。
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是_______________ 。
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是______________ (填化学式),写出元素⑤的单质与水反应的化学方程式_______________ ,写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式_______________ 。

请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是
(2)画出元素⑧形成的简单离子的结构示意图
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是
您最近一年使用:0次
名校
解题方法
2 . 根据所学知识,回答下列问题:
(1)写出C元素在元素周期表中的位置:___________ ;
(2)写出C与浓硫酸反应的化学方程式:___________ ;
(3)将胆矾晶体投入浓硫酸中,可观察到___________ ,体现了浓硫酸的___________ 性;
(4)除下列气体中的杂质所需要的试剂,括号内为杂质: (HCl)
(HCl)___________ ;NO( )
)___________
(1)写出C元素在元素周期表中的位置:
(2)写出C与浓硫酸反应的化学方程式:
(3)将胆矾晶体投入浓硫酸中,可观察到
(4)除下列气体中的杂质所需要的试剂,括号内为杂质:
 (HCl)
(HCl) )
)
您最近一年使用:0次
解题方法
3 . 下表列出了 九种元素在周期表中的位置,根据要求回答下列问题:
九种元素在周期表中的位置,根据要求回答下列问题:

(1)f的名称是_______ ,d的元素符号是_______ ;
(2)a在周期表中的位置是_______ ;
(3)h的原子结构示意图是_______ ;
(4)e、g、i按原子半径由大到小的顺序排列为_______ (填元素符号);
(5)c与h相比非金属性较强的是_______ (填元素符号),h的氢化物与i的氢化物相比,稳定性较弱的是_______ (填化学式);
(6)e的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物,在水溶液中反应的离子方程式为_______ ;
(7)g的单质与氧化铁在高温条件下反应的化学方程式为_______ ;
(8)i的氢化物的电子式为_______ 。
 九种元素在周期表中的位置,根据要求回答下列问题:
九种元素在周期表中的位置,根据要求回答下列问题:
(1)f的名称是
(2)a在周期表中的位置是
(3)h的原子结构示意图是
(4)e、g、i按原子半径由大到小的顺序排列为
(5)c与h相比非金属性较强的是
(6)e的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物,在水溶液中反应的离子方程式为
(7)g的单质与氧化铁在高温条件下反应的化学方程式为
(8)i的氢化物的电子式为
您最近一年使用:0次
名校
4 . Ⅰ.黑火药爆炸的化学方程式为: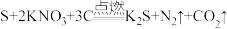 。回答下列问题:
。回答下列问题:
(1)硫元素在周期表的位置是_______ 。氨气的电子式_______ 。
(2)用电子式表示化合物 的形成过程为
的形成过程为_______ 。
(3)上述氧化产物结构式为_______ 。
(4)硫、氮及其化合物中,下列比较正确的是_______(选填编号)。
Ⅱ.如图列出了①~⑩十种元素在周期表中的位置:
请回答下列问题:
(5)上述元素中,M层电子数最多的是_______ (填元素名称)。
(6)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(7)下列可以比较⑤、⑥两元素金属性强弱的实验是_______(填字母)。
(8)元素⑦的最高价氧化物对应的水化物与元素⑨的最简单氢化物的水溶液反应的离子方程式_______ 。
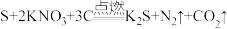 。回答下列问题:
。回答下列问题:(1)硫元素在周期表的位置是
(2)用电子式表示化合物
 的形成过程为
的形成过程为(3)上述氧化产物结构式为
(4)硫、氮及其化合物中,下列比较正确的是_______(选填编号)。
A.原子半径: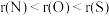 | B.热稳定性: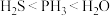 |
C.溶解度: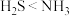 | D.微粒种类:氢硫酸<氨水 |
Ⅱ.如图列出了①~⑩十种元素在周期表中的位置:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
请回答下列问题:
(5)上述元素中,M层电子数最多的是
(6)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是
(7)下列可以比较⑤、⑥两元素金属性强弱的实验是_______(填字母)。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将形状、大小相同的这两种元素的单质分别与等体积20℃的水反应 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
您最近一年使用:0次
5 . 下表为长式周期表的一部分,其中的编号代表对应的元素。
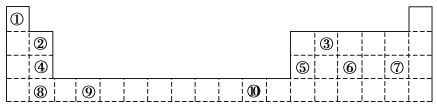
请回答下列问题:
(1)表中属于d区元素的是___________ (填元素符号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为___________ ;③和⑦形成的一种常见溶剂的化学式为___________ 。
(3)元素④的第一电离能___________ 元素⑤(选填“>”、“=”或“<”)的第一电离能;元素⑥的电负性___________ 元素⑦(选填“>”、“=”或“<”)的电负性。
(4)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:___________

请回答下列问题:
(1)表中属于d区元素的是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
(3)元素④的第一电离能
(4)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次
6 . 元素周期表中前7周期的元素数目如表所示(假设第7周期已排满):
(1)第6、7周期比第4、5周期多了14种元素,其原因是_______ 。
(2)周期表中_______ 族所含元素最多。
(3)请分析周期数与元素数目的关系后预言第8周期最多可能含有的元素种数为_______ 。
A.18 B.32 C.50 D.64
(4)如将现行族号取消,并按从左到右顺序将原有的各族依次称为1~18纵列,则32号元素锗(Ge)位于第_______ 周期第_______ 纵列。
| 周期 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元素种数 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
(1)第6、7周期比第4、5周期多了14种元素,其原因是
(2)周期表中
(3)请分析周期数与元素数目的关系后预言第8周期最多可能含有的元素种数为
A.18 B.32 C.50 D.64
(4)如将现行族号取消,并按从左到右顺序将原有的各族依次称为1~18纵列,则32号元素锗(Ge)位于第
您最近一年使用:0次
解题方法
7 . 用周期表中特殊位置的短周期元素填空
(1)族序数等于周期数的元素:___________ ;
(2)族序数等于周期数2倍的元素:___________ ;
(3)族序数等于周期数3倍的元素:___________ ;
(4)周期数是族序数2倍的元素:___________ ;
(5)周期数是族序数3倍的元素是:___________ ;
(6)最高正价不等于族序数的元素是:___________ 。
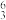 Li、
Li、 Li、
Li、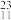 Na、
Na、 Mg、
Mg、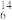 C、
C、 N中,
N中,
(7)___________ 和___________ 互为同位素;
(8)___________ 和___________ 的质量数相等,但不能互称同位素;
(1)族序数等于周期数的元素:
(2)族序数等于周期数2倍的元素:
(3)族序数等于周期数3倍的元素:
(4)周期数是族序数2倍的元素:
(5)周期数是族序数3倍的元素是:
(6)最高正价不等于族序数的元素是:
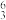 Li、
Li、 Li、
Li、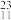 Na、
Na、 Mg、
Mg、 C、
C、 N中,
N中,(7)
(8)
您最近一年使用:0次
名校
解题方法
8 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
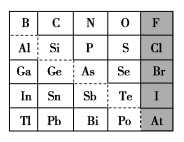
(1)元素 在元素周期表中的位置为第
在元素周期表中的位置为第______ 周期第______ 族。
(2) 的最高化合价为
的最高化合价为______ , 的最高价氧化物对应的水化物的化学式为
的最高价氧化物对应的水化物的化学式为______ , 的最高价氧化物为
的最高价氧化物为______ 。
(3)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是______ 元素(填元素符号)。
②酸性:
______ (填“>”“<”或“=”,下同) 。
。
③氢化物的还原性:
______  。
。
④原子半径:
______  。
。
(4)可在图中分界线(虚线)附近寻找______ (填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料
(5)从下列试剂中选择最佳试剂组合,比较 、
、 的非金属性强弱:
的非金属性强弱:______ 。(可供选择的药品有 固体、稀硫酸、盐酸、饱和
固体、稀硫酸、盐酸、饱和 溶液、饱和
溶液、饱和 溶液、硅酸钠溶液)
溶液、硅酸钠溶液)

(1)元素
 在元素周期表中的位置为第
在元素周期表中的位置为第(2)
 的最高化合价为
的最高化合价为 的最高价氧化物对应的水化物的化学式为
的最高价氧化物对应的水化物的化学式为 的最高价氧化物为
的最高价氧化物为(3)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是
②酸性:

 。
。③氢化物的还原性:

 。
。④原子半径:

 。
。(4)可在图中分界线(虚线)附近寻找
A.优良的催化剂 B.半导体材料 C.合金材料
(5)从下列试剂中选择最佳试剂组合,比较
 、
、 的非金属性强弱:
的非金属性强弱: 固体、稀硫酸、盐酸、饱和
固体、稀硫酸、盐酸、饱和 溶液、饱和
溶液、饱和 溶液、硅酸钠溶液)
溶液、硅酸钠溶液)
您最近一年使用:0次
2020-09-08更新
|
1564次组卷
|
6卷引用:内蒙古通辽市开鲁县第一中学2022-2023学年高一上学期期末考试化学试题
9 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,下图是元素周期表的一部分, 回答下列问题:
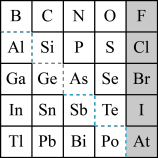
(1)元素Ga在元素周期表中的位置为:________ ;
(2)Sn的最高正价为_______ ,Cl的最高价氧化物对应水化物的化学式为______ ;
(3)根据元素周期律,推断:
①阴影部分元素形成的氢化物中热稳定性最高的是_____ ;(写化学式)
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4_______ H2SeO4 (填“>”、“<”、“=”或“无法比较”);
③氢化物的还原性:H2O_______ H2S (填“>”、“<”、“=”或“无法比较”);
④原子半径比较: N______ Si (填“>”、“<”、“=”或“无法比较”);
(4)可在图中分界线(虚线部分)附近寻找_______ (填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素形成的氢化物中热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4
③氢化物的还原性:H2O
④原子半径比较: N
(4)可在图中分界线(虚线部分)附近寻找
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药
您最近一年使用:0次
10 . 下表是元素周期表的一部分。回答下列问题:
(1)元素①~⑩中,金属性最强的元素的原子结构示意图为__________ 。
(2)写出元素②常见的一种同素异形体的名称:____________ 。
(3)元素⑦的单质与元素⑧氢化物的水溶液反应的离子方程式为___________ 。
(4)元素⑥的最高价氧化物对应的水化物的电子式为_________ ,元素⑩的单质的氧化性比元素⑤的单质的氧化性__________ (填“强”或“弱”)。
(5)元素④、⑧可组成多种微粒,其中可作为饮用水消毒剂的化合物分子是________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | |||||||||||||||
| ⑨ | ⑩ |
(1)元素①~⑩中,金属性最强的元素的原子结构示意图为
(2)写出元素②常见的一种同素异形体的名称:
(3)元素⑦的单质与元素⑧氢化物的水溶液反应的离子方程式为
(4)元素⑥的最高价氧化物对应的水化物的电子式为
(5)元素④、⑧可组成多种微粒,其中可作为饮用水消毒剂的化合物分子是
您最近一年使用:0次



