解题方法
1 . 作为元素周期律表现形式的元素周期表,反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表中的一部分,请参照以下六种元素(每种字母分别代表一种元素)在表中的位置,回答下列问题:
回答下列问题:
(1)M的原子结构示意图为________ 。
(2)M与Z可形成一种离子化合物 ,其电子式为
,其电子式为________ 。
(3)原子半径:X________ Z(填“大于”或“小于”,下同);简单氢化物的稳定性:Z________ N。
(4)X、Y的最高价氧化物对应水化物的酸性:________ 
________ (填化学式)。
(5)由M和Z组成的一种化合物可用作核潜艇中氧气的来源,该化合物的名称是________ ,其中含有的化学键类型是________ 、________ 。
| 族 周期 | ⅠA | 0 | ||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | X | Y | Z | |||||
3 | M | N | W |
(1)M的原子结构示意图为
(2)M与Z可形成一种离子化合物
 ,其电子式为
,其电子式为(3)原子半径:X
(4)X、Y的最高价氧化物对应水化物的酸性:

(5)由M和Z组成的一种化合物可用作核潜艇中氧气的来源,该化合物的名称是
您最近一年使用:0次
2 . C、N、O、F等元素的化合物在航天、美容、食品等多领域中有广泛的用途,请回答:
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为______ ;N、O、F的第一电离能由大到小的顺序为_____ (用元素符号表示)。
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为______ 晶体(填晶体类型)。
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第______ 周期第______ 族。
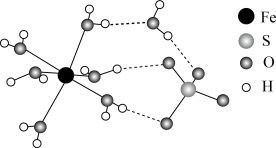
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO 的作用类型分别是
的作用类型分别是______ 、______ 。
A.离子键 B.配位键 C.氢键 D.金属键 中键角的大小并解释原因:
中键角的大小并解释原因:______ 。
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO
 的作用类型分别是
的作用类型分别是A.离子键 B.配位键 C.氢键 D.金属键
 中键角的大小并解释原因:
中键角的大小并解释原因:
您最近一年使用:0次
2023-04-20更新
|
188次组卷
|
2卷引用:山西省大同市2022-2023学年高二下学期期中考试化学试题
解题方法
3 . 核酸检测是常态化疫情防控的手段之一,核酸采样管中的红色液体是病毒核酸保存液,其成分之一的盐酸胍[结构简式为 ]的主要作用是使蛋白质变性并抑制酶活性。请回答以下问题:
]的主要作用是使蛋白质变性并抑制酶活性。请回答以下问题:
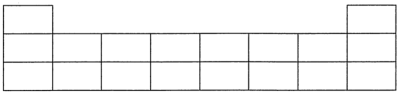
(1)下表是元素周期表中的短周期部分,请将盐酸胍中四种元素的元素符号填写在表中的相应位置。_____
(2)N位于元素周期表的第_______ 周期,第_______ 族。
(3)推测C、N的非金属性强弱:_______ 大于_______ 。
(4)HCl中所含化学键属于_______ ,请用电子式表示HCl的形成过程:_______ 。
 ]的主要作用是使蛋白质变性并抑制酶活性。请回答以下问题:
]的主要作用是使蛋白质变性并抑制酶活性。请回答以下问题:(1)下表是元素周期表中的短周期部分,请将盐酸胍中四种元素的元素符号填写在表中的相应位置。

(2)N位于元素周期表的第
(3)推测C、N的非金属性强弱:
(4)HCl中所含化学键属于
您最近一年使用:0次
名校
4 . A~R 9种元素在元素周期表中的位置如图。
回答下列问题:
(1)E的原子结构示意图为_______ 。
(2)常温下, 的状态为
的状态为_______ (填“液”、“固”或“气”)态。
(3)写出单质A与 在加热条件下发生反应的化学方程式:
在加热条件下发生反应的化学方程式:_______ 。
(4)化合物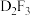 与NaOH溶液反应的离子方程式为
与NaOH溶液反应的离子方程式为_______ 。
(5)H元素形成的单质的用途有_______ (填一种即可)。
(6)最高价氧化物对应水化物的碱性:C_______ (填“>”、“<”或“=”)A,判断的理由为_______ 。
(7)化合物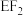 所含分子中的电子总数为
所含分子中的电子总数为_______ ,与其具有相同电子数的化合物分子为_______ (填标号)。
a. b.
b. c.
c. d.
d.
| 周期 | 族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | A | E | F | |||||
| 3 | C | D | G | H | ||||
| 4 | B | R | ||||||
(1)E的原子结构示意图为
(2)常温下,
 的状态为
的状态为(3)写出单质A与
 在加热条件下发生反应的化学方程式:
在加热条件下发生反应的化学方程式:(4)化合物
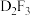 与NaOH溶液反应的离子方程式为
与NaOH溶液反应的离子方程式为(5)H元素形成的单质的用途有
(6)最高价氧化物对应水化物的碱性:C
(7)化合物
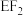 所含分子中的电子总数为
所含分子中的电子总数为a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次
2023-02-08更新
|
145次组卷
|
3卷引用:山西省忻州市河曲县中学校2022-2023学年高一下学期开学考试化学试题
名校
解题方法
5 . 金属Na、Mg、Al有广泛的应用。
(1)Al在元素周期表中的位置是______ 。
(2)金属镁可以用来生产金属铀(元素符号是U): ,该反应中,作为还原剂的物质是
,该反应中,作为还原剂的物质是______ (填化学式,下同),被还原的物质是______ 。
(3)为比较Na、Mg、Al的金属性,进行了如下实验(金属固体的表面积都相同):
由实验1和实验2得出的结论是:金属性,______ >______ >______ (填元素符号),用原子结构理论解释:同周期元素从左到右,______ 。
(4)写出Na和Al最高价氧化物的水化物相互反应的离子反应方程式______ 。
(1)Al在元素周期表中的位置是
(2)金属镁可以用来生产金属铀(元素符号是U):
 ,该反应中,作为还原剂的物质是
,该反应中,作为还原剂的物质是(3)为比较Na、Mg、Al的金属性,进行了如下实验(金属固体的表面积都相同):
| 实验1 | 实验2 |
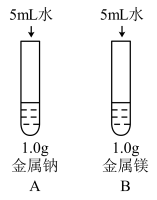 |  |
| 钠与水反应剧烈,镁与水反应缓慢 | 镁与盐酸反应剧烈,铝与盐酸反应缓慢 |
由实验1和实验2得出的结论是:金属性,
(4)写出Na和Al最高价氧化物的水化物相互反应的离子反应方程式
您最近一年使用:0次
2022-12-14更新
|
92次组卷
|
2卷引用:山西省太原市进山中学校2022-2023学年高一上学期期末考试化学试题
解题方法
6 . 下表是元素周期表的一部分,表中的每个编号代表一种短周期元素,回答下列问题:
(1)①和③两种元素形成化合物的电子式为___________ 。
(2)④、⑤、⑥三种元素的最高价氧化物对应水化物的碱性由强到弱的顺序为___________ (用化学式表示)。
(3)①和⑧两种元素按原子个数比2∶1组成的化合物中含有的化学键为___________ 。
(4)元素⑥的单质与①、③、④三种元素组成化合物的溶液反应的离子方程式为___________ 。
(5)元素②的一种氧化物具有还原性,可以冶炼生铁,写出其反应的化学方程式___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①和③两种元素形成化合物的电子式为
(2)④、⑤、⑥三种元素的最高价氧化物对应水化物的碱性由强到弱的顺序为
(3)①和⑧两种元素按原子个数比2∶1组成的化合物中含有的化学键为
(4)元素⑥的单质与①、③、④三种元素组成化合物的溶液反应的离子方程式为
(5)元素②的一种氧化物具有还原性,可以冶炼生铁,写出其反应的化学方程式
您最近一年使用:0次
7 . 下表显示了元素周期表中短周期的一部分,D、E、G、Q、M、X代表6种短周期元素,请回答以下问题。
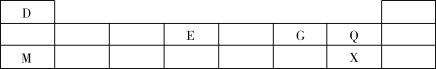
(1)E在元素周期表中的位置是第___________ 周期,第___________ 族,其原子结构示意图为___________ 。
(2)G的元素符号是___________ ,M的元素符号是___________ ,二者原子半径的关系是:G___________ M(填“>”“=”或“<”)。
(3)由M、X组成的化合物的电子式为___________ (用元素符号表示,下同),它属于___________ 化合物(填“离子”或“共价”)。
(4)用电子式表示DX的形成过程___________ ,DX中所含化学键的类型是___________ 。
(5)上述6种元素中,非金属性最强的是___________ 。

(1)E在元素周期表中的位置是第
(2)G的元素符号是
(3)由M、X组成的化合物的电子式为
(4)用电子式表示DX的形成过程
(5)上述6种元素中,非金属性最强的是
您最近一年使用:0次
名校
8 . 下表是元素周期表的一部分,请用化学符号回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为___________ 。
(2)②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是___________ ,最高价氧化物的水化物中酸性最强的是___________ 。
(3)第三周期元素形成的简单离子中半径最小的微粒是___________ ,写出该元素的单质分别与⑥、⑩最高价氧化物的水化物反应的离子方程式___________ 、___________ 。
| 主族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是
(3)第三周期元素形成的简单离子中半径最小的微粒是
您最近一年使用:0次
2021-12-06更新
|
1078次组卷
|
4卷引用:山东省“学情空间”区域教研共同体2022-2023学年高一上学期12月联考(人教版) 化学试题
山东省“学情空间”区域教研共同体2022-2023学年高一上学期12月联考(人教版) 化学试题(已下线)专题4.2.1 元素性质的周期性变化规律(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)浙江省舟山市舟山中学2021-2022学年高一下学期开学考试化学试题安徽省芜湖市第一中学2022-2023学年高一上学期选科分班考试化学试题
9 . 某元素原子的电子排布式为[Ar]3d104s24p1,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:
(1)该元素处于元素周期表的第_______ 周期,
(2)该元素处于元素周期表的第_______ 族,
(3)试推测该元素处于元素周期表的_______ 区,
(1)该元素处于元素周期表的第
(2)该元素处于元素周期表的第
(3)试推测该元素处于元素周期表的
您最近一年使用:0次
2021-05-30更新
|
845次组卷
|
4卷引用:山西省浑源县第七中学2020-2021学年高二下学期第一次月考化学试题
山西省浑源县第七中学2020-2021学年高二下学期第一次月考化学试题(已下线)1.2.1 原子结构与元素周期表(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)第1.2.1讲 原子结构与元素周期表-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)重庆第二十三中学校2021-2022学年高二下学期第一次月考化学试题
10 . 元素周期表的建立是化学发展史上重要的里程碑之一,它揭示了元素之间的内在联系。如图是元素周期表的短周期示意图,相应方格中每个序号代表处于该位置的一种元素。
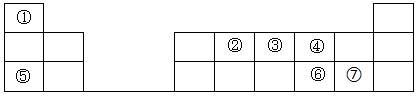
请回答下列问题:
(1)元素①的名称为___ 。
(2)元素③的最高价氧化物的水化物为___ (填化学式)
(3)⑥和⑦两种元素的气态氢化物中稳定性较强的是___ (填化学式)。
(4)②和④两种元素形成的常见气态化合物中化学键类型为___ 。
(5)⑤和⑦两种元素形成的化合物的电子式为___ 。

请回答下列问题:
(1)元素①的名称为
(2)元素③的最高价氧化物的水化物为
(3)⑥和⑦两种元素的气态氢化物中稳定性较强的是
(4)②和④两种元素形成的常见气态化合物中化学键类型为
(5)⑤和⑦两种元素形成的化合物的电子式为
您最近一年使用:0次



