1 . 下表是元素周期表的一部分,请根据表中的信息回答下列问题:
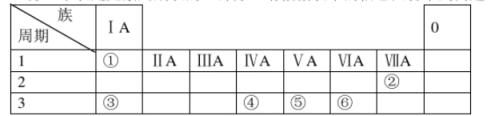
(1)元素①→⑥中金属性最强的是___________ (填元素符号)
(2)④⑤⑥三种元素分别对应的最高价氧化物的水化物酸性由强到弱的顺序是_______ (填化学式)
(3)比较②③的原子半径:②___________ ③(填>或<)
(4)元素周期律中某些区域的一些元素可用于制造半导体材料,这些元素常常位于周期表中______ 的分界线附近

(1)元素①→⑥中金属性最强的是
(2)④⑤⑥三种元素分别对应的最高价氧化物的水化物酸性由强到弱的顺序是
(3)比较②③的原子半径:②
(4)元素周期律中某些区域的一些元素可用于制造半导体材料,这些元素常常位于周期表中
您最近一年使用:0次
2021-05-25更新
|
434次组卷
|
2卷引用:山西省2020年普通高中学业水平考试化学试题
解题方法
2 . 科学家们用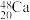 原子轰击某种铬原子,得到了
原子轰击某种铬原子,得到了 原子。
原子。
(1)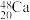 原子的核外电子数是
原子的核外电子数是_______ ,中子数是_______ 。
(2) 的原子结构示意图是
的原子结构示意图是 ,其中的x=
,其中的x=_______ ,y=_______ 。 位于元素周期表的第
位于元素周期表的第_______ 周期,第_______ 族,与它属于同族的一种元素是_______ 。
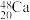 原子轰击某种铬原子,得到了
原子轰击某种铬原子,得到了 原子。
原子。(1)
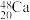 原子的核外电子数是
原子的核外电子数是(2)
 的原子结构示意图是
的原子结构示意图是 ,其中的x=
,其中的x= 位于元素周期表的第
位于元素周期表的第
您最近一年使用:0次
3 . 图中反应①是制备SiH4的一种方法,其副产物MgCl2·6NH3是优质的镁资源。回答下列问题:

(1)Si在元素周期表中的位置是______ ,NH3的电子式为_______ 。
(2)A2B的化学式为______ ,上图中可以循环使用的物质有______ 。
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料:______ (填化学式),其中含有的化学键类型是________ 。
(4)单质硼可用于生成具有优良抗冲击性能的硼钢。以硼酸(H3BO3)和金属镁为原料在加热条件下制备单质硼,用化学方程式表示其制备过程:________ 、___________ 。

(1)Si在元素周期表中的位置是
(2)A2B的化学式为
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料:
(4)单质硼可用于生成具有优良抗冲击性能的硼钢。以硼酸(H3BO3)和金属镁为原料在加热条件下制备单质硼,用化学方程式表示其制备过程:
您最近一年使用:0次
名校
解题方法
4 . 如表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在这些元素中,金属性最强的元素是__ ;
(2)化学性质最不活泼的元素其原子的原子结构示意图为__ ;
(3)元素的最高价氧化物对应的水化物中酸性最强的是__ ,碱性最强的是__ ,呈两性的氢氧化物是__ ;
(4)在③~⑦元素中,原子半径最大的是__ ;
(5)在⑦与⑩的单质中,化学性质较活泼的是____ ,可用什么化学反应说明该事实(写出反应的化学方程式):____ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(1)在这些元素中,金属性最强的元素是
(2)化学性质最不活泼的元素其原子的原子结构示意图为
(3)元素的最高价氧化物对应的水化物中酸性最强的是
(4)在③~⑦元素中,原子半径最大的是
(5)在⑦与⑩的单质中,化学性质较活泼的是
您最近一年使用:0次
5 . A、B、C、D四种元素在元素周期表中的位置如图所示。

请回答下列问题:
(1)A的元素名称是___ ,它在元素周期表第___ 周期,第___ 族。
(2)A、B、C相比,其原子半径由大到小的顺序是___ (用元素符号表示,下同)。
(3)C与D相比,非金属性较强的是___ ,能证明这一结论的事实是___ (用化学方程式表示)。

请回答下列问题:
(1)A的元素名称是
(2)A、B、C相比,其原子半径由大到小的顺序是
(3)C与D相比,非金属性较强的是
您最近一年使用:0次
名校
解题方法
6 . “阅读”、“质疑”、“解惑”是重要的学习方法,请回答下列问题:
(1)在元素周期表中氯元素与溴元素被置于同一主族,从原子结构分析,原因是___ ;氯元素与硫元素被置于同一周期,从原子结构分析,原因是___ 。
(2)甲同学将氯气通入硫化钠(Na2S)的溶液中,观察到产生淡黄色沉淀,反应的化学反应方程式为___ ,得出的结论是Cl-的还原性___ S2-(填“强于”或“弱于”)。
(3)甲同学通过“FeCl3和FeBr3溶液存在”这一事实推测“FeI3”溶液存在,但查阅资料后发现FeI3溶液不存在,可能的原因是___ 。
(4)甲同学将氟气通入氯化钠溶液并未出现“溶液颜色明显变化”的预测现象,可能的原因是___ 。
(1)在元素周期表中氯元素与溴元素被置于同一主族,从原子结构分析,原因是
(2)甲同学将氯气通入硫化钠(Na2S)的溶液中,观察到产生淡黄色沉淀,反应的化学反应方程式为
(3)甲同学通过“FeCl3和FeBr3溶液存在”这一事实推测“FeI3”溶液存在,但查阅资料后发现FeI3溶液不存在,可能的原因是
(4)甲同学将氟气通入氯化钠溶液并未出现“溶液颜色明显变化”的预测现象,可能的原因是
您最近一年使用:0次
2020-06-08更新
|
81次组卷
|
2卷引用:山西省太原市第五中学2019-2020学年高一下学期5月开学摸底考试化学试题
名校
解题方法
7 . 元素周期表是进行化学研究的重要工具,如图是元素周期表的一部分,其中①~⑨代表9种元素。请回答下列问题:

(1)上述元素中最高价氧化物对应的水化物的酸性最强的是___ (填物质的化学式)。
(2)上述元素中最稳定的简单氢化物是___ (填物质的化学式),请用电子式表示其形成过程:___ ;②④⑥形成的1:1:1型化合物的电子式为___ 。
(3)下列推断正确的是___ (填选项字母)。
A.⑨的单质可能为白色固体
B.⑧的单质能与水剧烈反应生成氢气
C.①、⑥的简单氢化物之间反应的产物中既含离子键又含极性键

(1)上述元素中最高价氧化物对应的水化物的酸性最强的是
(2)上述元素中最稳定的简单氢化物是
(3)下列推断正确的是
A.⑨的单质可能为白色固体
B.⑧的单质能与水剧烈反应生成氢气
C.①、⑥的简单氢化物之间反应的产物中既含离子键又含极性键
您最近一年使用:0次
2020-06-07更新
|
175次组卷
|
3卷引用:山西省太原市第五中学2019-2020学年高一下学期5月开学摸底考试化学试题
名校
8 . 下表是元素周期表一部分,列出了九种元素在周期表中的位置:
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是____________ 。
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是________ (填物质化学式)。写出⑥和⑧的最高价氧化物对应的水化物反应的离子方程式 _______________________________ 。
(3)只由④形成的18电子微粒的电子式________________ 。
(4)写出由①和③形成的离子化合物的化学式____________________________ 。
(5)用电子式表示⑦和⑨形成的化合物的形成过程_________________________________ 。
(6)表中元素③和⑤可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式_________________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
(3)只由④形成的18电子微粒的电子式
(4)写出由①和③形成的离子化合物的化学式
(5)用电子式表示⑦和⑨形成的化合物的形成过程
(6)表中元素③和⑤可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式
您最近一年使用:0次
2020-05-26更新
|
84次组卷
|
2卷引用:山西省朔州市怀仁县大地学校2019-2020学年高一下学期6月月考化学试题
解题方法
9 . (I)俄美科学家联合小组宣布合成出114号元素(FI)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中的位置______________ ,属于金属元素还是非金属元素?____
(2)如果该元素存在最高价氧化物对应的水化物,请写出其化学式___________________ 。
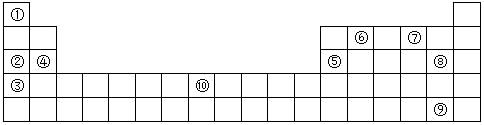
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
(1)元素⑦的氢化物与⑧的单质反应的离子方程式为__________ 。
(2)元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为___________ 。
(3)元素Fe的单质与⑦的氢化物高温下反应的化学方程式为___________ 。
(III)判断以下叙述正确的是__________ 。
部分短周期元素的原子半径及主要化合价
A.L2+、R2-的核外电子数相等
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物一定具有两性
D.氢化物的沸点为HnT>HnR
E. M的单质能与盐酸、NaOH溶液反应放出氢气
(1)该元素在周期表中的位置
(2)如果该元素存在最高价氧化物对应的水化物,请写出其化学式
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:

(1)元素⑦的氢化物与⑧的单质反应的离子方程式为
(2)元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为
(3)元素Fe的单质与⑦的氢化物高温下反应的化学方程式为
(III)判断以下叙述正确的是
部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.L2+、R2-的核外电子数相等
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物一定具有两性
D.氢化物的沸点为HnT>HnR
E. M的单质能与盐酸、NaOH溶液反应放出氢气
您最近一年使用:0次
名校
10 . 据南方日报报道,广东省珠江第二大水系北江流域因当地矿业的开发,造成附近河底沉积物中铊含量严重超标,致使当地人“靠江不饮北江水”。铊(Tl)是某超导体材料的组成元素之一,Tl3+与Ag在酸性介质中发生反应Tl3++2Ag=Tl++2Ag+。
(1)铊(Tl)的原子序数为81,铊在元素周期表中位于第____ 周期第______ 族。
(2)铊与下列某种元素位于同一主族,该元素是________ 。
A. 硼 B. 氮 C. 碳 D. 氟
(3)下列推断正确的是______ (填序号)。
A. 单质的还原性:Tl>Al B. 原子半径:Al>Tl C. 碱性:Al(OH)3>Tl(OH)3
D. 氧化性:Tl3+>Ag+E. Tl+最外层只有1个电子 F. Tl能形成+3价和+1价的化合物
(4)X元素是与铝属于对角线关系的第二周期元素,二者的单质化学性质相似。X单质与浓NaOH溶液反应的化学方程式是________ 。
(1)铊(Tl)的原子序数为81,铊在元素周期表中位于第
(2)铊与下列某种元素位于同一主族,该元素是
A. 硼 B. 氮 C. 碳 D. 氟
(3)下列推断正确的是
A. 单质的还原性:Tl>Al B. 原子半径:Al>Tl C. 碱性:Al(OH)3>Tl(OH)3
D. 氧化性:Tl3+>Ag+E. Tl+最外层只有1个电子 F. Tl能形成+3价和+1价的化合物
(4)X元素是与铝属于对角线关系的第二周期元素,二者的单质化学性质相似。X单质与浓NaOH溶液反应的化学方程式是
您最近一年使用:0次



