名校
1 . 如表所示为元素周期表的前四周期部分,根据图示结合所学知识回答下列问题:
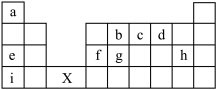
(1)h、i的简单离子半径由大到小的顺序为_______ (填离子符号)。
(2)i、e、f的最高价氧化物对应的水化物的碱性由强到弱的顺序是_______ (填化学式)。
(3)用电子式表示e和h形成离子化合物的过程:________ 。
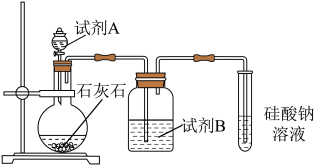
(4)非金属性:b_______ g(填“>”或“<”);以如图装置进行实验比较b、g对应的最高价氧化物对应水化物的酸性,则试剂A为_______ (填试剂名称),试剂B为_______ 。
(5)X处包含_______ 纵列,_______ 个族。
(6)i单质与d的简单氢化物反应的离子方程式为_______ 。

(1)h、i的简单离子半径由大到小的顺序为
(2)i、e、f的最高价氧化物对应的水化物的碱性由强到弱的顺序是
(3)用电子式表示e和h形成离子化合物的过程:
(4)非金属性:b

(5)X处包含
(6)i单质与d的简单氢化物反应的离子方程式为
您最近一年使用:0次
2 . I.我国科学家在铁基高温超导体的研究上取得重大突破,发现了该超导体是由Fe、Ba、As三种元素组成,这为进一步理解超导配对机理及其与电荷密度波的关系提供了重要实验证据。回答下列问题:
(1)As元素属于元素周期表的___________ 区元素,其价电子排布式是___________ 。
(2)基态Fe原子核外电子排布式为___________ 。
Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有___________ 种。
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的___________ 区(用符号填空),原子序数最大的在周期表的第___________ 周期、___________ 族。
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色,为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]2+___________ (填“无”或“有”)颜色。
(1)As元素属于元素周期表的
(2)基态Fe原子核外电子排布式为
Ⅱ.某元素原子的最外电子层只有一个电子,该电子的电子层数n=4。请回答下列问题:
(3)符合上述条件的元素共有
(4)在符合上述条件的元素中,原子序数最小的在元素周期表中的
(5)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色,为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]2+
您最近一年使用:0次
名校
解题方法
3 . 单质硅是制造太阳能电池板的主要原料,制备电池板时还需添加硼、氮、钛、钴、钙等多种化学物质。
请回答下列问题:
(1)基态硼原子的电子排布式为___________ ,下列钴原子的价层电子轨道表示式中,不符合洪特规则的是___________ (填选项字母)。
A.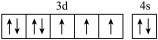 B.
B.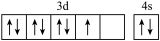
C.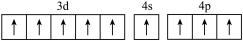 D.
D.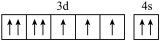
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)钛元素位于元素周期表___________ 区;基态钛原子中,最外层电子的电子云轮廓图为___________ 。
请回答下列问题:
(1)基态硼原子的电子排布式为
A.
 B.
B.
C.
 D.
D.
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为
(3)钛元素位于元素周期表
您最近一年使用:0次
4 . 立方砷化硼具有高载流子迁移率,超越硅的导热、导电性能,有望成为硅基元器件的替代方案,其晶胞结构如图所示,请回答下列问题:
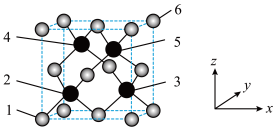
(1)As在元素周期表中的位置是_______ 。As属于_______ 区元素。
(2)该晶胞的化学式为_______ 。2、3、4、5四个原子所围成的空间结构为_______ 形。
(3)晶胞有两个基本要素。
①原子坐标参数,表示晶胞内部各原子的相对位置,图中1号原子的坐标参数为 ,6号原子的坐标参数为
,6号原子的坐标参数为 ,则2号原子的坐标参数为
,则2号原子的坐标参数为_______ 。
②晶胞参数是用来描述晶胞大小和形状的,设该晶胞的晶胞参数为a pm,阿伏加德罗常数为 ,则B、As原子之间的最短距离为
,则B、As原子之间的最短距离为_______ pm,该晶胞的密度为_______  。
。

(1)As在元素周期表中的位置是
(2)该晶胞的化学式为
(3)晶胞有两个基本要素。
①原子坐标参数,表示晶胞内部各原子的相对位置,图中1号原子的坐标参数为
 ,6号原子的坐标参数为
,6号原子的坐标参数为 ,则2号原子的坐标参数为
,则2号原子的坐标参数为②晶胞参数是用来描述晶胞大小和形状的,设该晶胞的晶胞参数为a pm,阿伏加德罗常数为
 ,则B、As原子之间的最短距离为
,则B、As原子之间的最短距离为 。
。
您最近一年使用:0次
名校
5 . 下表列出9种元素在元素周期表(元素周期表只给出部分)中的位置
请回答下列问题:
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的元素符号是_______ 。
(2)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式:_______ 。
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式为_______
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是_______ (填化学式;用“>”连接)。
(5)表中的ⅠA族、ⅡA族元素全部是金属元素,这种判断_______ (填“正确”或“错误”);根据元素周期律,自然界中最强的碱是_______ (填化学式)。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | |||||
| 4 | ⑨ |
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的元素符号是
(2)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式:
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式为
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是
(5)表中的ⅠA族、ⅡA族元素全部是金属元素,这种判断
您最近一年使用:0次
2023-01-16更新
|
410次组卷
|
4卷引用:江西省宜春市万载县万载二中 2023?2024 学年高一上学期期末模拟考试化学试卷
江西省宜春市万载县万载二中 2023?2024 学年高一上学期期末模拟考试化学试卷山东省莘县多校2022-2023学年高一上学期期末线上联考化学试题(已下线)【知识图鉴】单元讲练测必修第一册第四单元03巩固练安徽省六安市金寨县青山中学2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
6 . 为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素。请按题目要求回答下列问题:
(1)①~⑦对应元素中,非金属性最强的元素名称是_______ ;⑤在周期表中的位置为_______ 。
(2)②与③形成化合物的电子式为_______ ;①的最高价氧化物的结构式为_______ 。
(3)③、④、⑥三种元素最高价氧化物对应的水化物的碱性由强到弱的顺序是_______ (用化学式来回答)。
(4)①~⑦对应元素中,位于金属与非金属的分界线附近的是_______ (填对应的序号)。
| ① | ② | |||||||
| ③ | ④ | ⑤ | ||||||
| ⑥ | …… | ⑦ | ||||||
(2)②与③形成化合物的电子式为
(3)③、④、⑥三种元素最高价氧化物对应的水化物的碱性由强到弱的顺序是
(4)①~⑦对应元素中,位于金属与非金属的分界线附近的是
您最近一年使用:0次
2022-09-08更新
|
114次组卷
|
2卷引用:江西省宜春市宜丰中学2023-2024学年高一下学期开学考试化学试题
名校
解题方法
7 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)据汞的原子结构示意图 ,汞在第
,汞在第_______ 周期。
(2)①叠氮化钠(NaN3)可用于汽车安全气囊的产气药,NaN3在撞击时能发生分解反应生成两种单质。计算理论上65 gNaN3完全分解,释放出标准状况下的气体体积_______ L。
②氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,工业将氧化铝、氮气和碳在一定条件下反应制得AlN和CO,请将下列的化学反应方程式配平。_______
_______Al2O3+_______N2+_______C—______AlN+_______CO
(3)利用元素的化合价推测物质的性质是化学研究的重要于段。如图是硫元素的“价—类”二维图:

①从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______ (填化学式)。
②Z的浓溶液与铁单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为_______ 。
(1)据汞的原子结构示意图
 ,汞在第
,汞在第(2)①叠氮化钠(NaN3)可用于汽车安全气囊的产气药,NaN3在撞击时能发生分解反应生成两种单质。计算理论上65 gNaN3完全分解,释放出标准状况下的气体体积
②氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,工业将氧化铝、氮气和碳在一定条件下反应制得AlN和CO,请将下列的化学反应方程式配平。
_______Al2O3+_______N2+_______C—______AlN+_______CO
(3)利用元素的化合价推测物质的性质是化学研究的重要于段。如图是硫元素的“价—类”二维图:

①从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
②Z的浓溶液与铁单质在加热条件下可以发生化学反应生成Y,该反应的化学方程式为
您最近一年使用:0次
2022-04-20更新
|
375次组卷
|
2卷引用:江西省新余市2021-2022学年高一下学期期末考试化学试题
8 . 下表为元素周期表的一 部分,请回答有关问题
(1)已知元素⑩ 的一种核素,中子数为45,用原子符号表示该核素为_________ ;
(2)元素⑦、⑧、⑨其离子半径由大到小的顺序是_________ (离子符号表示),元素⑨ 的最高价氧化物的水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为__________ 。
(3)下列事实不能说明元素⑧的非金属性比元素⑦的非金属性强的是_ ;
(4)由上表中的元素构成的A+、B+、 C-、D、E五种含有10个电子的粒子,已知他们有如下转化关系:反应一: A++C-  D+E↑:反应二 : B++C-=2D;写出B+的化学式
D+E↑:反应二 : B++C-=2D;写出B+的化学式__________ ,反应一的离子方程式为___________ 。
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ |
(2)元素⑦、⑧、⑨其离子半径由大到小的顺序是
(3)下列事实不能说明元素⑧的非金属性比元素⑦的非金属性强的是_ ;
| A.元素⑧的单质与⑦的氢化物的水溶液反应,溶液变浑浊 |
| B.元素⑧的单质能将Fe氧化成三价铁,而元素⑦的单质只能将铁氧化成二价铁 |
| C.⑦和⑧两元素的简单氢化物受热分解,后者的分解温度高 |
| D.元素⑧的氢化物的水溶液的酸性比元素⑦的氢化物水溶液的酸性强 |
 D+E↑:反应二 : B++C-=2D;写出B+的化学式
D+E↑:反应二 : B++C-=2D;写出B+的化学式
您最近一年使用:0次
名校
9 . 自门捷列夫发现元素周期表以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增加,回答下列问题:
(1)2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”。元素Mc可由反应: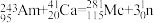 得到。该元素在周期表中的位置是
得到。该元素在周期表中的位置是_______ 。
(2) 氮和磷氢化物性质的比较
热稳定性:NH3_____ PH3(填“>”“<”)。
沸点:N2H4___ P2H4(填“>”“<”),判断依据是_______ 。
(3)铍、铝二者的单质、化合物均具有相似的化学性质,写出BeO与NaOH水溶液混合的化学方程式_______ 。
(1)2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”。元素Mc可由反应:
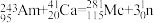 得到。该元素在周期表中的位置是
得到。该元素在周期表中的位置是(2) 氮和磷氢化物性质的比较
热稳定性:NH3
沸点:N2H4
(3)铍、铝二者的单质、化合物均具有相似的化学性质,写出BeO与NaOH水溶液混合的化学方程式
您最近一年使用:0次
名校
解题方法
10 . 下表为元素周期表的一部分,请参照元素①—⑩在表中的位置,用相应的化学用语 回答下列问题;
(1)表中⑩号元素有一种含20个中子的核素,请写出其原子符号_______ 。
(2)④、⑦、⑩的离子半径由大到小的顺序为_______ (用元素符号作答)。
(3)由表中④、⑥元素可以组成一种淡黄色的固体物质,画出该物质的电子式____ ,该物质含有的化学键类型有_____ 。
(4)元素⑩的一种含氧酸是常用的漂白性物质,这种含氧酸的结构式为____ ,元素⑤和⑩的氢化物中,酸性更强的是_____ 。
(5)上述10种元素中的两种能形成一种四核10电子分子,请用电子式表示其形成过程____ 。
| ① | |||||||
| ② | ③ | ④ | ⑤ | ||||
| ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中⑩号元素有一种含20个中子的核素,请写出其原子符号
(2)④、⑦、⑩的离子半径由大到小的顺序为
(3)由表中④、⑥元素可以组成一种淡黄色的固体物质,画出该物质的电子式
(4)元素⑩的一种含氧酸是常用的漂白性物质,这种含氧酸的结构式为
(5)上述10种元素中的两种能形成一种四核10电子分子,请用电子式表示其形成过程
您最近一年使用:0次
2021-05-24更新
|
190次组卷
|
4卷引用:江西省南昌市进贤县第一中学2020-2021学年高一下学期期末考试化学试题
江西省南昌市进贤县第一中学2020-2021学年高一下学期期末考试化学试题四川省遂宁市第二中学2020-2021学年高一下学期半期考试化学试题(已下线)专题03 化学键【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版必修2)河南省部分名校2020-2021学年高一下学期期末联考化学试题



