名校
解题方法
1 . 下表为元素周期表的一部分,请参照元素①—⑩在表中的位置,用相应的化学用语 回答下列问题;
(1)表中⑩号元素有一种含20个中子的核素,请写出其原子符号_______ 。
(2)④、⑦、⑩的离子半径由大到小的顺序为_______ (用元素符号作答)。
(3)由表中④、⑥元素可以组成一种淡黄色的固体物质,画出该物质的电子式____ ,该物质含有的化学键类型有_____ 。
(4)元素⑩的一种含氧酸是常用的漂白性物质,这种含氧酸的结构式为____ ,元素⑤和⑩的氢化物中,酸性更强的是_____ 。
(5)上述10种元素中的两种能形成一种四核10电子分子,请用电子式表示其形成过程____ 。
| ① | |||||||
| ② | ③ | ④ | ⑤ | ||||
| ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中⑩号元素有一种含20个中子的核素,请写出其原子符号
(2)④、⑦、⑩的离子半径由大到小的顺序为
(3)由表中④、⑥元素可以组成一种淡黄色的固体物质,画出该物质的电子式
(4)元素⑩的一种含氧酸是常用的漂白性物质,这种含氧酸的结构式为
(5)上述10种元素中的两种能形成一种四核10电子分子,请用电子式表示其形成过程
您最近一年使用:0次
2021-05-24更新
|
194次组卷
|
4卷引用:江西省南昌市进贤县第一中学2020-2021学年高一下学期期末考试化学试题
江西省南昌市进贤县第一中学2020-2021学年高一下学期期末考试化学试题四川省遂宁市第二中学2020-2021学年高一下学期半期考试化学试题(已下线)专题03 化学键【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版必修2)河南省部分名校2020-2021学年高一下学期期末联考化学试题
名校
2 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
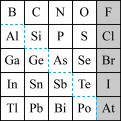
(1)元素Ga的原子结构示意图___________ ,镓(Ga)的氯化物与氨水反应的化学方程式为___________ ,
(2)Ge 的最高价氧化物对应水化物的化学式为___________ ,Bi的最高价氧化物为___________ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是___________ 元素(填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4___________ (填“>”“<”或“=”)H2SeO4。
③金属性比较:Tl___________ (填“>”“<”或“=”)Sn。
④氢化物的还原性:H2S___________ (填“>”“<”或“=”)H2O。
(4)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为___________ 。

(1)元素Ga的原子结构示意图
(2)Ge 的最高价氧化物对应水化物的化学式为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③金属性比较:Tl
④氢化物的还原性:H2S
(4)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为
您最近一年使用:0次
名校
3 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图元素周期表的回答下列问题。

(1)元素 Ga 在元素周期表中的位置为________ 。
(2) Sn 的最高正价为________ ;As 的气态氢化物为_____ ;CCl4的电子式________
(3)根据元素周期律推断:
①阴影部分元素氢化物热稳定性最高的是______ (填化学式)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4___ H2SeO4(填“>”、“<”或“=”)。
③简单氢化物的熔沸点:H2O__ H2S(填“>”“<”或“=”)。
(4)硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是____ 。
a.原子半径:In>Se
b.In 的金属性比 Se 强
c.In 的金属性比 Al 弱
d.硒化铟的化学式为 InSe2

(1)元素 Ga 在元素周期表中的位置为
(2) Sn 的最高正价为
(3)根据元素周期律推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③简单氢化物的熔沸点:H2O
(4)硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是
a.原子半径:In>Se
b.In 的金属性比 Se 强
c.In 的金属性比 Al 弱
d.硒化铟的化学式为 InSe2
您最近一年使用:0次
名校
4 . 下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题:
(1)自然界物质种类最多的元素在周期表中的位置是___ 。
(2)⑧⑨⑩的离子半径由大到小的顺序为___ (填离子符号)。
(3)写出由⑥⑧⑩元素形成的一种离子化合物的电子式:__ 。
(4)根据对角线元素性质相似规则,写出②的最高价氧化物对应的水化物与盐酸反应的离子方程式:___ 。
(5)已知W+X→Y+Z,W、X、Y、Z分别是由①⑤⑥三种元素中的两种形成的10电子粒子,写出该反应的离子方程式:__ 。
| IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
| 3 | ⑧ | ⑨ | ⑩ |
(1)自然界物质种类最多的元素在周期表中的位置是
(2)⑧⑨⑩的离子半径由大到小的顺序为
(3)写出由⑥⑧⑩元素形成的一种离子化合物的电子式:
(4)根据对角线元素性质相似规则,写出②的最高价氧化物对应的水化物与盐酸反应的离子方程式:
(5)已知W+X→Y+Z,W、X、Y、Z分别是由①⑤⑥三种元素中的两种形成的10电子粒子,写出该反应的离子方程式:
您最近一年使用:0次
5 . 自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增加。回答下列问题:
(1)2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”。元素Mc可由反应: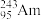 +
+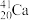 =
=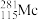 +3
+3 得到。该元素在周期表中的位置是
得到。该元素在周期表中的位置是___________ 。
(2)元素N的一种氢化物为N2H4,写出该化合物分子的电子式___________ ;该分子内存在的共价键类型有___________ 。
(3)铍、铝二者的单质、化合物均具有相似的化学性质,写出BeO溶液与NaOH的水溶液混合的化学方程式___________ 。
(1)2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”。元素Mc可由反应:
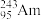 +
+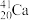 =
=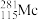 +3
+3 得到。该元素在周期表中的位置是
得到。该元素在周期表中的位置是(2)元素N的一种氢化物为N2H4,写出该化合物分子的电子式
(3)铍、铝二者的单质、化合物均具有相似的化学性质,写出BeO溶液与NaOH的水溶液混合的化学方程式
您最近一年使用:0次
名校
解题方法
6 . (1)现有下列10种物质:①O2;②H2;③NH4NO3;④Na2O2;⑤Ba(OH)2;⑥CH4;⑦CO2;⑧NaF;⑨NH3;⑩I2。
其中既含离子键又含非极性键的是___________ (填序号,下同);既含离子键又含极性键的是___________ ;属于电解质的是:___________ 。
(2)短周期的某元素的气态氢化物为H2R,则该元素的原子最外层有___________ 个电子。
(3)只含金属元素的主族位于第___________ 纵行。
(4)第四周期元素中,如第IIA族原子序数为a,则第IIIA族原子序数为___________ (用含a的式子表示)。
(5)周期表中位于第8纵行的铁元素属于第___________ 族,已知铁的原子序数为26,最外层有2个电子,则铁的原子结构示意图为___________ 。
(6)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子。若XY2为常见元素形成的离子化合物,则其电子式为___________ ;若XY2为共价化合物,则其结构式为___________ 。
其中既含离子键又含非极性键的是
(2)短周期的某元素的气态氢化物为H2R,则该元素的原子最外层有
(3)只含金属元素的主族位于第
(4)第四周期元素中,如第IIA族原子序数为a,则第IIIA族原子序数为
(5)周期表中位于第8纵行的铁元素属于第
(6)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子。若XY2为常见元素形成的离子化合物,则其电子式为
您最近一年使用:0次
2021-04-02更新
|
1002次组卷
|
2卷引用:江西省赣州市石城县石城中学2020-2021学年高一下学期3月月考化学试题
名校
7 . 2019 年是门捷列夫提出元素周期表 150 周年。下表为元素周期表的一部分,回答下列问题。
(1)元素①~⑨中,金属性最强的是______ (填元素符号)
(2)中国青年化学家姜雪峰被国际组织推选为“元素⑦代言人”,元素⑦的原子结构示意图是_________ 。
(3)④⑧⑨中形成的简单离子半径由大到小的顺序是______ (用离子符号表示)。
(4)写出由一个①原子和一个⑤原子及三个⑧原子构成的化合物分子的电子式________ 。
(5)元素③、⑤的最高价氧化物对应水化物中酸性较强的是______ (填化学式)。
(6)主族元素砷(As),原子序数为 33,广泛存在于自然界。
I、砷(As)在周期表中的位置是______ 。
II、下列说法正确的是________ (填序号)。
a.砷元素的最高化合价为+4
b.推测砷有多种氧化物
c.⑥的气态氢化物的还原性大于砷的气态氢化物的还原性
| IA | 0 | |||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | |||||||
(1)元素①~⑨中,金属性最强的是
(2)中国青年化学家姜雪峰被国际组织推选为“元素⑦代言人”,元素⑦的原子结构示意图是
(3)④⑧⑨中形成的简单离子半径由大到小的顺序是
(4)写出由一个①原子和一个⑤原子及三个⑧原子构成的化合物分子的电子式
(5)元素③、⑤的最高价氧化物对应水化物中酸性较强的是
(6)主族元素砷(As),原子序数为 33,广泛存在于自然界。
I、砷(As)在周期表中的位置是
II、下列说法正确的是
a.砷元素的最高化合价为+4
b.推测砷有多种氧化物
c.⑥的气态氢化物的还原性大于砷的气态氢化物的还原性
您最近一年使用:0次
名校
解题方法
8 . 下表为元素周期表的一部分,用请化学用语回答有关问题:
(1)C的元素符号是___________________ ;
(2)表中A与F的简单氢化物反应的化学方程式____________________________ ,E的单质与其下一周期同族元素的最高价氧化物在高温下反应的化学方程式_______________________________ ;
(3)表中所列元素中最高价氧化物对应水化物酸性最强的是__________________ (填写化学式)
(4)表中能形成的两性氢氧化物与A的最高价氧化物对应水化物反应的离子方程式____________________________________________________________ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
(1)C的元素符号是
(2)表中A与F的简单氢化物反应的化学方程式
(3)表中所列元素中最高价氧化物对应水化物酸性最强的是
(4)表中能形成的两性氢氧化物与A的最高价氧化物对应水化物反应的离子方程式
您最近一年使用:0次
名校
解题方法
9 . 下面是元素周期表的一部分,参照元素①~⑧在表中的位置。
请用化学用语回答下列问题:
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)___________________ 。
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)_____________ 。
(3)在①、④、⑤、⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:_____________________ 。
(4)由②最高价氧化物与⑤的同周期相邻主族元素的单质反应的化学方程式为:___________________________ 。
(5)②单质与③的最高价氧化物的水化物的浓溶液反应的离子方程式为______________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
请用化学用语回答下列问题:
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)
(3)在①、④、⑤、⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:
(4)由②最高价氧化物与⑤的同周期相邻主族元素的单质反应的化学方程式为:
(5)②单质与③的最高价氧化物的水化物的浓溶液反应的离子方程式为
您最近一年使用:0次
2020-08-28更新
|
94次组卷
|
2卷引用:江西省上高二中2020-2021学年高一下学期第五次月考化学试题
名校
解题方法
10 . 如图为元素周期表的一部分,请参照①-⑨在表中的位置,回答下列问题:(用元素符号或化学用语回答)
(1)由①②⑧三种元素形成的常见化合物的电子式为_____ ,其包含的化学键类型为_____ (填“离子键”、“共价键”)。
(2)⑦和⑨能以原子个数1:2形成化合物,用电子式表示其形成过程_____ 。
(3)金属性最强是_____ 。
(4)③的简单氢化物的沸点比⑦的简单氢化物的沸点_____ (填“高”或“低”),
(5)含氧酸酸性最强的是_____ 。(填分子式)
① | |||||||||||||||||
② | ③ | ||||||||||||||||
④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
⑨ |
(1)由①②⑧三种元素形成的常见化合物的电子式为
(2)⑦和⑨能以原子个数1:2形成化合物,用电子式表示其形成过程
(3)金属性最强是
(4)③的简单氢化物的沸点比⑦的简单氢化物的沸点
(5)含氧酸酸性最强的是
您最近一年使用:0次



