名校
1 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,下图是元素周期表的一部分,回答下列问题:
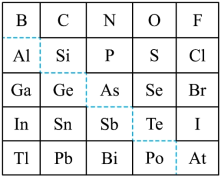
(1)元素Ga在元素周期表中的位置为:______ ;
(2)Sn的最高正价为______ ,C1的最高价氧化物对应水化物的化学式为______ ;
(3)根据元素周期律,推断
①表中元素形成的氢化物中热稳定性最高的是______ (写化学式),其电子式为______ 。
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4______ H2SeO4(填“>”、<”、“=”或“无法比较”);
③氢化物的还原性:H2O______ H2S(填“>”、“<”、“=”或“无法比较”)。
④原子半径比较:N______ Si(填“>”、“<”、“=”或“无法比较”)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断
①表中元素形成的氢化物中热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4
③氢化物的还原性:H2O
④原子半径比较:N
您最近一年使用:0次
名校
解题方法
2 . 下表列出了A~R9种元素在周期表中的位置。请回答下列问题。
(1)在这9种元素中,最外层电子数为1的元素为_____ (填元素符号),化学性质最不活泼的是_____ (填元素符号)。
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应水化物反应的离子方程式是_____ 。
(3)F、A、D三种元素的离子半径由大到小的顺序排列为_____ (填离子符号)。
(4)用电子式表示由C和H组成的化合物的形成过程:_____ 。
(5)由E和F形成的氧化物通入足量的B的氢氧化物中,其离子反应方程式为_____ 。
(6)由E和G所形成的化合物中所含有的化学键为_____ 。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应水化物反应的离子方程式是
(3)F、A、D三种元素的离子半径由大到小的顺序排列为
(4)用电子式表示由C和H组成的化合物的形成过程:
(5)由E和F形成的氧化物通入足量的B的氢氧化物中,其离子反应方程式为
(6)由E和G所形成的化合物中所含有的化学键为
您最近一年使用:0次
2023-12-24更新
|
432次组卷
|
2卷引用:甘肃省武威第七中学2023-2024学年高一上学期期末考试化学试题
名校
解题方法
3 . 下表是元素周期表的一部分,请参照元素①~⑦在表中的位置,请用化学用语回答下列问题:

(1)①~⑦元素中原子半径最大的是_______ 半径最小的是_______ (用元素符号表示);
(2)②、⑦两种元素所形成的气态氢化物中最稳定的是_______ (用化学式表示);
(3)③的单质着火时不能用水来灭火,原因之一是其燃烧的产物能与水反应,该反应的化学方程式为_______ ,该反应中产生标准状况下22.4 L的气体时,转移的电子的数目为_______ (用含 的代数式表示);
的代数式表示);
(4)写出③和④两种元素的最高价氧化物对应水化物反应的离子方程式_______ ;
(5)⑦元素单质的新制水溶液中能起杀菌消毒作用,光照易分解的弱酸是_______ 。(用化学式表示)

(1)①~⑦元素中原子半径最大的是
(2)②、⑦两种元素所形成的气态氢化物中最稳定的是
(3)③的单质着火时不能用水来灭火,原因之一是其燃烧的产物能与水反应,该反应的化学方程式为
 的代数式表示);
的代数式表示);(4)写出③和④两种元素的最高价氧化物对应水化物反应的离子方程式
(5)⑦元素单质的新制水溶液中能起杀菌消毒作用,光照易分解的弱酸是
您最近一年使用:0次
4 . 元素周期表的一部分如图,根据①~⑨在元素周期表中的位置,按题目要求回答下列问题:
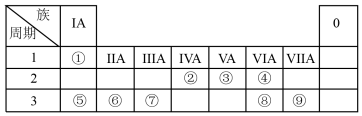
(1)在元素②~⑧中,非金属性最强的元素是_______ (填元素符号)。
(2)③~⑥四种元素的原子半径由大到小的顺序是_______ (填元素符号)。
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较强的是_______ (填化学式)。
(4)由元素①和元素④形成的原子个数比为1∶1的化合物中所含化学键的种类为_______ (填“离子键”、“极性共价键”或“非极性共价键”,有几种填几种);写出由元素⑤和元素④形成的原子个数比为1∶1的化合物的电子式:_______ 。
(5)写出元素⑦的单质与元素⑤的最高价氧化物对应的水化物之间反应的离子方程式:_______ 。
(6)元素⑤和元素⑧形成的常见化合物的化学式为_______ ,高温灼烧该化合物时,火焰呈_______ 色。

(1)在元素②~⑧中,非金属性最强的元素是
(2)③~⑥四种元素的原子半径由大到小的顺序是
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较强的是
(4)由元素①和元素④形成的原子个数比为1∶1的化合物中所含化学键的种类为
(5)写出元素⑦的单质与元素⑤的最高价氧化物对应的水化物之间反应的离子方程式:
(6)元素⑤和元素⑧形成的常见化合物的化学式为
您最近一年使用:0次
5 . 元素周期表的一部分,按要求完成各小题。
(1)化学性质最不活泼的元素____ ,(填元素符号,下同)非金属性最强的元素是____ ,金属性最强的单质与水反应的离子方程式为____ 。
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是____ 。
(3)①③⑤三种元素的原子半径由大到小的顺序为____ 。
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是____ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 二 | ⑥ | ⑦ | ⑪ | |||||
| 三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 四 | ② | ④ | ⑨ |
(1)化学性质最不活泼的元素
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是
(3)①③⑤三种元素的原子半径由大到小的顺序为
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是
您最近一年使用:0次
解题方法
6 . 在微观、宏观、符号之间建立联系是化学学科特有的特点。
图1是钾元素、硫元素在元素周期表中的信息,图2是一种微粒的结构示意图。
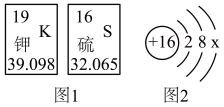
(1)钾元素的原子序数为_______ ,该元素属于_______ (填“金属元素”或“非金属元素”)
(2)硫元素的核内质子数为_______ ,其相对原子质量为_______ 。
a.若图2是硫原子的结构示意图,则x的值是_______ 。
b.若图2是硫离子的结构示意图,则x的值是_______ ,写出硫离子符号_______ 。
(3)写出由钾元素和硫元素组成的物质的化学式_______ 。
图1是钾元素、硫元素在元素周期表中的信息,图2是一种微粒的结构示意图。

(1)钾元素的原子序数为
(2)硫元素的核内质子数为
a.若图2是硫原子的结构示意图,则x的值是
b.若图2是硫离子的结构示意图,则x的值是
(3)写出由钾元素和硫元素组成的物质的化学式
您最近一年使用:0次
7 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
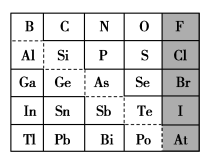
(1)Si的最高化合价为_______ ,Cl的最高价氧化物对应的水化物的化学式为_______ ,Bi的最高价氧化物的化学式为_______ 。
(2)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是_______ 元素(填元素符号)。
②酸性:
_______ (填“>”“<”或“=”,下同) 。
。
③氢化物的还原性:
_______  。
。
(3)N的氢化物和它的最高价含氧酸反应的化学方程式_______ 。

(1)Si的最高化合价为
(2)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是
②酸性:

 。
。③氢化物的还原性:

 。
。(3)N的氢化物和它的最高价含氧酸反应的化学方程式
您最近一年使用:0次
名校
解题方法
8 . 如表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题。
(1)地壳中含量最多的元素是____ 。
(2)氯元素位于元素周期表第____ 周期VIIA族。
(3)单质的化学性质最不活泼的是____ 。
(4)HF和HCl中,热稳定性较强的是____ 。
(5)元素最高价氧化物对应的水化物中,碱性最强的是____ (填化学式)。
(6)碳元素的最高价氧化物中碳元素与氧元素的质量比m(C):m(O)=____ 。
| 周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Al | Si | S | Cl | Ar |
(2)氯元素位于元素周期表第
(3)单质的化学性质最不活泼的是
(4)HF和HCl中,热稳定性较强的是
(5)元素最高价氧化物对应的水化物中,碱性最强的是
(6)碳元素的最高价氧化物中碳元素与氧元素的质量比m(C):m(O)=
您最近一年使用:0次
名校
9 . 1869年俄国科学家门捷列夫绘制出了第一张元素周期表,成为化学史上的里程碑之一,且大大地促进了化学学科的快速发展。下表是现代元素周期表的一部分,请据表回答下列问题:
(1)元素③的名称是___________ ,金属性最强的元素是___________ (填元素符号)。
(2)①②⑤三种元素原子半径由大到小的顺序为___________ (填序号)。
(3)元素⑦的单质的一种用途是___________ (填写“制造玻璃”或“制造计算机芯片”)。
(4)元素⑧⑨⑩最高价氧化物的水化物中酸性最强的是___________ (填化学式)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
二 | ① | ② | ③ | ||||
三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)元素③的名称是
(2)①②⑤三种元素原子半径由大到小的顺序为
(3)元素⑦的单质的一种用途是
(4)元素⑧⑨⑩最高价氧化物的水化物中酸性最强的是
您最近一年使用:0次
2022-03-16更新
|
637次组卷
|
3卷引用:甘肃省临夏县中学2022-2023学年高二下学期期中考试化学试题
10 . 元素周期表与元素周期律在化学学习研究中有很重要的作用。如表是元素周期表的一部分,回答下列问题(用相关化学用语回答)。
(1)⑤、⑥、⑨、⑩的简单离子半径由小到大的顺序____ ,写出⑥的原子结构示意图:____ 。
(2)元素①的一种同素异形体为天然存在的最硬的物质,它属于____ (填“晶体”或“非晶体”)。
(3)元素②、③、④的简单气态氢化物的稳定性最强的是____ (用化学式表示,下同),元素③、⑨简单氢化物沸点较高的是____ 。
(4)元素⑤、⑥最高价氧化物对应的水化物碱性更强的是____ ,元素⑪最高价氧化物对应的水化物的化学式是____ 。
(5)请用电子式表示元素⑤的氧化物的形成过程:____ ,该化合物属于____ (填“共价”或“离子”)化合物。
(6)⑤2⑨③3在加热条件下发生分解反应生成两种盐,其中一种产物为无氧酸盐,该反应的化学方程式:____ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 四 | ⑪ |
(2)元素①的一种同素异形体为天然存在的最硬的物质,它属于
(3)元素②、③、④的简单气态氢化物的稳定性最强的是
(4)元素⑤、⑥最高价氧化物对应的水化物碱性更强的是
(5)请用电子式表示元素⑤的氧化物的形成过程:
(6)⑤2⑨③3在加热条件下发生分解反应生成两种盐,其中一种产物为无氧酸盐,该反应的化学方程式:
您最近一年使用:0次
2022-03-07更新
|
668次组卷
|
3卷引用:甘肃省酒泉市2022-2023学年高一上学期1月期末考试化学试题
甘肃省酒泉市2022-2023学年高一上学期1月期末考试化学试题河北省保定市2021-2022学年高一上学期期末考试化学试题(已下线)专题08 元素周期表与元素周期律-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)



