1 . Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是___________ (填序号)。
a. b.
b. c.
c. d.
d.
(3)Ti原子最高能层电子的电子云轮廓形状为___________ ,Ti原子位于元素周期表中的___________ 区,与Ti同周期的过渡元素中,未成对电子数最多的的基态原子的外围电子的轨道表示式___________ 。
(4)N元素基态原子核外电子有___________ 种不同的空间运动状态,能量最高的电子所在原子轨道在空间有___________ 个伸展方向。
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.
 b.
b. c.
c. d.
d.
(3)Ti原子最高能层电子的电子云轮廓形状为
(4)N元素基态原子核外电子有
您最近一年使用:0次
2 . 人体必需的一些元素在周期表中的分布情况如下:

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是___________ 。H2O2是一种绿色氧化剂,电子式为___________ 。
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为___________ 。
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是___________ ,原子序数为___________ 。
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为___________ 。
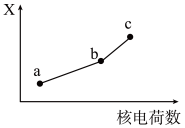
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________(填字母)。

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________(填字母)。

| A.若a、b、c表示氧族元素,则X表示对应氢化物的稳定性 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第IA族元素,则X表示对应离子的氧化性 |
| D.若a、b、c表示第IIA族元素,则X表示最高价氧化物对应水化物的碱性 |
您最近一年使用:0次
2023-12-05更新
|
259次组卷
|
3卷引用:湖北省宜城市第一中学等六校2023-2024学年高二上学期期中考试化学试题
解题方法
3 . 根据①~⑧元素的编号所在周期表中的位置,用相应的元素符号 或者化学用语 回答有关问题:
(1)能显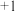 价,还能显
价,还能显 价的元素是
价的元素是_________ 。
(2)最高价氧化物对应水化物是强酸的元素是_________ 。
(3)最难形成化合物的元素是_________ 。
(4)①和④可形成原子数目比为1∶1的化合物,其电子式为_________ 。
(5)③、④、⑤分别与①形成的10电子分子的沸点由低到高的顺序为_________ 。
(6)⑥和⑦最高价氧化物对应水化物相互反应的离子方程式是________ 。
(7)第三周期某元素氢化物(组成为RH)能和冷水剧烈反应产生氢气,该反应的化学方程式为_____ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | ② | ||||||
2 | ③ | ④ | ⑤ | |||||
3 | ⑥ | ⑦ | ⑧ |
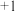 价,还能显
价,还能显 价的元素是
价的元素是(2)最高价氧化物对应水化物是强酸的元素是
(3)最难形成化合物的元素是
(4)①和④可形成原子数目比为1∶1的化合物,其电子式为
(5)③、④、⑤分别与①形成的10电子分子的沸点由低到高的顺序为
(6)⑥和⑦最高价氧化物对应水化物相互反应的离子方程式是
(7)第三周期某元素氢化物(组成为RH)能和冷水剧烈反应产生氢气,该反应的化学方程式为
您最近一年使用:0次
4 . 元素周期表反应了元素存在周期性的变化规律,下表是周期表中部分元素的部分信息:
分析并回答下列问题:
(1)周期表从左到右依次有18个纵行,上述元素在周期表的第______ 个纵行。
(2)上表中xBr、zAt的x=______ ,z=______ 。
(3)yI在周期表中的位置是_______________________ 。
(4)常温下,描述最接近砹单质物理性质的是 。
(5)单质从F2到I2分别与氢气反应的条件依次是 。
(6)下列化学式正确的是 。
(7)IBr是一种拟卤素,它的性质与卤素单质的化学性质相似。请写出Cl2和IBr分别与NaOH溶液反应的化学方程式①____ 、②____ 。其中属于氧化还原反应有____ 。
| 元素名称 | 氟 | 氯 | 溴 | 碘 | 砹 |
| 元素符号 | 9F | 17Cl | xBr | yI | zAt |
| 单质颜色(常态) | 浅黄绿色 | 黄绿色 | 深红棕色 | 紫黑色 | / |
| 单质熔点/℃ | -219.6 | -101 | -7.2 | 113.5 | / |
| 单质沸点/℃ | -188.1 | -34.6 | 58.78 | 184.4 | / |
| 主要化合价 | -1 | -1、+7 | -1、+7 | -1、+7 | / |
分析并回答下列问题:
(1)周期表从左到右依次有18个纵行,上述元素在周期表的第
(2)上表中xBr、zAt的x=
(3)yI在周期表中的位置是
(4)常温下,描述最接近砹单质物理性质的是 。
| A.红色液体易挥发 | B.无色气体易液化 |
| C.灰色固体易升华 | D.黑色固体易升华 |
| A.点燃、接触、加热、强热 | B.强热、接触、加热、点燃 |
| C.接触、点燃、加热、强热 | D.加热、接触、强热、加热 |
| A.Na2At | B.CAt4 | C.AgAt2 | D.At2O7 |
您最近一年使用:0次
5 . 根据以下9种元素在元素周期表中的位置,回答下列问题:
(1)①的原子轨道形状是_______ ;②③④的第一电离能由大到小的顺序是_______ (填编号)。
(2)下列可以判断⑤和⑥金属性强弱的是_______ (填序号)。
a.单质的熔点:⑤<⑥ b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥ d.最高价氧化物对应水化物的碱性:⑤>⑥
(3)③与⑦形成的化合物是一种性能优异的无机非金属材料,据元素周期律知识,写出其化学式_______ ,它的熔点高,硬度大,电绝缘性好,化学性质稳定。它的晶体类型是_______ ,试推测其可能有哪些用途_______ (填序号)。
a.制作坩埚 b.制作切削刀具 c.制作耐高温轴承
(4)⑧与⑨可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子稳定结构,试写出其结构式_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)下列可以判断⑤和⑥金属性强弱的是
a.单质的熔点:⑤<⑥ b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥ d.最高价氧化物对应水化物的碱性:⑤>⑥
(3)③与⑦形成的化合物是一种性能优异的无机非金属材料,据元素周期律知识,写出其化学式
a.制作坩埚 b.制作切削刀具 c.制作耐高温轴承
(4)⑧与⑨可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子稳定结构,试写出其结构式
您最近一年使用:0次
解题方法
6 . 回答下列问题:
(1)请按顺序补写出1-18号元素符号: H He Li Be B___N___F Ne Na___Si P___Ar___
(2)请正确标出下划线元素的化合价: H2O2___ ,NH3___ ,Fe2O3___ ,H2SO4___ ,HNO3___ ,KClO3___
(1)请按顺序补写出1-18号元素符号: H He Li Be B___N___F Ne Na___Si P___Ar
(2)请正确标出下划线元素的化合价: H2O2
您最近一年使用:0次
2022-09-16更新
|
80次组卷
|
2卷引用:湖北省宜城市第三中学2021-2022学年高一上学期期中化学试题
7 . 下面为元素周期表的一部分,根据元素①~⑧在表中的位置回答下列问题。
(1)①的元素名称为:___________ ,元素④的原子结构示意图为___________ 。
(2)②的最高价氧化物对应水化物酸性比③的最高价氧化物对应水化物酸性弱的原因是___________(填字母)。
(3)②、④组成的能引起温室效应的化合物的电子式为___________ ,其中含有的化学键为___________ 。
(4)②、⑧的最高价氧化物对应水化物的酸性从强到弱的顺序为___________ (用化学式表示)。
(5)③、⑤、⑦三种元素的离子半径从大到小顺序为___________ (用元素符号表示)。
(6)写出元素⑤⑥对应的最高价氧化物的水化物相互之间发生反应的化学方程式___________ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②的最高价氧化物对应水化物酸性比③的最高价氧化物对应水化物酸性弱的原因是___________(填字母)。
| A.②的单质为固体,而③的单质为气体 |
| B.原子半径②比③大 |
| C.②的非金属性比③弱 |
| D.原子序数③比②大 |
(4)②、⑧的最高价氧化物对应水化物的酸性从强到弱的顺序为
(5)③、⑤、⑦三种元素的离子半径从大到小顺序为
(6)写出元素⑤⑥对应的最高价氧化物的水化物相互之间发生反应的化学方程式
您最近一年使用:0次
2022-02-26更新
|
324次组卷
|
2卷引用:湖北省竹山县第二中学2021-2022学年高一下学期6月月考化学试题
名校
8 . 下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:
(1)金属性最强的是___________ (填元素名称)。
(2)⑨的离子结构示意图为___________ 。
(3)⑤元素和⑩元素的最简单氢化物的稳定性由强到弱的关系是___________ (填化学式)。
(4)④、⑤、⑥的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(5)⑧、⑨、⑩最高价氧化物对应的水化物酸性由弱到强的顺序是___________ (填化学式)
(6)用电子式表示④与⑥形成的原子个数比为1 ∶2的化合物的形成过程___________ 。
(7)⑧单质与⑥的最高价氧化物水化物的溶液发生反应,写出生成的阴离子为___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)⑨的离子结构示意图为
(3)⑤元素和⑩元素的最简单氢化物的稳定性由强到弱的关系是
(4)④、⑤、⑥的简单离子半径由大到小的顺序为
(5)⑧、⑨、⑩最高价氧化物对应的水化物酸性由弱到强的顺序是
(6)用电子式表示④与⑥形成的原子个数比为1 ∶2的化合物的形成过程
(7)⑧单质与⑥的最高价氧化物水化物的溶液发生反应,写出生成的阴离子为
您最近一年使用:0次
2022-01-22更新
|
526次组卷
|
3卷引用:湖北省麻城市实验高级中学2021-2022学年高一下学期2月迎春考化学试题
9 . 下表是元素周期表的一部分。表中所列字母分别代表一种元素。
回答下列问题:
(1)j在元素周期表中的位置是______ 。
(2)e、h、m形成的简单离子其半径由大到小的顺序为________ 。(填写离子符号)
(3)n与g形成的化合物为______ (填写化学式,下同),将该化合物进行焰色反应,火焰呈______ 色。
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为______ 。
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为______ 。
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg_____ Al(选填“>”或“<”);
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释______ 。
| a | b | |||||||
| c | d | e | f | |||||
| g | h | i | j | k | l | m | ||
| n |
(1)j在元素周期表中的位置是
(2)e、h、m形成的简单离子其半径由大到小的顺序为
(3)n与g形成的化合物为
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释
您最近一年使用:0次
2022-01-14更新
|
783次组卷
|
4卷引用:湖北省孝感市新高考联考协作体2022-2023学年高二上学期9月联考化学试题
湖北省孝感市新高考联考协作体2022-2023学年高二上学期9月联考化学试题湖南省怀化市2021-2022学年高一上学期期末考试化学试题(已下线)第四章 物质结构 元素周期律(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)(已下线)【2023】【高一下】【其他】【杭高卷四-期中复习卷】【高中化学】【刘尼尼收集】
名校
10 . 下表是元素周期表的一部分,针对表中的①~⑦种元素,填写下列空白(涉及表中元素一律用对应化学符号表示):

(1)在这些元素中,化学性质最不活泼的是___________ (填元素符号),原子结构示意图为___________ 。
(2)元素⑦在周期表中的位置是___________ 。
(3)在元素①③⑥中,与氧气加热条件下反应最不剧烈的单质是___________ (填元素符号),化学方程式为___________ 。
(4)碘位于元素周期表中元素⑦的正下方,其原子序数为___________ ,碘的一种核素含有78个中子,常用于甲状腺功能检查和甲状腺疾病治疗,该核素符号为___________ 。
(5)元素②形成的氧化物中,能造成温室效应的是___________ (填化学式);2mol该氧化物与3mol元素③的最高价氧化物对应的水化物充分反应,所得溶液常温下的pH___________ 7。(用“>”、“<”或“=”作答)

(1)在这些元素中,化学性质最不活泼的是
(2)元素⑦在周期表中的位置是
(3)在元素①③⑥中,与氧气加热条件下反应最不剧烈的单质是
(4)碘位于元素周期表中元素⑦的正下方,其原子序数为
(5)元素②形成的氧化物中,能造成温室效应的是
您最近一年使用:0次



