解题方法
1 . 回答下列问题。
(1)氮元素在元素周期表中的位置是第___________ 周期,第___________ 族。
(2) 是元素周期表中第
是元素周期表中第___________ 号元素。
(3) 的M能层电子排布式是
的M能层电子排布式是___________ ,价层电子排布图是___________ ,原子结构示意图是___________ 。
(1)氮元素在元素周期表中的位置是第
(2)
 是元素周期表中第
是元素周期表中第(3)
 的M能层电子排布式是
的M能层电子排布式是
您最近一年使用:0次
名校
2 . 下图是某牙膏成分表的一部分,回答下列问题:
(1)牙膏属于___________ (填“混合物”或“纯净物”)。
(2)含氟牙膏能预防龋齿,这里的“氟”指的是___________ (填“分子”“原子”或“元素”)。
(3)二氧化硅(SiO2)中硅元素的化合价为___________ 。
(4)人被有些蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,使人产生痛痒感。在叮咬处涂抹牙膏就可减轻痛痒,说明该牙膏呈___________ (填“酸性”“碱性”或“中性”)。
| XX牙膏 成分:二氧化硅、水、 纤维素胶、碳酸钠、 香精、单氟磷酸钠、 碳酸氢钠… |
(2)含氟牙膏能预防龋齿,这里的“氟”指的是
(3)二氧化硅(SiO2)中硅元素的化合价为
(4)人被有些蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,使人产生痛痒感。在叮咬处涂抹牙膏就可减轻痛痒,说明该牙膏呈
您最近一年使用:0次
3 . 元素周期表中锑元素的数据如图。

(1)根据锑的价层电子排布式5s25p3可知,锑在元素周期表中位于第___________ 周期,第___________ 族。
(2)基态锑原子中有___________ 个未成对电子,这些未成对电子具有___________ (填“相同”或“不同”)的自旋状态。
(3)基态锑原子的5s轨道形状为___________ 形,该原子最外层电子占有___________ 个轨道。
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。则两种元素的电负性Sb___________ Bi;原子半径Sb___________ Bi (填“>”或“<”)。

(1)根据锑的价层电子排布式5s25p3可知,锑在元素周期表中位于第
(2)基态锑原子中有
(3)基态锑原子的5s轨道形状为
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。则两种元素的电负性Sb
您最近一年使用:0次
名校
4 . 已知 的3d轨道上有6个电子,试回答:
的3d轨道上有6个电子,试回答:
(1)M元素原子的核外电子排布式为_______ 。
(2)M元素在元素周期表中的位置为_______ 。
(3)M的基态原子共有_______ 种不同能级的电子,该原子最外层电子数为_______ ,价层电子数为_______ 。
(4)某元素原子的基态电子排布式为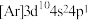 ,该元素处于元素周期表的第
,该元素处于元素周期表的第_______ 周期第_______ 族。试推测该元素处于元素周期表的_______ 区,该元素原子的价电子排布图为_______ 。
(5)与M元素相对比,铬(Cr)元素的原子核外电子排布有其特点,请写出Cr基态原子核外电子排布式_______ 。
 的3d轨道上有6个电子,试回答:
的3d轨道上有6个电子,试回答:(1)M元素原子的核外电子排布式为
(2)M元素在元素周期表中的位置为
(3)M的基态原子共有
(4)某元素原子的基态电子排布式为
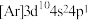 ,该元素处于元素周期表的第
,该元素处于元素周期表的第(5)与M元素相对比,铬(Cr)元素的原子核外电子排布有其特点,请写出Cr基态原子核外电子排布式
您最近一年使用:0次
解题方法
5 . 按要求完成下列填空
(1)写出KOH电子式_______ ;写出CO2的结构式_______
(2)短周期主族元素中周期序数和族序数相等的元素有_______ (填元素符号)
(3)用电子式表示下列化合物的形成过程H2S:_______ ;MgF2:_______ 。
(4)A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为_______ 。
(1)写出KOH电子式
(2)短周期主族元素中周期序数和族序数相等的元素有
(3)用电子式表示下列化合物的形成过程H2S:
(4)A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为
您最近一年使用:0次
名校
6 . 下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:
(1)金属性最强的是___________ (填元素名称)。
(2)⑨的离子结构示意图为___________ 。
(3)⑤元素和⑩元素的最简单氢化物的稳定性由强到弱的关系是___________ (填化学式)。
(4)④、⑤、⑥的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(5)⑧、⑨、⑩最高价氧化物对应的水化物酸性由弱到强的顺序是___________ (填化学式)
(6)用电子式表示④与⑥形成的原子个数比为1 ∶2的化合物的形成过程___________ 。
(7)⑧单质与⑥的最高价氧化物水化物的溶液发生反应,写出生成的阴离子为___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)⑨的离子结构示意图为
(3)⑤元素和⑩元素的最简单氢化物的稳定性由强到弱的关系是
(4)④、⑤、⑥的简单离子半径由大到小的顺序为
(5)⑧、⑨、⑩最高价氧化物对应的水化物酸性由弱到强的顺序是
(6)用电子式表示④与⑥形成的原子个数比为1 ∶2的化合物的形成过程
(7)⑧单质与⑥的最高价氧化物水化物的溶液发生反应,写出生成的阴离子为
您最近一年使用:0次
2022-01-22更新
|
526次组卷
|
3卷引用:宁夏青铜峡市宁朔中学、吴忠中学青铜峡分校2021-2022学年高一下学期期中考试化学试题
名校
7 . 锶元素的粒子结构示意图和在元素周期表中显示的信息如图所示:
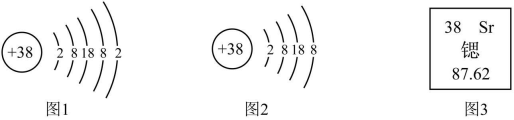
(1)锶属于___________ 元素(填“金属”或“非金属”)。
(2)锶元素的原子序数为___________ ,相对原子质量为___________ 。
(3)图2所表示的粒子的化学符号是___________ 。
(4)它与地壳中含量第一位的元素组成物质的化学式是___________ 。

(1)锶属于
(2)锶元素的原子序数为
(3)图2所表示的粒子的化学符号是
(4)它与地壳中含量第一位的元素组成物质的化学式是
您最近一年使用:0次
名校
解题方法
8 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)元素②的原子结构示意图是___________ ,形成化合物种类最多的元素是___________ 。(填元素符号)
(2)元素⑨在周期表中所处位置___________ ,从元素原子得失电子的角度看,元素⑨具有___________ (填“氧化性”或“还原性”)。
(3)元素③与元素⑤形成原子个数比为1:1的化合物的电子式为___________ ,该化合物中存在的化学键类型有___________ 、___________ 。
(4)第三周期元素除⑩外原子半径最大的是___________ (填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是___________ (填化学式,下同),具有两性的是___________ ,这两种物质反应的离子方程式为___________ 。
(5)元素④、⑤、⑥形成简单离子的半径由大到小的顺序是___________ 。(填离子符号)
 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素⑨在周期表中所处位置
(3)元素③与元素⑤形成原子个数比为1:1的化合物的电子式为
(4)第三周期元素除⑩外原子半径最大的是
(5)元素④、⑤、⑥形成简单离子的半径由大到小的顺序是
您最近一年使用:0次
名校
解题方法
9 . 据报道,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将给量子计算机的研究带来重大突破。已知铷是37号元素。根据相关知识回答下列问题:
(1)铷(Rb)位于元素周期表的第___ 周期___ 族。
(2)关于铷的结构和性质判断正确的是___ (填序号)。
①与水反应比钠剧烈
②原子半径比钠的小
③氧化物暴露在空气中易吸收CO2
④阳离子最外层电子数和镁离子最外层电子数相同
⑤是还原剂
(3)现有铷和另一种碱金属形成的合金50g,当它与足量水反应时,放出标准状况下的氢气22.4L,这种碱金属可能是___ (填字母)。
A.Li B.Na C.K D.Cs
(1)铷(Rb)位于元素周期表的第
(2)关于铷的结构和性质判断正确的是
①与水反应比钠剧烈
②原子半径比钠的小
③氧化物暴露在空气中易吸收CO2
④阳离子最外层电子数和镁离子最外层电子数相同
⑤是还原剂
(3)现有铷和另一种碱金属形成的合金50g,当它与足量水反应时,放出标准状况下的氢气22.4L,这种碱金属可能是
A.Li B.Na C.K D.Cs
您最近一年使用:0次
名校
解题方法
10 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:

(1)元素⑦的名称为______ ,在周期表中的位置______________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_______ ,碱性最强的化合物的电子式是__________ 。
(3)用电子式表示元素④和⑥的化合物的形成过程:____________ ,该化合物属于______ (填“共价”或“离子”)化合物。
(4)写出一种由上述元素组成的既有离子键又有共价键的物质的化学式______ 。
(5)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是_________ (用离子符号表示)

(1)元素⑦的名称为
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素④和⑥的化合物的形成过程:
(4)写出一种由上述元素组成的既有离子键又有共价键的物质的化学式
(5)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是
您最近一年使用:0次
2020-07-13更新
|
320次组卷
|
2卷引用:宁夏银川市宁夏大学附属中学2019-2020学年高一下学期期中考试化学试题



