1 . 元素在周期表中的位置反映了元素的原子结构和元素的性质。针对下表中的①~⑩种元素,回答以下问题:

(1)第三周期金属元素中原子半径最小的元素为________ (写序号);表中的X元素在第________ 周期第________ 族。
(2)④、⑤分别与①元素组成含10个电子的分子化学式分别为________ 、________ ;
(3)通过单质之间的置换反应,可以比较卤素单质的氧化性强弱。请用离子方程式表示⑧和⑨元素单质的氧化性强弱:________________ ;
(4)用电子式表示②与⑦形成化合物的过程:________________ ;
(5)由①②⑤元素组成的化合物的化学键类型为________ 、________ ;
(6)写出能证明②的金属性强于③的化学事实________ (任写一条)。

(1)第三周期金属元素中原子半径最小的元素为
(2)④、⑤分别与①元素组成含10个电子的分子化学式分别为
(3)通过单质之间的置换反应,可以比较卤素单质的氧化性强弱。请用离子方程式表示⑧和⑨元素单质的氧化性强弱:
(4)用电子式表示②与⑦形成化合物的过程:
(5)由①②⑤元素组成的化合物的化学键类型为
(6)写出能证明②的金属性强于③的化学事实
您最近一年使用:0次
名校
解题方法
2 . 155年前门捷列夫制得世界上第一张元素周期表,它反映了元素之间的内在联系,是对元素的一种很好的自然分类。如图为现代元素周期表的一部分,请回答下列问题:(以下问题均用相应的化学用语表达 )

(1)在这10种元素中,非金属性最强的元素在周期表中的位置是___________ 。
(2)由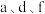 三种元素形成的化合物含有的化学键有
三种元素形成的化合物含有的化学键有___________ (填写化学键类型),属于___________ 化合物。
(3)元素b、c形成的简单气态氢化物中较稳定的是___________ (写具体的化学式,下同);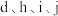 的简单离子半径由大到小的顺序排列为
的简单离子半径由大到小的顺序排列为___________ 。
(4)用电子式表示元素g与e的化合物形成的过程___________ 。
(5)在含有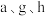 简单阳离子的
简单阳离子的 溶液中,逐滴滴加
溶液中,逐滴滴加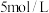 的
的 溶液到过量,生成沉淀的质量与加入的
溶液到过量,生成沉淀的质量与加入的 溶液的体积关系如图所示。由图中数据分析计算
溶液的体积关系如图所示。由图中数据分析计算
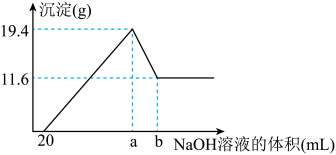
①沉淀减少时发生的离子方程式:___________ 。
②a点的数值为:___________ mL。

(1)在这10种元素中,非金属性最强的元素在周期表中的位置是
(2)由
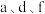 三种元素形成的化合物含有的化学键有
三种元素形成的化合物含有的化学键有(3)元素b、c形成的简单气态氢化物中较稳定的是
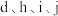 的简单离子半径由大到小的顺序排列为
的简单离子半径由大到小的顺序排列为(4)用电子式表示元素g与e的化合物形成的过程
(5)在含有
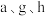 简单阳离子的
简单阳离子的 溶液中,逐滴滴加
溶液中,逐滴滴加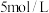 的
的 溶液到过量,生成沉淀的质量与加入的
溶液到过量,生成沉淀的质量与加入的 溶液的体积关系如图所示。由图中数据分析计算
溶液的体积关系如图所示。由图中数据分析计算
①沉淀减少时发生的离子方程式:
②a点的数值为:
您最近一年使用:0次
解题方法
3 . 下表列出了A~R9种元素在周期表中的位置:
请回答下列问题。
(1)这些元素分别为:A___________ ,B___________ ,C___________ ,D___________ ,E___________ ,F___________ ,G___________ ,R___________ ,其中化学性质最不活泼的是___________ (用元素符号表示)。
(2)画出G的原子结构示意图___________ 。
(3)元素周期表共有___________ 个周期___________ 个族,18纵行元素化合价通常表现为___________ 价所以称为0族元素,又叫惰性气体元素。A位于___________ 周期___________ 族
(4)H元素与A元素形成的化合物高温灼烧时,火焰呈___________ 色。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
(1)这些元素分别为:A
(2)画出G的原子结构示意图
(3)元素周期表共有
(4)H元素与A元素形成的化合物高温灼烧时,火焰呈
您最近一年使用:0次
2024-01-05更新
|
150次组卷
|
2卷引用:广西钦州市第四中学2023-2024学年高一上学期12月考试化学试卷
名校
解题方法
4 . 金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)基态Na原子的原子结构示意图表示式为___________ ,在周期表中的位置是___________ 。
(2)Na2O2的电子式为___________ 。Na2O2可作供氧剂,写出Na2O2与CO2反应的化学方程式___________ 。若有1molNa2O2参加反应则转移电子的物质的量为___________ mol。
(3)采用空气和Na为原料可直接制备Na2O2。空气与熔融金属Na反应前需依次通过___________ 、___________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应: ___________MnO +___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式
+___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式_________ ;该反应说明Na2O2具有___________ 性(选填“氧化”,“还原”或“漂白”)。
(5)天然碱的主要成分为Na2CO3·NaHCO3·2H2O,1molNa2CO3·NaHCO3·2H2O经充分加热得到Na2CO3的质量为___________ g。
(1)基态Na原子的原子结构示意图表示式为
(2)Na2O2的电子式为
(3)采用空气和Na为原料可直接制备Na2O2。空气与熔融金属Na反应前需依次通过
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应: ___________MnO
 +___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式
+___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式(5)天然碱的主要成分为Na2CO3·NaHCO3·2H2O,1molNa2CO3·NaHCO3·2H2O经充分加热得到Na2CO3的质量为
您最近一年使用:0次
2023-12-02更新
|
196次组卷
|
2卷引用:广西钦州市第四中学2023-2024学年高一上学期12月考试化学试卷
名校
解题方法
5 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
(1)②的最高价氧化物的分子式为_______ ;⑦的最高价氧化物对应水化物的分子式为_______ 。
(2)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:_______ 。
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_______(填字母)。
(4)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为_______ 。
②铯单质与 反应的化学反应方程式为
反应的化学反应方程式为_______ 。
③预测铯单质的还原性比钠单质的还原性_______ (填“弱”或“强”)。
④下列推断正确的是_______ (填字母)。
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为_______ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_______(填字母)。
| A.在化合物中最高正化合价为+6 | B.单质可以与 气体反应并置换出单质S 气体反应并置换出单质S |
| C.最高价氧化物对应水化物的酸性比硫酸弱 | D.单质在常温下可与氢气化合 |
①铯的原子序数为
②铯单质与
 反应的化学反应方程式为
反应的化学反应方程式为③预测铯单质的还原性比钠单质的还原性
④下列推断正确的是
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
2023-11-10更新
|
882次组卷
|
2卷引用:广西柳州铁一中学2022-2023学年高一上学期期末考试化学试题
6 . 下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:
(1)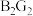 的电子式为
的电子式为___________ 。
(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是___________ (填化学式)。
(3)B、C、E、H四种元素对应的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序为___________ (填化学式)。
(5)请写出B、E的最高价氧化物对应的水化物发生反应的化学方程式:___________ 。
| A | |||||||||||||||||
| G | I | ||||||||||||||||
| B | E | F | H | ||||||||||||||
| C | D | J |
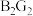 的电子式为
的电子式为(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是
(3)B、C、E、H四种元素对应的简单离子半径由大到小的顺序是
(4)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序为
(5)请写出B、E的最高价氧化物对应的水化物发生反应的化学方程式:
您最近一年使用:0次
7 . 完成下列问题:
(1)N、O、Mg、Al、S、Fe是常见的六种元素,按要求回答下列问题:
①Fe位于元素周期表第_____ 周期第_____ 族。
②基态N原子核外电子排布式为_____ ;基态O原子核外有_____ 种运动状态的电子。
③基态S原子核外电子占据的最高能级的电子云轮廓图为_____ 形。
④Mg、Al两种元素中第一电离能较大的是_____ 填元素符号)。
(2)几种元素的电负性数据如表:
①AlBr3的熔点_____ AlF3的熔点(填“大于”、“小于”或“等于”),原因是_____ 。
②根据同一主族元素电负性递变规律,预测碘元素的电负性数值范围为_____ 。
(1)N、O、Mg、Al、S、Fe是常见的六种元素,按要求回答下列问题:
①Fe位于元素周期表第
②基态N原子核外电子排布式为
③基态S原子核外电子占据的最高能级的电子云轮廓图为
④Mg、Al两种元素中第一电离能较大的是
(2)几种元素的电负性数据如表:
| O | F | Al | Br | …… |
| 3.5 | 4.0 | 1.5 | 2.8 | …… |
②根据同一主族元素电负性递变规律,预测碘元素的电负性数值范围为
您最近一年使用:0次
8 . 如表是元素周期表的一部分。回答下列问题:
(1)地球上99%的溴元素存在于海水中,因此溴被称为“海洋元素”。
①该表中溴在元素周期表中的位置为____________ 。
②该表中最高价氧化物对应的水化物酸性最强的是______ (填化学式),该元素形成化合物HXO的结构式为______ (X用对应元素符号表示)。
③卤素互化物(如IBr)与卤素单质性质相似。已知IBr能与水发生非氧化还原反应,写出IBr与水反应的化学方程式____________ ,IBr中含有的化学键是______ (填“离子键”、“极性键”或“非极性键”)。
(2) 溶于水形成
溶于水形成 溶液,向所得溶液中通入
溶液,向所得溶液中通入 气体,反应生成Se和
气体,反应生成Se和 。写出
。写出 与
与 反应的化学方程式
反应的化学方程式____________ 。
(3)已知某主族元素离子结构示意图为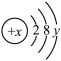 ,其中
,其中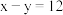 ,此元素与氯元素组成化合物的电子式为
,此元素与氯元素组成化合物的电子式为______ 。
16 S 硫 32.06 | 17 Cl 氯 35.45 |
34 Se 硒 78.96 | 35 Br 溴 79.90 |
53 I 碘 126.9 |
(1)地球上99%的溴元素存在于海水中,因此溴被称为“海洋元素”。
①该表中溴在元素周期表中的位置为
②该表中最高价氧化物对应的水化物酸性最强的是
③卤素互化物(如IBr)与卤素单质性质相似。已知IBr能与水发生非氧化还原反应,写出IBr与水反应的化学方程式
(2)
 溶于水形成
溶于水形成 溶液,向所得溶液中通入
溶液,向所得溶液中通入 气体,反应生成Se和
气体,反应生成Se和 。写出
。写出 与
与 反应的化学方程式
反应的化学方程式(3)已知某主族元素离子结构示意图为
 ,其中
,其中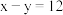 ,此元素与氯元素组成化合物的电子式为
,此元素与氯元素组成化合物的电子式为
您最近一年使用:0次
解题方法
9 . NaOH被大量用于制皂、造纸和纺织品生产。回答下列问题。
(1)H元素位于元素周期表的第_______ 周期第IA族。
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的_______ (填“大”或“小”)。
(3)NaOH所含的两种非金属元素中,非金属性较强的是_______ (填“H”或“O”)。
(4)Na的最高价氧化物对应的水化物的化学式为_______ 。
(1)H元素位于元素周期表的第
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的
(3)NaOH所含的两种非金属元素中,非金属性较强的是
(4)Na的最高价氧化物对应的水化物的化学式为
您最近一年使用:0次
解题方法
10 . NaOH被大量用于制皂、造纸和纺织品生产。回答下列问题。
(1)H元素位于元素周期表的第____ 周期第IA族。
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的____ (填“大”或“小”)。
(3)NaOH所含的两种非金属元素中,非金属性较强的是___ (填“H”或“O”)。
(4)Na的最高价氧化物的化学式为____ 。
(1)H元素位于元素周期表的第
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的
(3)NaOH所含的两种非金属元素中,非金属性较强的是
(4)Na的最高价氧化物的化学式为
您最近一年使用:0次



