解题方法
1 . NaOH被大量用于制皂、造纸和纺织品生产。回答下列问题。
(1)H元素位于元素周期表的第____ 周期第IA族。
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的____ (填“大”或“小”)。
(3)NaOH所含的两种非金属元素中,非金属性较强的是___ (填“H”或“O”)。
(4)Na的最高价氧化物的化学式为____ 。
(1)H元素位于元素周期表的第
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的
(3)NaOH所含的两种非金属元素中,非金属性较强的是
(4)Na的最高价氧化物的化学式为
您最近一年使用:0次
名校
2 . 下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:
(1)金属性最强的是___________ (填元素名称)。
(2)⑨的离子结构示意图为___________ 。
(3)⑤元素和⑩元素的最简单氢化物的稳定性由强到弱的关系是___________ (填化学式)。
(4)④、⑤、⑥的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(5)⑧、⑨、⑩最高价氧化物对应的水化物酸性由弱到强的顺序是___________ (填化学式)
(6)用电子式表示④与⑥形成的原子个数比为1 ∶2的化合物的形成过程___________ 。
(7)⑧单质与⑥的最高价氧化物水化物的溶液发生反应,写出生成的阴离子为___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)⑨的离子结构示意图为
(3)⑤元素和⑩元素的最简单氢化物的稳定性由强到弱的关系是
(4)④、⑤、⑥的简单离子半径由大到小的顺序为
(5)⑧、⑨、⑩最高价氧化物对应的水化物酸性由弱到强的顺序是
(6)用电子式表示④与⑥形成的原子个数比为1 ∶2的化合物的形成过程
(7)⑧单质与⑥的最高价氧化物水化物的溶液发生反应,写出生成的阴离子为
您最近一年使用:0次
2022-01-22更新
|
527次组卷
|
3卷引用:广西百色市2021-2022学年高一上学期期末教学质量调研化学试题
3 . 根据微观结构回答下列问题:
(1)ⅥA族中,原子半径最小的元素是___________ (填元素符号)。
(2)已知碘原子结构示意图如图所示,则:

①碘在元素周期表中的位置为___________ ;
②碘的非金属性比氯___________ (填“强”或“弱”);
③碘元素的最高化合价为___________ ;
④碘的最高价氧化物对应的水化物的化学式为___________ ,属于___________ (填“离子”或“共价”)化合物;
⑤单质碘属于___________ (填“晶体”或“非晶体”);
⑥碘升华克服的作用力是___________ 。
(1)ⅥA族中,原子半径最小的元素是
(2)已知碘原子结构示意图如图所示,则:

①碘在元素周期表中的位置为
②碘的非金属性比氯
③碘元素的最高化合价为
④碘的最高价氧化物对应的水化物的化学式为
⑤单质碘属于
⑥碘升华克服的作用力是
您最近一年使用:0次
名校
4 . 下图是元素周期表的一部分,请回答下列问题:
(1)Z元素在元素周期表中位于第_______ 族。
(2)Z的原子半径_______ (填“大于”“小于”或“等于”)Si的原子半径。
(3)Cl元素的非金属性比Z元素的_______ (填“强”或“弱”)。
(4)Z元素的气态氢化物的化学式为_______ 。
(5)P(红磷)与P4(白磷)是由同种元素组成的不同种物质,二者互为_______ (填“同素异形体”“同分异构体”或“同位素”)。
| 2 | ... | N | O | F | Ne |
| 3 | ... | P | Z | Cl | Ar |
(1)Z元素在元素周期表中位于第
(2)Z的原子半径
(3)Cl元素的非金属性比Z元素的
(4)Z元素的气态氢化物的化学式为
(5)P(红磷)与P4(白磷)是由同种元素组成的不同种物质,二者互为
您最近一年使用:0次
名校
5 . 我国科研团队成功研发“硅—石墨烯—锗晶体管”,代表着我国在这一尖端科技领域走在了世界的前列。
(1)碳元素在元素周期表中的位置是第___ 周期、第IVA族。
(2)硅元素最高价氧化物的化学式为___ 。
(3)在元素周期表中,锗(Ge)位于第4周期,与Si同主族。Ge—Si与Ge—Te作温差发电,可用于宇航、卫星与空间站的启动电源。下列关于Ge的推断中,正确的是___ (填字母)。
a.原子的最外层电子数为4
b.原子半径:Ge>Si
c.最高价氧化物对应的水化物酸性强于H2SiO3
(1)碳元素在元素周期表中的位置是第
(2)硅元素最高价氧化物的化学式为
(3)在元素周期表中,锗(Ge)位于第4周期,与Si同主族。Ge—Si与Ge—Te作温差发电,可用于宇航、卫星与空间站的启动电源。下列关于Ge的推断中,正确的是
a.原子的最外层电子数为4
b.原子半径:Ge>Si
c.最高价氧化物对应的水化物酸性强于H2SiO3
您最近一年使用:0次
6 . 根据题给信息回答问题
(1)某元素原子的价电子构型为4s24p1,它属于第___________ 周期第___________ 族,属于___________ 区元素。
(2)在1~18号元素中,除稀有气体元素外,原子半径最大的元素是___________ (用元素符号表示,下同),电负性最大的元素是___________ ;第一电离能最大的元素是___________ 。第三周期原子半径最小的主族元素的价电子排布式为___________ 。
(3)写出Cu+的核外电子排布式:___________ 。按电子排布,可将周期表中的元素划分成五个区域,第四周期元素中属于s区的元素有___________ 种,
(4)某元素原子的3p轨道有1个未成对电子,该元素为___________ (用元素符号表示)。
(1)某元素原子的价电子构型为4s24p1,它属于第
(2)在1~18号元素中,除稀有气体元素外,原子半径最大的元素是
(3)写出Cu+的核外电子排布式:
(4)某元素原子的3p轨道有1个未成对电子,该元素为
您最近一年使用:0次
2021-07-20更新
|
502次组卷
|
5卷引用:广西钦州市第四中学2022-2023学年高二下学期2月考试化学试题
广西钦州市第四中学2022-2023学年高二下学期2月考试化学试题吉林省通化县综合高级中学2020-2021学年高二下学期期末考试化学试题(已下线)第一章 原子结构与性质 章节过关检测-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)黑龙江省齐齐哈尔市第八中学2021-2022学年高二下学期开学考试化学试题(已下线)专题01 物质的结构与性质-备战2023-2024学年高二化学下学期期末真题分类汇编(辽宁、黑龙江、吉林专用)
7 . 根据下表回答问题:
(1)甲元素最高价氧化物对应的水化物呈___________ 性(填“酸、碱”),乙元素最高价氧化物对应的水化物的化学式为___________ 。
(2)比较这甲、乙、丁三种元素的原子半径大小:___________ (填元素符号)。
(3)丙在周期表的位置为___________ 。
(4)甲元素最高价氧化物对应水化物与丁元素最高价氧化物反应的化学方程式为___________ 。
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 元素符号 | ① | Cl | O | Al |
原子结构示意图 | 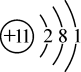 | 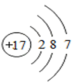 | 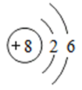 | 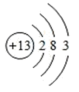 |
| 周期 | 三 | 三 | 二 | 三 |
| 族 | ⅠA | ⅦA | ③ | ⅢA |
(1)甲元素最高价氧化物对应的水化物呈
(2)比较这甲、乙、丁三种元素的原子半径大小:
(3)丙在周期表的位置为
(4)甲元素最高价氧化物对应水化物与丁元素最高价氧化物反应的化学方程式为
您最近一年使用:0次
解题方法
8 . 如表列出了①~⑦七种元素在周期表中的位置:
请按要求回答下列问题:
(1)元素③的原子结构示意图是___________ ,以上元素的最高价氧化物形成的水化物酸性最强的是___________ (填分子式)。
(2)②、③、⑥三种元素的原子形成的简单离子半径由大到小的顺序排列为___________ (用离子符号表示)。
(3)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为___________ 。
(4)②和⑦按原子个数比1:1形成离子化合物乙的电子式为___________
(5)下列物质中,互为同系物的是___________ ,互为同分异构体的是___________ ,互为同素异形体的是___________ ,属于同位素的是___________ 。
①正戊烷 ②白磷 ③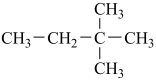 ④
④ ⑤
⑤ ⑥红磷 ⑦
⑥红磷 ⑦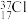
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 二 | ① | ⑦ | ||||||
| 三 | ② | ③ | ④ | ⑤ | ⑥ |
请按要求回答下列问题:
(1)元素③的原子结构示意图是
(2)②、③、⑥三种元素的原子形成的简单离子半径由大到小的顺序排列为
(3)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为
(4)②和⑦按原子个数比1:1形成离子化合物乙的电子式为
(5)下列物质中,互为同系物的是
①正戊烷 ②白磷 ③
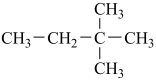 ④
④ ⑤
⑤ ⑥红磷 ⑦
⑥红磷 ⑦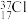
您最近一年使用:0次
2021-06-30更新
|
269次组卷
|
2卷引用:广西岑溪市2020-2021学年高一下学期期末考试化学(理)试题
名校
解题方法
9 . 如图是元素周期表中的一部分,请结合元素周期表和元素周期律回答下列问题。
(1)画出N的原子结构示意图:___ 。
(2)Na与Cl相比,原子半径较大的是:___ 。
(3)F、Cl分别形成的气态氢化物中,更稳定的氢化物是___ 。
周期 族 | ⅠA | 0 | |||||||
| 1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | He | |
| 2 | Li | Be | B | C | N | O | F | Ne | |
| 3 | Na | Mg | ...... | Al | Si | P | S | Cl | Ar |
(2)Na与Cl相比,原子半径较大的是:
(3)F、Cl分别形成的气态氢化物中,更稳定的氢化物是
您最近一年使用:0次
名校
10 . 元素在周期表中的位置反映了元素的原子结构和性质。请回答下列有关硼(B)元素的问题:
(1)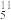 B原子核内的中子数为
B原子核内的中子数为___ 。
(2)铝元素在元素周期表中的位置为第三周期第IIIA族,硼元素在元素周期表中的位置为___ 。
(3)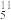 B的原子半径比
B的原子半径比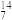 N的原子半径
N的原子半径___ (填“大”或“小”)。
(4)硼元素的最高价氧化物对应的水化物酸性比氮元素的最高价氧化物对应的水化物酸性___ (填“强”或“弱”)。
(1)
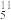 B原子核内的中子数为
B原子核内的中子数为(2)铝元素在元素周期表中的位置为第三周期第IIIA族,硼元素在元素周期表中的位置为
(3)
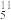 B的原子半径比
B的原子半径比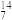 N的原子半径
N的原子半径(4)硼元素的最高价氧化物对应的水化物酸性比氮元素的最高价氧化物对应的水化物酸性
您最近一年使用:0次
2021-05-12更新
|
44次组卷
|
4卷引用:广西兴安县第三中学2019-2020学年高二上学期期中考试化学(文)试题



