1 . 如图是元素周期表的一部分,其中每个数字序号代表一种 短周期元素。根据表中所列①~⑩元素,请按要求回答下列问题:

(1)元素⑤形成的氧化物的电子式为_______ ;①、⑦两种元素的最高价氧化物的熔点较高的是________ (填化学式)。
(2)①~⑨元素的最高价氧化物的水化物中酸性最强的是_______ (填化学式)。
(3)由③④⑩三种元素组成的离子化合物中所含有的化学键有______ 。
(4)①的单质与②的最高价氧化物的水化物的浓溶液反应的化学方程式为_________ 。
(5)下列事实能说明③非金属性比⑧强的有___________ (填字母)。
a.通常状况下,③的单质是无色气体,⑧的单质是固体
b.③的单质与⑧的氢化物溶液反应,溶液变浑浊
c.③与⑧两元素的简单氢化物受热分解,前者的分解温度高
d.常温常压下,③与⑧两元素的简单氢化物的沸点,前者高

(1)元素⑤形成的氧化物的电子式为
(2)①~⑨元素的最高价氧化物的水化物中酸性最强的是
(3)由③④⑩三种元素组成的离子化合物中所含有的化学键有
(4)①的单质与②的最高价氧化物的水化物的浓溶液反应的化学方程式为
(5)下列事实能说明③非金属性比⑧强的有
a.通常状况下,③的单质是无色气体,⑧的单质是固体
b.③的单质与⑧的氢化物溶液反应,溶液变浑浊
c.③与⑧两元素的简单氢化物受热分解,前者的分解温度高
d.常温常压下,③与⑧两元素的简单氢化物的沸点,前者高
您最近一年使用:0次
解题方法
2 . 元素周期表的一部分如图所示,回答下列问题:
(l)X的原子结构示意图为____________ 。
(2)Y元素位于元素周期表中第_______ 周期__________ 族。
(3)X、Y原子半径由大到小的顺序为__ (填化学式,下同),Z、Y最简单氢化物热稳定性由强到弱的顺序为__ 。
(4)W的最高价氧化物对应水化物的化学式为______ ,该水化物中含有______ (填“共价键”、“离子键’)。
| 族 周期 | IA | 0 | |||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | X | Y | |||||||
| 3 | Z | ||||||||
| 4 | W | …… |
(l)X的原子结构示意图为
(2)Y元素位于元素周期表中第
(3)X、Y原子半径由大到小的顺序为
(4)W的最高价氧化物对应水化物的化学式为
您最近一年使用:0次
2020-08-15更新
|
82次组卷
|
2卷引用:广西壮族自治区北海市2019-2020学年高一下学期期末教学质量检测化学试题
3 . 图为周期表的一部分,表中所列字母分别代表周期表对应的化学元素,针对所列元素回答问题
(1)元素C在周期表的位置是_______
(2)元素A和B形成的二元化合物中,能标志一个国家石油化学工业发展水平的_______ (填化学式),该物质使溴的四氯化碳溶液褪色的化学方程式为_______
(3)能形成两性氢氧化物的元素是______ (填元素符号)。
(4)元素G 、H 、I形成的简单离子中,半径最大的是______ (填离子符号)。
(5)E单质在H单质中燃烧的现象是_______ ,生成物的电子式为_______
(6)元素C和D的最简单氢化物中,沸点比较高的是__________ (填化学式);E和D形成的化合物E2D2和水反应的化学方程式是_______
| A | |||||||||||||||||
| B | C | D | |||||||||||||||
| E | F | G | H | ||||||||||||||
| I |
(1)元素C在周期表的位置是
(2)元素A和B形成的二元化合物中,能标志一个国家石油化学工业发展水平的
(3)能形成两性氢氧化物的元素是
(4)元素G 、H 、I形成的简单离子中,半径最大的是
(5)E单质在H单质中燃烧的现象是
(6)元素C和D的最简单氢化物中,沸点比较高的是
您最近一年使用:0次
名校
4 . 依据下表选择有关序号,并用相应的元素符号或化学式填空。
(1)这些元素中,_____ 是最活泼的金属元素;_____ 是最活泼的非金属元素;_______ 是最不活泼的元素。
(2)短周期元素最高价氧化物对应的水化物中,________ 酸性最强;________ 碱性最强;________ 呈两性。
(3)⑥和⑭的金属性较强的是________ ;其最高价氧化物的水化物的碱性强弱顺序是________ 。
(4)第三周期的元素中,______ 原子半径最大。
(5)在所形成的气态氢化物中,最稳定的是__________ 。
(6)①元素能形成多种同素异形体,举出两种单质的例子________ 、________ 。
(7)②元素与氢元素可形成多种10电子微粒,列举两例________ 、________ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | H | |||||||
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
| 四 | ⑬ | ⑭ | …… |
(1)这些元素中,
(2)短周期元素最高价氧化物对应的水化物中,
(3)⑥和⑭的金属性较强的是
(4)第三周期的元素中,
(5)在所形成的气态氢化物中,最稳定的是
(6)①元素能形成多种同素异形体,举出两种单质的例子
(7)②元素与氢元素可形成多种10电子微粒,列举两例
您最近一年使用:0次
名校
5 . 元素①~⑩在周期表中的位置如表所示,请回答下列有关问题。
(1)写出下列元素的符号:①__________ ;⑦__________ 。
(2)在这些元素中,最不活泼的元素是__________ (填元素符号,下同)。
(3)③与④比较,化学性质较活泼的是__________ 。
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(2)在这些元素中,最不活泼的元素是
(3)③与④比较,化学性质较活泼的是
您最近一年使用:0次
名校
6 . 第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
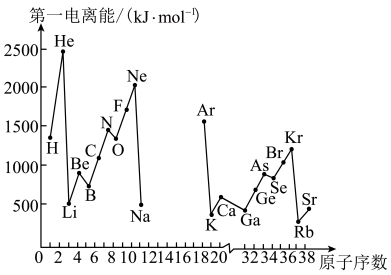
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为____ <Al<__ ;(填元素符号)
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是_____ 。
(3)上图中第一电离能最小的元素在周期表中的位置是第________ 周期________ 族;

(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是
(3)上图中第一电离能最小的元素在周期表中的位置是第
您最近一年使用:0次
名校
7 . 下表是元素周期表的一部分,请回答:
(1)元素⑦的原子结构示意图为_____ ;元素⑩的名称为______ ;
(2)在这些元素中,化学性质最活泼的金属元素是____ (填元素符号,下同),最不活泼的元素是___ ;原子半径最小的元素是_____ ;
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是___ (填化学式,下同);具有两性的是____ 。
| 族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(1)元素⑦的原子结构示意图为
(2)在这些元素中,化学性质最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
8 . (1)元素周期表有______ 个横行、________________ 个周期,每一周期中元素原子的_________ 相同,从左到右原子半径依次___________________ (填“增大”或“减小”)、核对外层电子的引力逐渐________ (填“增强”或“减弱”) 、元素失电子能力逐渐________ (填“增强”或“减弱”)、元素的非金属性________ (填“增强”或“减弱”)、阴离子的还原性_________ (填“增强”或“减弱”)、最高价氧化物对应水化物酸性________ (填“增强”或“减弱”)、气态氢化物的稳定性________ (填“增强”或“减弱”);
(2)元素周期表有____ 纵列、_______________ 个族,第ⅥA族处在第_______ 列,同一主族从上到下,元素的金属性依次_________ (填“增强”或“减弱”)、元素失电子的能力________ (填“增强”或“减弱”)、阳离子的氧化性________ (填“增强”或“减弱”)、最高价氧化物对应水化物酸性________ (填“增强”或“减弱”)。
(2)元素周期表有
您最近一年使用:0次
2019-05-28更新
|
164次组卷
|
3卷引用:广西贵港市立德高中2020-2021学年高一3月月考化学试题
名校
9 . 下表是元素周期表短周期的一部分:
请按要求用化学用语回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为________________ ;
(2)元素②、③、④的简单氢化物的沸点由低到高的顺序:_____________________ ;
(3)用电子式表示元素④与元素⑥形成的化合物的形成过程____________ ;
(4)比元素⑦的原子序数多17的元素在周期表的位置为________________ ;
(5)写出由①④⑤三种元素组成的一种离子化合物的电子式_______________ ,若将其溶于水,破坏了其中的__________ (填“离子键”、“共价键”或“离子键和共价键”);
(6)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物按物质的量之比4 :1反应的离子方程式________ 。

请按要求用化学用语回答下列问题:
(1)元素④、⑥、⑨的离子半径由大到小的顺序为
(2)元素②、③、④的简单氢化物的沸点由低到高的顺序:
(3)用电子式表示元素④与元素⑥形成的化合物的形成过程
(4)比元素⑦的原子序数多17的元素在周期表的位置为
(5)写出由①④⑤三种元素组成的一种离子化合物的电子式
(6)元素①和元素④形成的化合物及元素①和元素⑧形成的化合物均为18电子分子,请写出这两种化合物按物质的量之比4 :1反应的离子方程式
您最近一年使用:0次
2019-05-09更新
|
2349次组卷
|
3卷引用:【全国百强校】广西壮族自治区南宁市第三中学2018-2019学年高一(理)下学期期中考试化学试题
名校
10 . 元素在周期表中的位置反映了元素的原子结构和性质。请回答下列有关硼(B)元素的问题:
(1)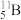 原子核内的中子数为
原子核内的中子数为________ 。
(2)硼元素在元素周期表中的位置为___________ 。
(3)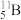 的原子半径
的原子半径__________ 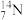 的原子半径(填“大于”或“小于”)。
的原子半径(填“大于”或“小于”)。
(4)硼元素的最高价氧化物对应的水化物酸性比氮元素的最高价氧化物对应的水化物酸性_______ (填“强”或“弱”)。
(5)四氢硼锂(LiBH4)是一种重要的化学试剂,低温下可与HCl气体发生如下反应:2 LiBH4 + 2 HCl = 2 LiCl + B2H6 + 2H2该反应中,LiBH4和B2H6中的氢元素均显-1价。请回答下列问题。LiBH4中硼元素的化合价为__________ ;该反应的还原剂为____________ ;4 mol LiBH4完全反应后共失去_____ mol电子。
(1)
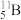 原子核内的中子数为
原子核内的中子数为(2)硼元素在元素周期表中的位置为
(3)
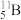 的原子半径
的原子半径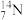 的原子半径(填“大于”或“小于”)。
的原子半径(填“大于”或“小于”)。(4)硼元素的最高价氧化物对应的水化物酸性比氮元素的最高价氧化物对应的水化物酸性
(5)四氢硼锂(LiBH4)是一种重要的化学试剂,低温下可与HCl气体发生如下反应:2 LiBH4 + 2 HCl = 2 LiCl + B2H6 + 2H2该反应中,LiBH4和B2H6中的氢元素均显-1价。请回答下列问题。LiBH4中硼元素的化合价为
您最近一年使用:0次



