名校
1 . 下列说法是否正确(正确的打“√”,不正确的打“×”)若不正确请说明理由。
(1)元素周期表中每一横行称为一周期,每一纵列称为一个族。_________ ;
(2)FeCl3与Cu的反应为置换反应。_________ ;
(3)1 mol Na2O溶于水中形成1 L溶液,所得溶液的物质的量浓度为1 mol/L。_________ ;
(4)镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料。_________
(1)元素周期表中每一横行称为一周期,每一纵列称为一个族。
(2)FeCl3与Cu的反应为置换反应。
(3)1 mol Na2O溶于水中形成1 L溶液,所得溶液的物质的量浓度为1 mol/L。
(4)镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料。
您最近一年使用:0次
2 . 元素周期表中,铍(Be)与铝处于对角线的位置,它们的性质相似。试回答:
(1)Be元素在元素周期表中的位置:___________ ,有关Be性质的推断不正确的是___________ (填序号)。
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点,能耐酸碱
c.常温时, 溶液的
溶液的
(2)已知: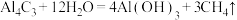 ,写出
,写出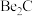 与NaOH溶液反应的离子方程式(铍酸根离子为
与NaOH溶液反应的离子方程式(铍酸根离子为 ):
):___________
(3)基态铝原子的价电子排布式为___________ ,镁铝合金经过高温淬火获得一种储钠材料,用___________ 法测定其晶胞结构如图1所示,图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为___________ ,该立方晶胞的晶胞的密度为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶胞中镁铝之间的最近距离为
,则该晶胞中镁铝之间的最近距离为___________ pm。(列出计算式,可不化简)。
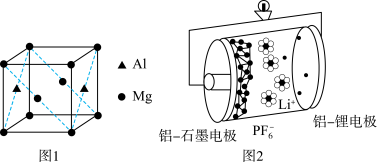
(4)铝石墨双离子电池是一种全新的低成本、高效能电池,反应原理为: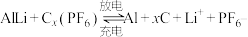 ,电池结构如图2所示。放电时,正极反应式为
,电池结构如图2所示。放电时,正极反应式为___________ ,充电时,应将铝-石墨电极与外接电源的___________ 极相连。
(1)Be元素在元素周期表中的位置:
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点,能耐酸碱
c.常温时,
 溶液的
溶液的
(2)已知:
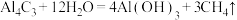 ,写出
,写出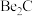 与NaOH溶液反应的离子方程式(铍酸根离子为
与NaOH溶液反应的离子方程式(铍酸根离子为 ):
):(3)基态铝原子的价电子排布式为
 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶胞中镁铝之间的最近距离为
,则该晶胞中镁铝之间的最近距离为
(4)铝石墨双离子电池是一种全新的低成本、高效能电池,反应原理为:
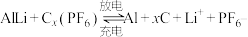 ,电池结构如图2所示。放电时,正极反应式为
,电池结构如图2所示。放电时,正极反应式为
您最近一年使用:0次
解题方法
3 . 按要求完成下列问题。
(1)硒(Se)是人体必需的微量元素,与O为同一主族元素,Se原子比O原子多两个电子层,则Se的原子序数为____ ,其最高价氧化物对应的水化物化学式为____ 。
(2)X射线衍射法可以测定某些分子结构,NH3分子结构为_____ 。
(3)水在液态时,几个水分子可以形成缔合水分子(H2O)n的原因是水分子之间存在____ 。
(4)漂白粉(有效成分Ca(ClO)2)与空气中CO2和水蒸气反应的化学方程式:____ 。
(5)完成氧化还原反应的离子方程式:____ 。
Cr2O +Fe2++_____=Cr3++Fe3++____
+Fe2++_____=Cr3++Fe3++____
(6)一定条件下金属钠和H2反应生成甲,甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。化合物甲和NaAlH4都是重要的还原剂。将4.80g甲加热至完全分解,得到金属钠和2.24L(已折算成标准状况)的H2。
①甲的化学式____ 。
②甲与AlCl3反应得到NaAlH4的化学方程式:____ 。
③NaAlH4与水发生氧化还原反应的化学方程式:____ 。
④甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式:____ 。
(1)硒(Se)是人体必需的微量元素,与O为同一主族元素,Se原子比O原子多两个电子层,则Se的原子序数为
(2)X射线衍射法可以测定某些分子结构,NH3分子结构为
(3)水在液态时,几个水分子可以形成缔合水分子(H2O)n的原因是水分子之间存在
(4)漂白粉(有效成分Ca(ClO)2)与空气中CO2和水蒸气反应的化学方程式:
(5)完成氧化还原反应的离子方程式:
Cr2O
 +Fe2++_____=Cr3++Fe3++____
+Fe2++_____=Cr3++Fe3++____(6)一定条件下金属钠和H2反应生成甲,甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。化合物甲和NaAlH4都是重要的还原剂。将4.80g甲加热至完全分解,得到金属钠和2.24L(已折算成标准状况)的H2。
①甲的化学式
②甲与AlCl3反应得到NaAlH4的化学方程式:
③NaAlH4与水发生氧化还原反应的化学方程式:
④甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式:
您最近一年使用:0次
2022-11-16更新
|
159次组卷
|
2卷引用:天津市部分区2022-2023学年高三上学期期中考试化学试题
4 . 如图是氨元素的几种价态与物质类别的对应关系:

回答下列问题:
(1)写出氮元素在元素周期表的位置_______ 。
(2)从氢元素化合价分析, 具有氧化性和还原性。写出
具有氧化性和还原性。写出 生成A的化学反应方程式:
生成A的化学反应方程式:_______ ,这个反应 体现了
体现了_______ 性。
(3) 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为_______ 。写出用C检验 的存在的离子方程式
的存在的离子方程式_______ 。
(4)物质B为氮元素的气态氢化物,B的化学式为_______ ;实验室制取B的化学方程式为_______ 。
(5)浓硝酸与木炭在加热条件下反应的化学方程式为_______ 。

回答下列问题:
(1)写出氮元素在元素周期表的位置
(2)从氢元素化合价分析,
 具有氧化性和还原性。写出
具有氧化性和还原性。写出 生成A的化学反应方程式:
生成A的化学反应方程式: 体现了
体现了(3)
 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为 的存在的离子方程式
的存在的离子方程式(4)物质B为氮元素的气态氢化物,B的化学式为
(5)浓硝酸与木炭在加热条件下反应的化学方程式为
您最近一年使用:0次
名校
解题方法
5 . 已知主族元素,A、B、C、D、E的原子的结构示意图分别为:
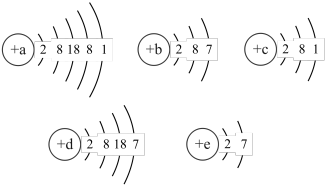
请回答下列问题:
(1)属于同周期的元素是___________ (填元素符号,下同)。
(2)A、B、C、D、E中属于短周期元素的是___________ 。
(3)上述元素形成的单质氧化性最强的是___________ (填化学式)。
(4)aA在周期表中的位置___________ 周期___________ 族。
(5)金属性最强的元素是___________ 。
(6)C、D元素可形成离子化合物,该化合物的电子式为___________ 。
(7)B、C、E形成的简单离子半径最小的是___________ (填离子符号)。

请回答下列问题:
(1)属于同周期的元素是
(2)A、B、C、D、E中属于短周期元素的是
(3)上述元素形成的单质氧化性最强的是
(4)aA在周期表中的位置
(5)金属性最强的元素是
(6)C、D元素可形成离子化合物,该化合物的电子式为
(7)B、C、E形成的简单离子半径最小的是
您最近一年使用:0次
2022-03-05更新
|
275次组卷
|
2卷引用:天津市部分区2021-2022学年高一上学期期末(下学期期初)考试化学试题
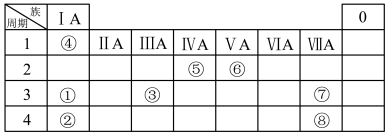
6 . 几种主族元素在周期表中的位置如下
(1)⑥元素的简单氢化物的化学式是_______ 。
(2)①③⑦三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为_______ ,该元素在周期表中的位置是_______ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是_______ (填化学式)①与③最高价氧化物对应水化物反应的离子方程_______ 。
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:_______ 。下列表述中能证明这一事实的是_______ (填字母)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱
(1)⑥元素的简单氢化物的化学式是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱
您最近一年使用:0次
2022-01-22更新
|
914次组卷
|
4卷引用:天津市武清区黄花店中学2023-2024学年高三上学期第二次练习化学试题
天津市武清区黄花店中学2023-2024学年高三上学期第二次练习化学试题广东省湛江市2021-2022学年高一上学期期末调研考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第四单元02基础练(已下线)专题突破卷05?物质结构 元素周期律?-2024年高考化学一轮复习考点通关卷(新教材新高考)
名校
7 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
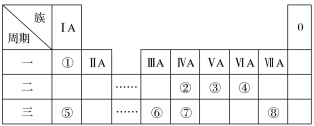
(1)②的元素符号是___________ ;⑦的一种中子数为14的原子符号为___________ 。
(2)①③④三种元素可形成含10个电子的分子分别是___________ 、___________ 。(填化学式)
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为___________ ,该元素在周期表中的位置是___________ 。
(4)⑤的单质与D2O反应的离子方程式为___________ 。
(5)⑥的单质与氢氧化钠溶液反应的离子方程式为___________ 。
(6)实验室制备⑧单质的化学方程式为___________ 。

(1)②的元素符号是
(2)①③④三种元素可形成含10个电子的分子分别是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)⑤的单质与D2O反应的离子方程式为
(5)⑥的单质与氢氧化钠溶液反应的离子方程式为
(6)实验室制备⑧单质的化学方程式为
您最近一年使用:0次
名校
解题方法
8 . 1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一、元素周期表与元素周期律在化学学习研究中有很重要的作用。
(1)下表是元素周期表的一部分
i.元素④的过氧化物的电子式为___________ ,其最高价氧化物对应的水化物含有的化学键类型为___________ ,⑩元素最高价氧化物对应的水化物的化学式是___________ 。
ii.元素①、②、③的简单氢化物的稳定性最强的是___________ (用化学式表示,下同),②、⑧简单氢化物熔点高的是___________ ,④、⑤最高价氧化物的水化物碱性更强的是___________ ,④、⑤、⑧、⑨的简单离子半径由大到小的顺序(用离子符号表示)___________ 。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置___________ 。
ii.铷单质性质活泼写出在点燃条件下它与氯气反应的化学方程式:___________ ;铷单质易与水反应,反应的离子方程式为___________ ,实验表明铷与水反应比钠与水反应___________ (填“剧烈”或“缓慢”);反应过程中铷在水___________ (填“面”或“底”)与水反应。同主族元素的同类化合物的化学性质相似,写出过氧化铷与 反应的化学方程式:
反应的化学方程式:___________ 。
(1)下表是元素周期表的一部分
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 四 | ⑩ |
i.元素④的过氧化物的电子式为
ii.元素①、②、③的简单氢化物的稳定性最强的是
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置
ii.铷单质性质活泼写出在点燃条件下它与氯气反应的化学方程式:
 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
名校
解题方法
9 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
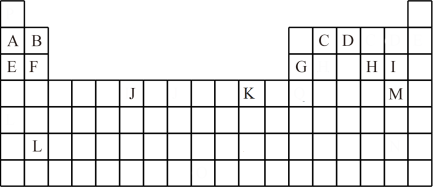
试回答下列问题:
(1)写出基态 原子的电子排布式:
原子的电子排布式:_______ , 的原子序数:
的原子序数:_______ , 的简化电子排布式:
的简化电子排布式:_______ 。
(2)下列关于元素在元素周期表中的位置的叙述正确的是_______ (填选项字母)。
A. 位于元素周期表中第四周期第ⅡB族,属于
位于元素周期表中第四周期第ⅡB族,属于 区元素
区元素
B. 位于元素周期表中第四周期第ⅣB族,属于
位于元素周期表中第四周期第ⅣB族,属于 区元素
区元素
C. 位于元素周期表中第三周期第ⅡA族,属于
位于元素周期表中第三周期第ⅡA族,属于 区元素
区元素
D. 位于元素周期表中第三周期第ⅦA族,属于
位于元素周期表中第三周期第ⅦA族,属于 区元素
区元素
(3)下列有关说法正确的是_______ (填选项字母)。
A.第一电离能:G>F>E B.电负性:D>C C.原子半径:B>E D.最高价含氧酸的酸性:I>H

试回答下列问题:
(1)写出基态
 原子的电子排布式:
原子的电子排布式: 的原子序数:
的原子序数: 的简化电子排布式:
的简化电子排布式:(2)下列关于元素在元素周期表中的位置的叙述正确的是
A.
 位于元素周期表中第四周期第ⅡB族,属于
位于元素周期表中第四周期第ⅡB族,属于 区元素
区元素B.
 位于元素周期表中第四周期第ⅣB族,属于
位于元素周期表中第四周期第ⅣB族,属于 区元素
区元素C.
 位于元素周期表中第三周期第ⅡA族,属于
位于元素周期表中第三周期第ⅡA族,属于 区元素
区元素D.
 位于元素周期表中第三周期第ⅦA族,属于
位于元素周期表中第三周期第ⅦA族,属于 区元素
区元素(3)下列有关说法正确的是
A.第一电离能:G>F>E B.电负性:D>C C.原子半径:B>E D.最高价含氧酸的酸性:I>H
您最近一年使用:0次
2021-01-19更新
|
1117次组卷
|
4卷引用:天津市耀华中学2020-2021学年高二上学期期末考试化学试题
天津市耀华中学2020-2021学年高二上学期期末考试化学试题(已下线)专题二 原子结构与元素的性质-2020-2021学年高二《新题速递·化学》(人教版选修3)2月刊 (同步课堂必刷题)(已下线)专题二 原子结构与元素的性质-2020-2021学年高二《新题速递·化学》(人教版2019选择性必修2)2月刊 (同步课堂必刷题)第一章原子结构与性质(提升卷)
10 . 下表列出了①~⑩十种元素在周期表中的位置:
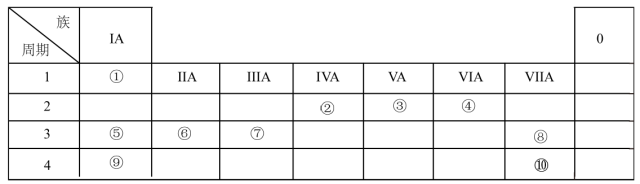
请按要求回答下列问题:
(1)元素⑤的原子结构示意图为___ ;元素②的最高价氧化物的电子式是___ 。
(2)⑤、⑥、⑨三种元素原子半径由大到小的顺序是___ (填元素符号);这三种元素最高价氧化物对应水化物中碱性最强的是___ (填化学式)。
(3)③、④元素的简单氢化物的稳定性较弱的是___ (填化学式)。
(4)①、②、④三种元素形成的有机物的分子结构模型如图所示,写出该有机物的结构简式:___ ;①与②所形成的最简单的烯烃与溴的四氯化碳溶液反应的化学方程式:___ 。

(5)元素⑦的最高价氧化物对应的水化物与氢氧化钠溶液反应的离子方程式:___ 。
(6)写出元素⑨的单质与水反应的化学方程式:___ 。
(7)请从原子结构的角度解释,元素⑧非金属性比元素⑩强的原因:___ 。

请按要求回答下列问题:
(1)元素⑤的原子结构示意图为
(2)⑤、⑥、⑨三种元素原子半径由大到小的顺序是
(3)③、④元素的简单氢化物的稳定性较弱的是
(4)①、②、④三种元素形成的有机物的分子结构模型如图所示,写出该有机物的结构简式:

(5)元素⑦的最高价氧化物对应的水化物与氢氧化钠溶液反应的离子方程式:
(6)写出元素⑨的单质与水反应的化学方程式:
(7)请从原子结构的角度解释,元素⑧非金属性比元素⑩强的原因:
您最近一年使用:0次
2020-07-11更新
|
349次组卷
|
2卷引用:天津市南开区2020届高中学业水平合格性考试模拟试卷化学试题



