23-24高二下·全国·课后作业
1 . 1869年俄国科学家门捷列夫绘制出了第一张元素周期表,成为化学史上的里程碑之一,且大大地促进了化学学科的快速发展。下表是现代元素周期表的一部分,请据表回答下列问题:
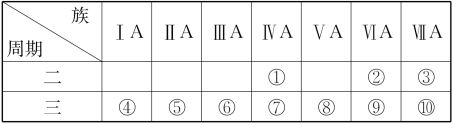
(1)元素③的名称是___________ ,金属性最强的元素是___________ (填元素符号)。
(2)①②⑤三种元素原子半径由大到小的顺序为___________ (填序号)。
(3)元素⑦的单质的一种用途是___________ (填写“制造玻璃”或“制造计算机芯片”)。
(4)元素⑧⑨⑩最高价氧化物的水化物中酸性最强的是___________ (填化学式)。

(1)元素③的名称是
(2)①②⑤三种元素原子半径由大到小的顺序为
(3)元素⑦的单质的一种用途是
(4)元素⑧⑨⑩最高价氧化物的水化物中酸性最强的是
您最近一年使用:0次
2 . 核外电子排布与元素周期系的基本结构
①根据构造原理得出的核外电子排布可以解释元素周期系中每个周期的元素数。第一周期从1s1开始,以1s2结束,只有_______ 种元素。其余各周期总是从ns能级开始,以np结束,而从ns能级开始以np结束递增的核电荷数(或电子数)就_______ 每个周期里的元素数。
②周期、能级组、元素种类的对应关系
①根据构造原理得出的核外电子排布可以解释元素周期系中每个周期的元素数。第一周期从1s1开始,以1s2结束,只有
②周期、能级组、元素种类的对应关系
| 周期 | 对应能级组 | 对应能级组最多所能容纳的电子数 | 周期中所含元素种类 |
| 1 | 1s | 2 | 2 |
| 2 | 8 | ||
| 3 | 3s、3p | 8 | 8 |
| 4 | 18 | ||
| 5 | 5s、4d、5p | 18 | 18 |
| 6 | 32 | ||
| 7 | 7s、5f、6d、7p | 32 | 32 |
您最近一年使用:0次
3 . 元素在周期表中的位置与元素原子的结构、性质间的关系
(1)在元素周期表中,同族元素价层电子数_______ ,是同族元素性质_______ 的结构基础。
(2)长周期比短周期多出的元素,其原子的最外层电子数_______ 2(Pd除外),所以它们全部是_______ 。
(1)在元素周期表中,同族元素价层电子数
(2)长周期比短周期多出的元素,其原子的最外层电子数
您最近一年使用:0次
4 . 核外电子排布与元素周期表的分区
按电子排布式中最后填入电子的_______ 可将元素周期表分为s、p、d、f4个区,而IB、IIB族这2个纵行的元素的核外电子可理解为先填满了_______ 能级而后再填充_______ 能级而得名ds区。5个区的位置关系如下图所示:
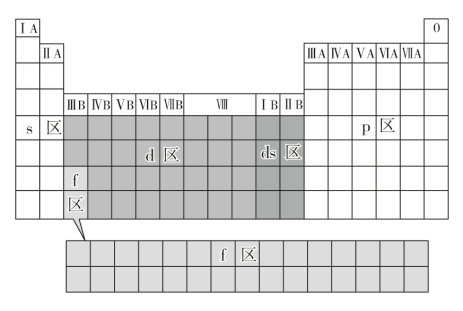
按电子排布式中最后填入电子的

您最近一年使用:0次
23-24高一下·全国·课前预习
5 . 元素周期系和元素周期表
按元素原子的_______ 递增排列的序列叫元素周期系。元素周期表是呈现元素周期系的_______ 。元素周期系_______ ,元素周期表_______ 。
按元素原子的
您最近一年使用:0次
6 . 元素周期表是元素周期律的具体表现形式,是学习和研究化学的重要工具,下图是元素周期表的一部分。

(1)氧元素在周期表中的位置是第_______ 周期_______ 族,氧原子的电子式为_______ 。
(2)某元素的结构示意图为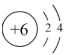 ,请在上图相应位置填入该元素的元素符号
,请在上图相应位置填入该元素的元素符号_______ 。
(3)元素性质呈现周期性变化的根本原因是_______。

(1)氧元素在周期表中的位置是第
(2)某元素的结构示意图为
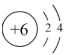 ,请在上图相应位置填入该元素的元素符号
,请在上图相应位置填入该元素的元素符号(3)元素性质呈现周期性变化的根本原因是_______。
| A.元素相对原子质量的递增 |
| B.元素原子半径呈现周期性变化 |
| C.元素原子核外电子排布呈现周期性变化 |
| D.元素金属性和非金属性呈现周期性变化 |
您最近一年使用:0次
7 . 已知元素周期表中共有18纵行,如图实线表示元素周期表的边界。按电子排布,可把周期表里的元素划分为几个区:s区、p区、d区、ds区等。除ds区外,其他区的名称来自按构造原理最后填入的电子的能级符号。
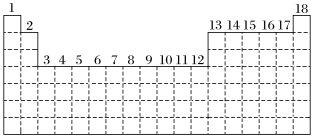
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影 和
和 表示d区和ds区。
表示d区和ds区。___________
(2)有的同学受这种划分的启发,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在___________ 区。
(3)随着科学技术的发展,不断有新的元素被发现。若把第七周期排满,则元素周期表共可以排布___________ 种元素。

(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影
 和
和 表示d区和ds区。
表示d区和ds区。(2)有的同学受这种划分的启发,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在
(3)随着科学技术的发展,不断有新的元素被发现。若把第七周期排满,则元素周期表共可以排布
您最近一年使用:0次
2023高三·全国·专题练习
8 . 1869年,俄国化学家门捷列夫提出了元素周期律,并在此基础上发表了第一张元素周期表。为了纪念元素周期表诞生150年,联合国将2019年定为“国际化学元素周期表年”,并认为元素周期表是“科学共同的语言”。
(1)认识元素周期表的结构:
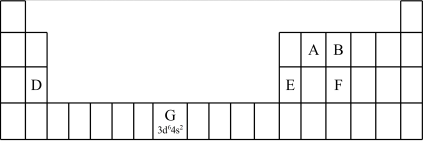
①在元素周期表中,第ⅠB、ⅡB元素属于___________ 区。
②2017年5月9日我国发布了113号Nh、115号Mc、117号Ts、118号Og四种元素,则下列说法正确的是___________ (填字母序号)。
a.113号元素在周期表中的位置是第七周期VB族
b.117号元素Ts位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:Nh>Mc
(2)认识原子结构与元素周期表的关系:见表中元素G的信息,其中“3d64s2”称为该元素原子的___________ ,该元素M能层上具有___________ 种不同运动状态的电子。
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D___________ E(填“>”“<”或“=”)。
②气态氢化物的沸点:B___________ F(填“>”“<”或“=”),理由是___________ 。
(1)认识元素周期表的结构:

①在元素周期表中,第ⅠB、ⅡB元素属于
②2017年5月9日我国发布了113号Nh、115号Mc、117号Ts、118号Og四种元素,则下列说法正确的是
a.113号元素在周期表中的位置是第七周期VB族
b.117号元素Ts位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:Nh>Mc
(2)认识原子结构与元素周期表的关系:见表中元素G的信息,其中“3d64s2”称为该元素原子的
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:D
②气态氢化物的沸点:B
您最近一年使用:0次
9 . 请根据构造原理,按要求写出下列电子排布式或原子结构示意图:
(1)16S的电子排布式___________ 。
(2)29Cu的简化电子排布式___________ 。
(3)某元素原子的电子排布式为[Ar]3d104s24p3,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:
①该元素处于元素周期表的第___________ 周期。
②该元素处于元素周期表的第___________ 族。
③试推测该元素处于元素周期表的___________ 区。
(1)16S的电子排布式
(2)29Cu的简化电子排布式
(3)某元素原子的电子排布式为[Ar]3d104s24p3,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:
①该元素处于元素周期表的第
②该元素处于元素周期表的第
③试推测该元素处于元素周期表的
您最近一年使用:0次
23-24高一上·福建泉州·阶段练习
10 . 按要求填空。
(1)已知A原子,其核外电子数为17,则A是_______ (填元素符号)。
(2)已知B原子,L层上的电子数为K层的3倍,则其原子结构示意图是_______ 。
(3)已知C原子,其最外层电子数等于次外层电子数的2倍,则C的元素名称是_______ 。
(4)某元素D的原子得到2个电子后,电子层排布与氖原子相同的,写出该元素的离子结构示意图_______ 。
(1)已知A原子,其核外电子数为17,则A是
(2)已知B原子,L层上的电子数为K层的3倍,则其原子结构示意图是
(3)已知C原子,其最外层电子数等于次外层电子数的2倍,则C的元素名称是
(4)某元素D的原子得到2个电子后,电子层排布与氖原子相同的,写出该元素的离子结构示意图
您最近一年使用:0次



