名校
解题方法
1 . 下表列出了①~⑥六种元素在周期表中的位置。
请按要求回答下列问题:
(1)写出①的元素符号___________________ 。
(2)⑥的原子结构示意图是_______________ 。
(3)写出③与⑤的单质反应的化学方程式__________________________ 。
(4)③和④中金属性较弱的是_______________ (填化学式)。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||
(1)写出①的元素符号
(2)⑥的原子结构示意图是
(3)写出③与⑤的单质反应的化学方程式
(4)③和④中金属性较弱的是
您最近一年使用:0次
2017-07-01更新
|
95次组卷
|
3卷引用:宁夏育才中学2016-2017学年高一7月学业水平文化课模拟考试化学试题
名校
2 . 硫化锌荧光材料的研究从1868年法国化学家Sidot发现至今已有近150年的历史。其中立方硫化锌的晶胞如图所示。请回答下列问题:
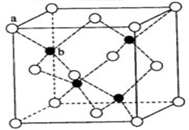
(1)锌元素在周期表中的位于第______ 周期_____ 族, 属于_____ 区;
(2)基态锌原子的价电子排布式为_________ ;
(3)一般锌元素常表现为+2 价的原因是_____ ;
(4)立方硫化锌晶体的每个晶胞中含有_____ 个锌离子, 其配位数为_____ ;含有_____ 个硫离子,其配位数为_____ ;
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,其晶胞边长为540.0 pm,密度为_________ g·cm-3(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为_____ pm(列式表示)。

(1)锌元素在周期表中的位于第
(2)基态锌原子的价电子排布式为
(3)一般锌元素常表现为+2 价的原因是
(4)立方硫化锌晶体的每个晶胞中含有
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,其晶胞边长为540.0 pm,密度为
您最近一年使用:0次
名校
3 . 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)上述十种元素中,最高价氧化物水化物酸性最强的化合物的化学式是___________ ,(填化学符号 ,下同),最高价氧化物水化物碱性最强的化合物的化学式是_____________ ,最高价氧化物水化物显两性的氢氧化物的化学式是_____________ 。
(2)③与④的气态氢化物的稳定性由大到小的顺序是_____________ 。
(3)④、⑤、⑥的离子半径由大到小的顺序是__________________ 。
(4)①、③形成的阳离子的电子式是______________ 。
(5)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:______________ 。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)上述十种元素中,最高价氧化物水化物酸性最强的化合物的化学式是
(2)③与④的气态氢化物的稳定性由大到小的顺序是
(3)④、⑤、⑥的离子半径由大到小的顺序是
(4)①、③形成的阳离子的电子式是
(5)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
您最近一年使用:0次
名校
4 . 下表列出了①~⑨九种元素在周期表中的位置。
请按要求回答下列问题:
(1)①~⑨九种元素中非金属性最强的是________ (填元素符号)。
(2)元素⑧的原子结构示意图是_________ ;由①、④、⑥三种元素组成的化合物,其电子式是_________ 。
(3)元素②、⑧的气态氢化物的稳定性较强的是________________ (填化学式);元素③、⑨的最高价氧化物对应的水化物的酸性较强的是________________ (填化学式)。
(4)③、④、⑧三种元素的原子半径由大到小的顺序是________________ (填元素符号)。
(5)元素⑤、⑥组成的化合物的化学键类型是________________________ 。
(6)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式是________________
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
请按要求回答下列问题:
(1)①~⑨九种元素中非金属性最强的是
(2)元素⑧的原子结构示意图是
(3)元素②、⑧的气态氢化物的稳定性较强的是
(4)③、④、⑧三种元素的原子半径由大到小的顺序是
(5)元素⑤、⑥组成的化合物的化学键类型是
(6)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式是
您最近一年使用:0次
2016-12-09更新
|
654次组卷
|
6卷引用:宁夏吴忠中学2019-2020学年高一下学期期末考试化学试题
12-13高一下·广东东莞·期中
名校
解题方法
5 . 下表是周期表中的一部分,根据A-I在周期表中的位置,第(1)~ (4)小题用元素符号或化学式回答,(5)~(8)小题按题目要求回答。
(1)表中元素,化学性质最不活泼的是_______ ,只有负价而无正价的是________ ,氧化性最强的单质是______ ,还原性最强的单质是________ 。
(2)最高价氧化物的水化物碱性最强的是___ ,酸性最强的是____ ,呈两性的是 _______ 。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的______________ ,
(4)在B、C、E、F、G、H中,原子半径最大的是_________ ,
(5)A和D组成化合物的电子式_____________________ ,
(6)A和E组成化合物的化学式_____________________ ,
(7)用电子式表示B和H组成化合物的形成过程______________________________ ,
(8)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式___________________________________________ 。
| 族 周期 | I A | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)最高价氧化物的水化物碱性最强的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的
(4)在B、C、E、F、G、H中,原子半径最大的是
(5)A和D组成化合物的电子式
(6)A和E组成化合物的化学式
(7)用电子式表示B和H组成化合物的形成过程
(8)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式
您最近一年使用:0次
2016-12-09更新
|
1047次组卷
|
3卷引用:宁夏青铜峡市高级中学2017-2018学年高一下学期期中考试化学试题
宁夏青铜峡市高级中学2017-2018学年高一下学期期中考试化学试题(已下线)2012-2013学年广东省东莞市第七高级中学高一下学期期中考试化学试卷河北省石家庄市元氏县第四中学2019-2020学年高一下学期期中考试化学试题
9-10高一下·宁夏吴忠·期末
6 . 海洋面积占地球总面积的71% 。海洋中含有丰富的资源,海水中的钠盐、镁盐等都是重要的化工原料,从海水中提取铀、重水对一个国家来说具有战略意义。
(1)写出镁元素在周期表中的位置:_______________________
(2)氯化钠的电子式__________ ,用电子式表示水的形成过程__________________________
(3)写出重水中的氢元素的核素符号:________
(1)写出镁元素在周期表中的位置:
(2)氯化钠的电子式
(3)写出重水中的氢元素的核素符号:
您最近一年使用:0次



