名校
解题方法
1 . 下图为元素周期表的一部分,根据元素①~⑧在表中的位置回答下列问题。
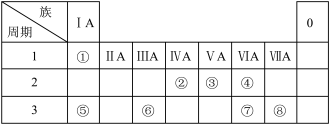
(1)元素⑧的最高价氧化物对应水化物的分子式为_______ ;
(2)元素①与④形成的18电子的化合物的结构式为_______ ;
(3)用电子式表示元素⑤与⑧形成化合物的过程_______ ;
(4)元素⑥的单质与⑤的最高价氧化物对应水化物反应的化学方程式_______ ;
(5)假设元素⑧的对应元素符号为X,若在一定条件下,X单质能够与硫反应生成一种用途广泛的硫化剂S2X2。该硫化剂S2X2与足量水反应有淡黄色沉淀生成,同时生成能够使品红溶液褪色的无色气体,则该反应的化学方程式是_______ (元素X请用具体元素符号表示)。

(1)元素⑧的最高价氧化物对应水化物的分子式为
(2)元素①与④形成的18电子的化合物的结构式为
(3)用电子式表示元素⑤与⑧形成化合物的过程
(4)元素⑥的单质与⑤的最高价氧化物对应水化物反应的化学方程式
(5)假设元素⑧的对应元素符号为X,若在一定条件下,X单质能够与硫反应生成一种用途广泛的硫化剂S2X2。该硫化剂S2X2与足量水反应有淡黄色沉淀生成,同时生成能够使品红溶液褪色的无色气体,则该反应的化学方程式是
您最近一年使用:0次
2021-03-16更新
|
685次组卷
|
6卷引用:甘肃省民勤县第一中学2020-2021学年高一下学期 第一次月考化学(理)试题
名校
2 . 下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
(1)11种元素中,化学性质最不活泼的是__________ ,原子半径最小的是_________ 。
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是___________ 。
(3)②③④中形成的简单离子半径由大到小的顺序是_________________ 。
(4)元素⑦的氢化物电子式为_______ ,该氢化物常温下和元素②的单质反应的离子方程式是________________ 。
(5)①和⑨的最高价氧化物对应的水化物化学式为__________ 和__________ 。①和⑨两元素形成化合物中化学键的类型为____________ ,该化合物灼烧时焰色为_________ ,该化合物的溶液与元素⑧的单质反应的离子方程式为__________________ 。
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(7)⑧⑨⑪三种元素形成的气态氢化物最稳定的是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)11种元素中,化学性质最不活泼的是
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是
(3)②③④中形成的简单离子半径由大到小的顺序是
(4)元素⑦的氢化物电子式为
(5)①和⑨的最高价氧化物对应的水化物化学式为
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为
(7)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
您最近一年使用:0次
2021-01-20更新
|
1811次组卷
|
6卷引用:甘肃省金昌市第一中学2020-2021学年高一下学期期中考试化学(理)试题
甘肃省金昌市第一中学2020-2021学年高一下学期期中考试化学(理)试题新疆哈密市第八中学2019-2020学年高一下学期期中考试化学试题(已下线)专题07 物质结构与元素周期律-备战2021届高考化学二轮复习题型专练河南省新蔡县第一高级中学2020-2021学年高一下学期5月月考化学试题(已下线)专题17 化学键(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练福建省政和县第二中学2022-2023学年高一下学期第一次月考化学试题
名校
解题方法
3 . 我们周围的物质世界是由100多种元素组成的,为了便于研究元素的性质,常常需要寻找它们之间的内在规律。表列出的是l~18号元素的部分最高正化合价和最低负化合价。请阅读并回答下列问题:
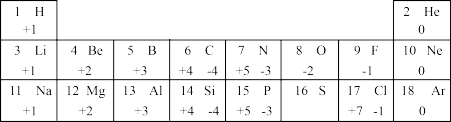
(1)1l号元素属于_________ 元素(填“金属”或“非金属”),它在化学反应中形成的离子与__________ (填元素符号)原子具有相同的核外电子排布。
(2)16号元素的原子核外电子数为____________ ,推测该元素最低负化合价为__________ ,最高正化合价的氧化物的化学式为_______________ 。
(3)从化合价角度,我们可以发现一些规律。请写出其中的—个:__________ 。
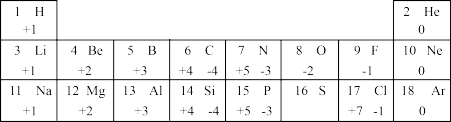
(1)1l号元素属于
(2)16号元素的原子核外电子数为
(3)从化合价角度,我们可以发现一些规律。请写出其中的—个:
您最近一年使用:0次
4 . 下表列出了①~⑨九种元素在周期表中的位置:请按要求回答下列问题:
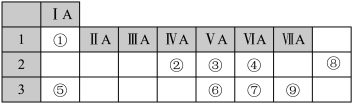
(1)元素④的名称是______ ,元素④在周期表中所处位置______ ,从元素原子得失电子的角度看,元素④形成的单质具有______ 性(填“氧化”或“还原”).
(2)元素⑦的原子结构示意图是______ .
(3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:______ (写氢化物的化学式).
(4)写出元素⑤形成的单质与水反应的化学方程式_________ .

(1)元素④的名称是
(2)元素⑦的原子结构示意图是
(3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:
(4)写出元素⑤形成的单质与水反应的化学方程式
您最近一年使用:0次
名校
5 . 下表列出了①~⑩10种元素在周期表中的位置。
(1)上述元素中,金属性最强的是(填元素符号,下同)________ ,③④⑤三种元素的原子半径由大到小的顺序是____________ 。
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是________ (填化学式)
(3)元素⑥的氢化物的电子式为____________ ,该氢化物与元素⑥的最高价氧化物对应的水化物反应的化学方程式为____________ 。
(4)比较⑥和⑦氢化物的稳定性由强到弱的顺序是____________ (填化学式)。
| 族 周期 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ⑩ | |||||
| 3 | ① | ③ | ④ | ⑦ | ⑧ | |||
| 4 | ② | ⑨ |
(1)上述元素中,金属性最强的是(填元素符号,下同)
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是
(3)元素⑥的氢化物的电子式为
(4)比较⑥和⑦氢化物的稳定性由强到弱的顺序是
您最近一年使用:0次
名校
解题方法
6 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
(1)在③~⑦元素中,原子半径最大的是__________ (填元素符号);
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有__________________ ;
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:_________ 。
(4)③、⑤、⑦、⑧所形成的离子,其半径由小到大的顺序是________ (填离子符号)
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_____________ (填物质化学式);呈两性的氢氧化物是_________ (填物质化学式),该化合物与NaOH溶液反应的离子方程式为___________ 。
(6)用电子式表示元素③与⑨形成化合物的过程_____________________________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(1)在③~⑦元素中,原子半径最大的是
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:
(4)③、⑤、⑦、⑧所形成的离子,其半径由小到大的顺序是
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
(6)用电子式表示元素③与⑨形成化合物的过程
您最近一年使用:0次
2020-04-13更新
|
1066次组卷
|
6卷引用:甘肃省兰州市第五十五中学2020-2021学年高一下学期3月月考化学试题
名校
7 . (1)现有下列10种物质:①O2;②H2;③NH4NO3;④Na2O2;⑤Ba(OH)2;⑥CH4;⑦CO2;⑧NaF;⑨NH3;⑩I2。其中既含离子键又含非极性键的是________ (填序号,下同);既含离子键又含极性键的是________ ;。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子。若XY2为常见元素形成的离子化合物,则其电子式为______________________________________________ ;若XY2为共价化合物,则其结构式为_________________________________________ 。
(3)氯化铝的物理性质非常特殊,如氯化铝的熔点为190℃,但在180℃就开始升华。据此判断,氯化铝是______________ (填“共价化合物”或“离子化合物”),可以证明该判断正确的实验依据是_______________________________________ 。
(4)现有a~g七种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:
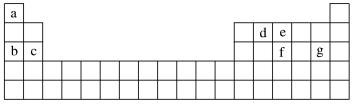
元素的原子间最容易形成离子键的是____ (填字母,下同),容易形成共价键的是____ 。
A.c和f B.b和g C.d和g D.b和e
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子。若XY2为常见元素形成的离子化合物,则其电子式为
(3)氯化铝的物理性质非常特殊,如氯化铝的熔点为190℃,但在180℃就开始升华。据此判断,氯化铝是
(4)现有a~g七种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:

元素的原子间最容易形成离子键的是
A.c和f B.b和g C.d和g D.b和e
您最近一年使用:0次
8 . 下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,在这些元素中,化学性质最不活泼的是_____________ (填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物是_________ ,碱性最强的化合物是_________ 。
(3)最高价氧化物是两性氧化物的元素是_________ 。
(4)元素④与⑥形成的化合物属于_____________ (填“共价”或“离子”)化合物。
(5)①与⑦形成的化合物的化学式__________________ 。
(6)写出⑥的原子结构示意图_____________ 。
| 主族 周期 | I A | IIA | IIIA | IVA | V A | VIA | VIIA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(1)在这些元素中,在这些元素中,化学性质最不活泼的是
(2)在最高价氧化物的水化物中,酸性最强的化合物是
(3)最高价氧化物是两性氧化物的元素是
(4)元素④与⑥形成的化合物属于
(5)①与⑦形成的化合物的化学式
(6)写出⑥的原子结构示意图
您最近一年使用:0次
2019-05-29更新
|
125次组卷
|
3卷引用:甘肃省庆阳市第六中学2021-2022学年高二上学期第一次月考化学(文)试题
甘肃省庆阳市第六中学2021-2022学年高二上学期第一次月考化学(文)试题【市级联考】山东省威海市2018-2019学年高一下学期期中考试化学试题(已下线)2019年6月8日 《每日一题》 必修2 周末培优
9 . 下表是元素周期表的一部分,回答下列问题:
(1)写出①、⑥两种元素的名称:_______ 、_______ 。
(2)这些元素的最高价氧化物对应水化物中,酸性最强的是_____ (填化学式,下同);能形成两性氢氧化物的元素是_______ (填元素符号)。
| 族 周期 | ⅠA | 0 | ||||||
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(1)写出①、⑥两种元素的名称:
(2)这些元素的最高价氧化物对应水化物中,酸性最强的是
您最近一年使用:0次
10 . 下表为元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题。
(1)①~⑩中,最活泼的金属元素是________ (写元素符号,下同),最不活泼的元素是________ 。
(2)①⑧的简单离子,其半径更大的是________ (写离子符号)。
(3)⑧⑨的气态氢化物,更稳定的是____________ (填化学式)。
(4)元素的非金属性:⑥________ ⑦(填“>”或“<”)。
(5)①~⑨的最高价氧化物的水化物中:酸性最强的是____________ (填化学式);碱性最强的是__________ (填化学式),该碱与⑤的最高价氧化物的水化物反应的离子方程式为__________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑦ | ⑧ | ⑩ | |||||
| 3 | ① | ② | ⑤ | ⑥ | ⑨ | |||
| 4 | ② | ④ |
(2)①⑧的简单离子,其半径更大的是
(3)⑧⑨的气态氢化物,更稳定的是
(4)元素的非金属性:⑥
(5)①~⑨的最高价氧化物的水化物中:酸性最强的是
您最近一年使用:0次
2019-04-24更新
|
120次组卷
|
4卷引用:甘肃省武威市第五中学2018-2019学年高一下学期第一次月考化学试题
甘肃省武威市第五中学2018-2019学年高一下学期第一次月考化学试题福建省德化县第一中学、永安市第一中学、漳平市第一中学2017--2018学年高一年第一次联考(4月)化学试题(已下线)5.1.4 元素周期表的应用(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)湖南省邵阳市新邵县2021-2022学年高一上学期期末质量检测化学试题



