1 . 下面是元素周期表的草图,表中所列字母代号分别代表某一种元素,请回答:

(1)表中的实线表示元素周期表的左右边界,请用实线补全元素周期表的上下边界。________
(2)表中最活泼的金属与最活泼的非金属形成的物质是________ (填化学式)。
(3)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:_______ ,这两种化合物中所含的化学键有______ (填字母)。
A.极性共价键 B.非极性共价键 C.离子键
(4) e、f、k、m对应的单原子离子的半径由大到小的顺序为____________ (填离子符号)。
(5) d、m对应的离子还原性由强到弱顺序为__________ (填离子符号)。
(6) d、e、m的气态氢化物中,最不稳定的是__________ (填分子式)。

(1)表中的实线表示元素周期表的左右边界,请用实线补全元素周期表的上下边界。
(2)表中最活泼的金属与最活泼的非金属形成的物质是
(3)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:
A.极性共价键 B.非极性共价键 C.离子键
(4) e、f、k、m对应的单原子离子的半径由大到小的顺序为
(5) d、m对应的离子还原性由强到弱顺序为
(6) d、e、m的气态氢化物中,最不稳定的是
您最近一年使用:0次
名校
2 . 下表列出了①~⑨九种元素在周期表中的位置:
请按要求 回答下列问题。
(1)元素③的名称是__ ,元素⑨的元素符号是____ ,元素④形成的单质具有____ (填“氧化性”或“还原性”)。
(2)元素⑦⑧⑨的气态氢化物的稳定性由弱到强的顺序:____ (用化学式表示)。
(3)写出一条能说明元素⑤的金属性比元素⑥强的事实:_____ 。
(4)写出元素⑤形成的单质与水反应的离子方程式:_____ 。
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素③的名称是
(2)元素⑦⑧⑨的气态氢化物的稳定性由弱到强的顺序:
(3)写出一条能说明元素⑤的金属性比元素⑥强的事实:
(4)写出元素⑤形成的单质与水反应的离子方程式:
您最近一年使用:0次
名校
3 . 在第三周期元素中,除稀有气体元素外:
(1)最高价氧化物对应水化物碱性最强的是___ ;
(2)氧化物中具有两性的是_____ ;
(3)最高价氧化物对应水化物酸性最强的是_____ (用化学式回答,下同);
(4)最不稳定的气态氢化物是____ ;
(5)原子半径最小的元素是___ (填元素符号);
(6)金属性最强的元素是____ (填元素符号) 。
(1)最高价氧化物对应水化物碱性最强的是
(2)氧化物中具有两性的是
(3)最高价氧化物对应水化物酸性最强的是
(4)最不稳定的气态氢化物是
(5)原子半径最小的元素是
(6)金属性最强的元素是
您最近一年使用:0次
名校
解题方法
4 . 下表是元素周期表的一部分,回答下列有关问题:
(1)①-⑪中,属于长周期的元素是______  填序号
填序号 。
。
(2)①-⑪中,最活泼的金属元素是______  填元素符号
填元素符号 ,在空气中燃烧的产物是
,在空气中燃烧的产物是______  写出电子式
写出电子式 。
。
(3)①-⑪中,最不活泼的元素其原子结构示意图为______ 。
(4)③④⑤三种元素对应的简单阳离子中,半径最大的离子结构示意图为______ 。
(5)在这些元素的最高价氧化物对应水化物中,呈两性的氢氧化物是______  写化学式
写化学式 。
。
(6)若将④⑤的单质用导线相连插入稀硫酸溶液中形成原电池,则该原电池的负极反应式______ 。
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ | ⑪ |
 填序号
填序号 。
。(2)①-⑪中,最活泼的金属元素是
 填元素符号
填元素符号 ,在空气中燃烧的产物是
,在空气中燃烧的产物是 写出电子式
写出电子式 。
。(3)①-⑪中,最不活泼的元素其原子结构示意图为
(4)③④⑤三种元素对应的简单阳离子中,半径最大的离子结构示意图为
(5)在这些元素的最高价氧化物对应水化物中,呈两性的氢氧化物是
 写化学式
写化学式 。
。(6)若将④⑤的单质用导线相连插入稀硫酸溶液中形成原电池,则该原电池的负极反应式
您最近一年使用:0次
名校
解题方法
5 . 下图为元素周期表的一部分,根据元素a~j在周期表中的位置,按要求回答下列问题。
(1)f、g、h的单质分别与水反应,最剧烈的是___________ (填元素符号)。
(2)c、i的氢化物稳定性较强的是____________ (填化学式)。
(3)c、f可形成既含离子键又含非极性键的化合物,该化合物的电子式为__________ 。
(4)d、f、g的离子半径最大的是_______________ (填离子符号)。
(5)f的最高价氧化物的水化物与h的最高价氧化物的水化物反应的离子方程式为:_______
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | a | |||||||
| 2 | b | c | d | e | ||||
| 3 | f | g | h | i | j | |||
(1)f、g、h的单质分别与水反应,最剧烈的是
(2)c、i的氢化物稳定性较强的是
(3)c、f可形成既含离子键又含非极性键的化合物,该化合物的电子式为
(4)d、f、g的离子半径最大的是
(5)f的最高价氧化物的水化物与h的最高价氧化物的水化物反应的离子方程式为:
您最近一年使用:0次
名校
6 . 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
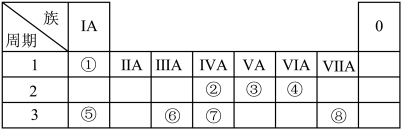
(1)②、④元素的原子按1∶2组成化合物的电子式:(用元素符号表示)_________________ 。
(2)⑤、⑧元素的化合物的用电子式表示形成过程:___________________________ 。
(3)①、⑤、⑥阳离子氧化性由弱到强的顺序是(用离子符号表示)_____________ 。
(4)①、④、⑤中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:________________ 。
(5)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________ 。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(6)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
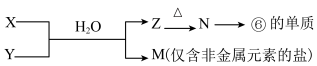
X溶液与Y溶液反应的离子方程式为___________________________________

(1)②、④元素的原子按1∶2组成化合物的电子式:(用元素符号表示)
(2)⑤、⑧元素的化合物的用电子式表示形成过程:
(3)①、⑤、⑥阳离子氧化性由弱到强的顺序是(用离子符号表示)
(4)①、④、⑤中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(5)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(6)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为
您最近一年使用:0次
2011·江西吉安·一模
7 . 纯净物A、B、C、D、E均是中学常见的物质。其转化关系如图所示(图中某些生成物已略去),物质A与物质B之间的反应不在溶液中进行,通常状况下D为气体

请回答下列问题:
(1)若A、B、D均为短周期元素的单质,C为化合物且气体D就是物质B,又知D气体不可燃,则B的分子式是_______ ,化合物E的化学式为________ 。
(2)若A、C、D均为短周期元素的单质,B、E为氧化物,且化合物E通常状况下为气体,在一定条件下E还可以和氧气发生反应。则A位于在周期表中的________ 周期______ 族。A和B反应生成C的化学方程式是______ 。

请回答下列问题:
(1)若A、B、D均为短周期元素的单质,C为化合物且气体D就是物质B,又知D气体不可燃,则B的分子式是
(2)若A、C、D均为短周期元素的单质,B、E为氧化物,且化合物E通常状况下为气体,在一定条件下E还可以和氧气发生反应。则A位于在周期表中的
您最近一年使用:0次
名校
8 . 铁及其化合物在生产和生活中有着广泛的应用。
(1)铁元素在元素周期表中的位置为_____ 。
(2)等物质的量的铁分别与足量的盐酸、水蒸气在一定条件下反应,产生相同条件下的气体体积比为_____ ,铁在高温条件下与水蒸气反应的化学方程式为______________ 。
(3)高铁酸钾(K2FeO4)也是常用的水处理剂。它的制备方法有多种:其中熔融法又称为过氧化钠氧化法。先在高温熔融的条件下制备高铁酸钠:Fe+3Na2O2 Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:
Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:_______________________________________ 。
(1)铁元素在元素周期表中的位置为
(2)等物质的量的铁分别与足量的盐酸、水蒸气在一定条件下反应,产生相同条件下的气体体积比为
(3)高铁酸钾(K2FeO4)也是常用的水处理剂。它的制备方法有多种:其中熔融法又称为过氧化钠氧化法。先在高温熔融的条件下制备高铁酸钠:Fe+3Na2O2
 Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:
Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4=K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:
您最近一年使用:0次
9 . 下表为元素周期表的一部分,请参照元素①﹣⑩在表中的位置,回答下列问题:
(1)自然界物质种类最多的元素在周期表中的位置是______
(2)⑧⑨⑩的离子半径由大到小的顺序为______ (填化学用语).
(3)写出由⑥、⑧、⑩元素形成的一种离子化合物的电子式______
(4)根据斜线性质相似规则,②的最高价氧化物对应的水化物与盐酸反应的离子方程式____________
(5)③的氧化物,氢氧化物有两性,写出③的单质与⑧的最高价氧化物的水化物反应的化学方程式______
(6)已知W+X=Y+Z,W、X、Y、Z分别是由①⑤⑥三种元素形成的四种十电子粒子,写出该反应的离子方程式______ .
| IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
| 3 | ⑧ | ⑨ | ⑩ |
(1)自然界物质种类最多的元素在周期表中的位置是
(2)⑧⑨⑩的离子半径由大到小的顺序为
(3)写出由⑥、⑧、⑩元素形成的一种离子化合物的电子式
(4)根据斜线性质相似规则,②的最高价氧化物对应的水化物与盐酸反应的离子方程式
(5)③的氧化物,氢氧化物有两性,写出③的单质与⑧的最高价氧化物的水化物反应的化学方程式
(6)已知W+X=Y+Z,W、X、Y、Z分别是由①⑤⑥三种元素形成的四种十电子粒子,写出该反应的离子方程式
您最近一年使用:0次
10 . 下表列出了①~⑩十种元素在周期表中的位置:
请按要求回答下列问题。
(1)元素⑧对应的简单离子的结构示意图是____________ 。
(2)以上元素中,化学性质最不活泼的是____________ (填元素符号)。
(3)写出元素⑤形成的单质在空气中燃烧的化学方程式______________________ ,这一反应是____________ (填“吸热”或“放热”)反应。
(4)用电子式表示④与⑤形成的A2B型化合物的形成过程___________________________ 。
(5)在这些元素的最高价氧化物对应水化物 中,酸性最强的化合物的分子式是:__________ ,与元素⑥的最高价氧化物对应水化物 发生反应时的离子方程式为________________
(6)③的简单氢化物与③的最高价氧化物对应的水化物反应的生成物中含有的的化学键有____________________________ 。
| ⅠA | ||||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
请按要求回答下列问题。
(1)元素⑧对应的简单离子的结构示意图是
(2)以上元素中,化学性质最不活泼的是
(3)写出元素⑤形成的单质在空气中燃烧的化学方程式
(4)用电子式表示④与⑤形成的A2B型化合物的形成过程
(5)在这些元素的最高价氧化物对应
(6)③的简单氢化物与③的最高价氧化物对应的水化物反应的生成物中含有的的化学键有
您最近一年使用:0次



