解题方法
1 . 香花石是1958年中国地质学家发现的第一种世界新矿物,其主要成分的化学式为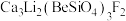 ,回答下列问题:
,回答下列问题:
(1)质子数与中子数相等的 原子的符号
原子的符号______ , 的结构示意图为
的结构示意图为______ 。
(2) 位于元素周期表第
位于元素周期表第______ 周期______ 族。
(3)香花石的主要成分的组成元素中,原子半径最小的是______ (填元素符号,下同),最大的是______ 。
(4) 的电子式为
的电子式为______ 。
(5)用电子式表示 (过氧化钙)的形成过程:
(过氧化钙)的形成过程:______ 。
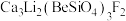 ,回答下列问题:
,回答下列问题:(1)质子数与中子数相等的
 原子的符号
原子的符号 的结构示意图为
的结构示意图为(2)
 位于元素周期表第
位于元素周期表第(3)香花石的主要成分的组成元素中,原子半径最小的是
(4)
 的电子式为
的电子式为(5)用电子式表示
 (过氧化钙)的形成过程:
(过氧化钙)的形成过程:
您最近一年使用:0次
解题方法
2 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)非金属性最强的元素是____ (填元素符号,下同),考古时利用____ 测定一些文物的年代。
(2)第三周期元素除⑩外原子半径最小的是____ (填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是____ (填氧化物的化学式,下同)、具有两性的是____ 。
(3)由⑨和⑥两种元素组成的化合物的电子式是____ ;
(4)②和③两种元素的气态氢化物更稳定的是____ (填“②”或“③”)。
| IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)非金属性最强的元素是
(2)第三周期元素除⑩外原子半径最小的是
(3)由⑨和⑥两种元素组成的化合物的电子式是
(4)②和③两种元素的气态氢化物更稳定的是
您最近一年使用:0次
名校
解题方法
3 . 2019年是元素周期表诞生150周年,元素周期表(律)在学习、研究和生产实践中有很重要的作用。下表为元素周期表的一部分,回答下列问题。
(1)元素①~⑧中,金属性最强的是________ (填元素符号)。
(2)中国青年化学家姜雪峰被国际组织推选为“元素⑦代言人”,元素⑦的原子结构示意图是_________ ,其氢化物的电子式是_________ 。
(3)比较元素②、③的最高价氧化物对应水化物的酸性:______ >______ (填化学式)。说明你判断的理由:_________ 。
(4)主族元素砷(As)的部分信息如图所示。

①砷(As)在周期表中的位置是______ 。
②下列说法正确的是_______ (填序号)。
a.砷元素的最高化合价为+4
b.推测砷有多种氧化物
c.③的气态氢化物的还原性大于砷的气态氢化物的还原性
(5)某小组同学设计实验比较VIIA元素的非金属性:Cl>Br>I。已知:常温下浓盐酸与高锰酸钾反应生成氯气。
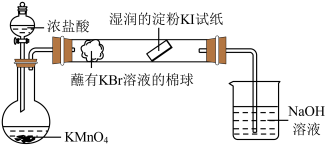
打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙红色,湿润的淀粉KI试纸变蓝,据此现象能否说明非金属性:Br >I,并说明理由_________ 。
| IA | 0 | |||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ||||||||
(2)中国青年化学家姜雪峰被国际组织推选为“元素⑦代言人”,元素⑦的原子结构示意图是
(3)比较元素②、③的最高价氧化物对应水化物的酸性:
(4)主族元素砷(As)的部分信息如图所示。

①砷(As)在周期表中的位置是
②下列说法正确的是
a.砷元素的最高化合价为+4
b.推测砷有多种氧化物
c.③的气态氢化物的还原性大于砷的气态氢化物的还原性
(5)某小组同学设计实验比较VIIA元素的非金属性:Cl>Br>I。已知:常温下浓盐酸与高锰酸钾反应生成氯气。

打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙红色,湿润的淀粉KI试纸变蓝,据此现象能否说明非金属性:Br >I,并说明理由
您最近一年使用:0次
4 . 下列编号代表元素周期表中的一部分元素,用化学式回答下列问题:
(1)①、③、⑤的最高价氧化物的水化物碱性由强到弱顺序为___________ (填化学式,下同)。
(2)②、③、④形成的简单阳离子半径由大到小的顺序是_______________ 。
(3)⑨和⑩的最高价氧化物对应的水化物化学式为_______ 和_________ 。①在氧气中点燃生成淡黄色的固体,该固体的电子式为_______________ ,①能够与水剧烈反应,请写出该反应的化学方程式_______________ ,将元素⑩的单质通入NaBr溶液中,反应的离子方程式为_______________ 。
(4)⑥、⑦、⑧三种元素形成的气态氢化物的稳定性排序是____________ (填化学式,下同),三种元素非金属性由强到弱的顺序为___________ 。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ⑦ | ⑧ | |||||
| 三 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 四 | ② | ④ |
(1)①、③、⑤的最高价氧化物的水化物碱性由强到弱顺序为
(2)②、③、④形成的简单阳离子半径由大到小的顺序是
(3)⑨和⑩的最高价氧化物对应的水化物化学式为
(4)⑥、⑦、⑧三种元素形成的气态氢化物的稳定性排序是
您最近一年使用:0次
5 . 下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
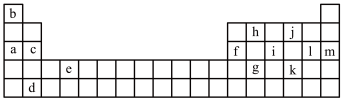
表中所列元素中:
属于短周期元素的有_____________________________________ (填字母,下同);属于主族元素的有__________________________________________ ;e元素在元素周期表中的位置是第__________ 周期第__________ 族。

表中所列元素中:
属于短周期元素的有
您最近一年使用:0次
名校
6 . 标号为①~⑩的元素,在元素周期表中的位置如下:
试回答下列问题:
(1)(填写元素符号)①_____ ③______ ⑤_____ ⑦_____
(2)①和④号元素形成的化合物的化学式为________ ,用电子式表示其形成过程为__________ 。
(3)⑦和⑧号元素的最高价氧化物的水化物的碱性是:______ ﹥_________ (填化学式)。⑨和⑩号元素的最高价氧化物的水化物的酸性是: ______ ﹥_________ (填化学式)。
(4)①、⑤、⑦号元素形成的一种化合物的电子式是________ ,在该化合物中既含有________ 键,又含有________ 键。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ||||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ |
试回答下列问题:
(1)(填写元素符号)①
(2)①和④号元素形成的化合物的化学式为
(3)⑦和⑧号元素的最高价氧化物的水化物的碱性是:
(4)①、⑤、⑦号元素形成的一种化合物的电子式是
您最近一年使用:0次
2019-08-09更新
|
584次组卷
|
4卷引用:贵州省毕节市实验高级中学2019-2020学年高一下学期期中考试化学试题
7 . 2019年是门捷列夫提出元素周期表150周年,根据元素周期表和周期律,回答问题。
Ⅰ.下表显示了元素周期表中短周期的一部分,①〜⑥代表6种短周期元素。其中②与氢元素形成的简单氢化物分子中含10个电子,能够使湿润的红色石蕊试纸变蓝。
(1)①在周期表中所处的位置为__________ 。
(2)与②同族的第四周期元素的原子结构示意图为__________ 。
(3)写出③与⑥的简单氢化物中沸点较高的分子的电子式__________ 。
(4)④的单质与水反应的离子方程式为__________ 。
(5)工业制取⑤的单质的化学方程式为__________ 。
Ⅱ.某同学欲利用下图装置验证同周期或同主族元素性质递变规律。
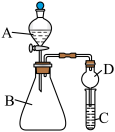
(6)干燥管D的作用是__________ 。
(7)证明非金属性:Cl>I。在A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液观察到C中溶液变蓝,则C试管中发生反应的离子方程式为__________ 。
(8)证明非金属性:N>C,在A中加稀硝酸,B中加碳酸钙,C中加澄清石灰水;观察到C中溶液__________ 的现象,该实验设计的原理是利用最高价氧化物对应水化物的酸性强弱来比较元素非金属性的强弱。
Ⅲ.到目前为止,元素周期表的第七周期已经被填满。
(9)请你设想一下,如果发现120号元素,下列有关它在周期表的位置或性质的说法错误的两项是__________ 。
①在第八周期ⅡA族;②最外层电子数是2;③比钙的熔点高;④与水反应放出氢气但比钙缓慢;⑤该元素单质需隔绝空气密封保存;⑥该元素的氧化物属于离子化合物
Ⅰ.下表显示了元素周期表中短周期的一部分,①〜⑥代表6种短周期元素。其中②与氢元素形成的简单氢化物分子中含10个电子,能够使湿润的红色石蕊试纸变蓝。
① | ② | ③ | ||||
④ | ⑤ | ⑥ |
(2)与②同族的第四周期元素的原子结构示意图为
(3)写出③与⑥的简单氢化物中沸点较高的分子的电子式
(4)④的单质与水反应的离子方程式为
(5)工业制取⑤的单质的化学方程式为
Ⅱ.某同学欲利用下图装置验证同周期或同主族元素性质递变规律。

(6)干燥管D的作用是
(7)证明非金属性:Cl>I。在A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液观察到C中溶液变蓝,则C试管中发生反应的离子方程式为
(8)证明非金属性:N>C,在A中加稀硝酸,B中加碳酸钙,C中加澄清石灰水;观察到C中溶液
Ⅲ.到目前为止,元素周期表的第七周期已经被填满。
(9)请你设想一下,如果发现120号元素,下列有关它在周期表的位置或性质的说法错误的两项是
①在第八周期ⅡA族;②最外层电子数是2;③比钙的熔点高;④与水反应放出氢气但比钙缓慢;⑤该元素单质需隔绝空气密封保存;⑥该元素的氧化物属于离子化合物
您最近一年使用:0次
2019-08-04更新
|
197次组卷
|
2卷引用:贵州省毕节市金沙县第一中学2020-2021学年高一下学期第一次月考化学试题
名校
8 . 元素周期表是学习化学的重要工具,它隐含着许多信息和规律。请根据下表中短周期元素的原子半径和主要化合价,回答表后问题。
(1)元素①在周期表中的位置为_____ 。
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为____ (填化学式)。
(3)元素①、③形成的18电子化合物的电子式为____ ,元素②、⑧的最高价氧化物对应的水化物中,碱性较强的是______ (填化学式)。
(4)元素②、⑤形成化合物的电子式为_____ 。
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑧的最高价氧化物对应水化物反应的离子方程式为______
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10 m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)元素①在周期表中的位置为
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为
(3)元素①、③形成的18电子化合物的电子式为
(4)元素②、⑤形成化合物的电子式为
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑧的最高价氧化物对应水化物反应的离子方程式为
您最近一年使用:0次
2019-04-15更新
|
212次组卷
|
2卷引用:【全国百强校】贵州省思南中学2018-2019学年高二下学期期中考试化学试题
名校
9 . 根据原子结构和元素周期律,回答:116号元素处于周期表第______ 周期,第______ 族;原子核外有_______ 个电子层,最外层有_______ 个电子;它是_________ (填金属或非金属)元素。
您最近一年使用:0次
名校
10 . 元素周期表有____ 个横行,叫周期,每一周期中元素原子的_________ 相同,从左到右元素的金属性____ (填增强或减弱);元素周期表中有_____ 列,第ⅥA族处在第_____ 列,同一主族从上到下,元素的非金属性依次_______ (填增强或减弱)。
您最近一年使用:0次



