2024·黑龙江吉林·模拟预测
解题方法
1 . 一种从废钼催化剂(主要成分为MoO3、MoS2,含少量CoO、CoS、NiO、Fe2O3等)中回收有价值金属的工艺流程如图。
②溶液中金属离子开始沉淀和完全沉淀的pH如表:
③钼酸铵[(NH4)2MoO4]为白色晶体,具有很高的水溶性,不溶于乙醇。
回答下列问题:
(1)催化剂中含多种金属元素,其中铁在元素周期表中的位置:第______ 周期第_____ 族。基态Co原子的价电子排布式为______ 。
(2)钼酸铵[(NH4)2MoO4]中Mo元素的化合价为______ ;“焙烧”时MoS2转化为MoO3,该反应的化学方程式为______ 。
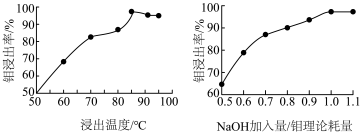
(3)“碱浸”时,浸出温度、NaOH加入量/钼理论耗量对钼浸出率的影响如图。______ 、NaOH加入量/钼理论耗量______ 。
(4)“除铁”时应调节溶液pH的范围为_______ 。
(5)若“沉钴镍”时调节溶液pH=9.5,则此时溶液中p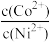 =
=______ (pX=-lgX)。
(6)经过降温结晶、过滤、洗涤、干燥等操作得到(NH4)2MoO4•7H2O晶体,洗涤时所选用的最佳试剂为______ 。

②溶液中金属离子开始沉淀和完全沉淀的pH如表:
| 金属离子 | Fe3+ | Co2+ | Ni2+ |
| 开始沉淀时的pH | 2.2 | 6.4 | 7.2 |
| 沉淀完全时(c=1.0×10-5mol•L-1)的pH | 3.2 | 9.0 | 8.7 |
回答下列问题:
(1)催化剂中含多种金属元素,其中铁在元素周期表中的位置:第
(2)钼酸铵[(NH4)2MoO4]中Mo元素的化合价为
(3)“碱浸”时,浸出温度、NaOH加入量/钼理论耗量对钼浸出率的影响如图。
(4)“除铁”时应调节溶液pH的范围为
(5)若“沉钴镍”时调节溶液pH=9.5,则此时溶液中p
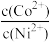 =
=(6)经过降温结晶、过滤、洗涤、干燥等操作得到(NH4)2MoO4•7H2O晶体,洗涤时所选用的最佳试剂为
您最近一年使用:0次
2 . 磷化硼是一种超硬耐磨涂层材料,结构与金刚石相似,其晶胞结构如图所示。请回答下列问题:___________ ,基态磷原子中电子的运动状态有___________ 种,与硼同主族的第四周期元素的基态原子价层电子的轨道表示式为___________ 。
(2) 为一元弱酸,
为一元弱酸, 分子中
分子中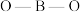 的键角
的键角___________ (填“ ”“
”“ ”或“
”或“ ”)
”) (中的
(中的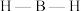 的键角,原因为
的键角,原因为___________ 。
(3)磷化硼晶体属于___________ 晶体,其中硼原子的配位数为___________ 。
(4)磷化硼的化学式为___________ ,该晶体的密度为___________  (用含a、
(用含a、 的代数式表示,阿伏加德罗常数的值为
的代数式表示,阿伏加德罗常数的值为 )。
)。

(2)
 为一元弱酸,
为一元弱酸, 分子中
分子中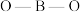 的键角
的键角 ”“
”“ ”或“
”或“ ”)
”) (中的
(中的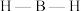 的键角,原因为
的键角,原因为(3)磷化硼晶体属于
(4)磷化硼的化学式为
 (用含a、
(用含a、 的代数式表示,阿伏加德罗常数的值为
的代数式表示,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解题方法
3 . 铬酸铅俗称铬黄,主要用于油漆、油墨、塑料以及橡胶等行业。一种以含铬废水(含 、
、 、
、 )和草酸泥渣(含
)和草酸泥渣(含 、
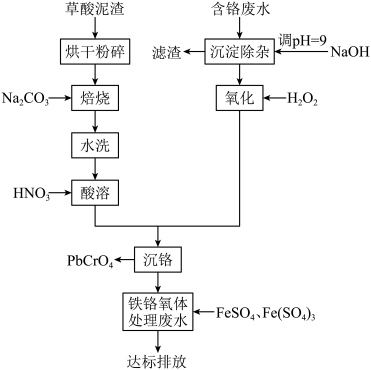
、 )为原料制备铬酸铅的流程如图所示,已知:
)为原料制备铬酸铅的流程如图所示,已知:
___________ ,基态铬原子价电子排布式为___________ 。
(2)草酸泥渣“粉碎”的目的是___________ ,“焙烧”时加入 是为了将
是为了将 转化为
转化为 ,同时放出
,同时放出 ,该转化过程的化学方程式为
,该转化过程的化学方程式为___________ 。
(3)滤渣的主要成分为 、
、___________ (填化学式)。
(4)“氧化”步骤加入过氧化氢溶液发生反应的离子方程式为___________ 。
(5)为了提高沉铬率,用平衡移动原理解释“酸溶”过程中所加硝酸不能过量的原因是___________ 。
(6)处理含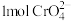 的废水时,
的废水时, 被还原成
被还原成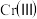 ,若投入
,若投入 ,使金属阳离子恰好完全形成铁铬氧体
,使金属阳离子恰好完全形成铁铬氧体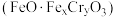 沉淀,理论上还需要
沉淀,理论上还需要 的物质的量为
的物质的量为___________  。
。
 、
、 、
、 )和草酸泥渣(含
)和草酸泥渣(含 、
、 )为原料制备铬酸铅的流程如图所示,已知:
)为原料制备铬酸铅的流程如图所示,已知:
(2)草酸泥渣“粉碎”的目的是
 是为了将
是为了将 转化为
转化为 ,同时放出
,同时放出 ,该转化过程的化学方程式为
,该转化过程的化学方程式为(3)滤渣的主要成分为
 、
、(4)“氧化”步骤加入过氧化氢溶液发生反应的离子方程式为
(5)为了提高沉铬率,用平衡移动原理解释“酸溶”过程中所加硝酸不能过量的原因是
(6)处理含
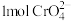 的废水时,
的废水时, 被还原成
被还原成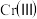 ,若投入
,若投入 ,使金属阳离子恰好完全形成铁铬氧体
,使金属阳离子恰好完全形成铁铬氧体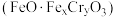 沉淀,理论上还需要
沉淀,理论上还需要 的物质的量为
的物质的量为 。
。
您最近一年使用:0次
解题方法
4 . 钪( )及其化合物在电子、超导合金和催化剂等领域有重要应用。一种利用钛白废酸液(含
)及其化合物在电子、超导合金和催化剂等领域有重要应用。一种利用钛白废酸液(含 、
、 、
、 的硫酸废液)和赤泥(含有
的硫酸废液)和赤泥(含有 、
、 、
、 、
、 )联合制备
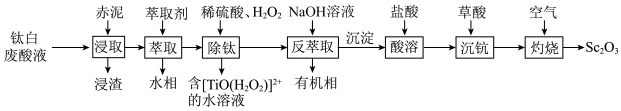
)联合制备 的工艺流程如图所示。回答下列问题:
的工艺流程如图所示。回答下列问题:
已知:25℃时,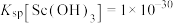 。
。
(1)基态 的简化电子排布式为
的简化电子排布式为___________ 。
(2)为提高“浸取”速率,可采取的措施有___________ (写出一条即可),“浸渣”的主要成分是___________ (写化学式);水相中含有的金属离子主要是___________ (写离子符号)。
(3)“除钛”时,加入 的作用是
的作用是___________ 。
(4)25℃时,若使“反萃取”后水溶液中的 沉淀完全(离子浓度
沉淀完全(离子浓度 ),应控制溶液的
),应控制溶液的 不低于
不低于___________ (保留两位有效数字)。
(5)写出草酸钪晶体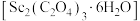 “灼烧”时发生反应的化学方程式:
“灼烧”时发生反应的化学方程式:___________ 。
 )及其化合物在电子、超导合金和催化剂等领域有重要应用。一种利用钛白废酸液(含
)及其化合物在电子、超导合金和催化剂等领域有重要应用。一种利用钛白废酸液(含 、
、 、
、 的硫酸废液)和赤泥(含有
的硫酸废液)和赤泥(含有 、
、 、
、 、
、 )联合制备
)联合制备 的工艺流程如图所示。回答下列问题:
的工艺流程如图所示。回答下列问题:
已知:25℃时,
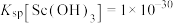 。
。(1)基态
 的简化电子排布式为
的简化电子排布式为(2)为提高“浸取”速率,可采取的措施有
(3)“除钛”时,加入
 的作用是
的作用是(4)25℃时,若使“反萃取”后水溶液中的
 沉淀完全(离子浓度
沉淀完全(离子浓度 ),应控制溶液的
),应控制溶液的 不低于
不低于(5)写出草酸钪晶体
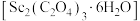 “灼烧”时发生反应的化学方程式:
“灼烧”时发生反应的化学方程式:
您最近一年使用:0次
名校
解题方法
5 . 硒(Se)是一种有抗癌、抗氧化作用的元素,可形成多种化合物。某化合物是潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

A.Se的基态原子价电子排布式为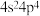 |
| B.该化合物的晶体类型是离子晶体 |
C.该化合物的化学式为 |
D.距离K最近的 八面体有4个 八面体有4个 |
您最近一年使用:0次
2023-11-06更新
|
791次组卷
|
8卷引用:吉林省通化市梅河口市第五中学2023-2024学年高三上学期1月期末化学试题
6 . 回答下列问题
(1)已知Se与O同族,基态Se原子价层电子的运动状态有___________ 种,基态O原子的电子排布式不能表示为1s22s22p 2p
2p ,因为这违背了
,因为这违背了___________ (填选项)。
A.能量最低原理 B.泡利不相容原理 C.洪特规则
(2)请写出O原子的价层电子轨道表示式:___________ ,基态Be、B、O三种元素的原子第一电离能由大到小的顺序为___________ ,KF、KCl、KBr三种晶体中熔点最高的是___________ 。
(3)BeO晶体是制备氟硼铍酸钾晶体的原料之一,其晶胞结构与ZnS类似,如图所示。Be原子的配位数是___________ ;该晶胞中原子的位置可以用原子分数坐标表示,若原子A、B的坐标分别为(0,0,0)、 ( ,
, ,1);则C原子坐标为
,1);则C原子坐标为___________ 。设晶胞参数为a pm,用NA表示阿伏加德罗常数的值,则BeO晶体的密度为___________ g·cm-3(用含a和NA的式子表示)。

(1)已知Se与O同族,基态Se原子价层电子的运动状态有
 2p
2p ,因为这违背了
,因为这违背了A.能量最低原理 B.泡利不相容原理 C.洪特规则
(2)请写出O原子的价层电子轨道表示式:
(3)BeO晶体是制备氟硼铍酸钾晶体的原料之一,其晶胞结构与ZnS类似,如图所示。Be原子的配位数是
 ,
, ,1);则C原子坐标为
,1);则C原子坐标为
您最近一年使用:0次
名校
解题方法
7 . 碳族元素中的Sn和氧族元素中的Te的有机化合物受到广泛关注。文献报道了利用有八面体结构的有机碲酸A与三甲基氯化锡B合成了一种具有抗癌活性的含碲和锡有机化合物C,反应前后Te和Sn的杂化方式不变。请回答下列问题:

(1)Te原子的最高能层理论上所具有的轨道数为_____ 。
(2)气态TeO3分子的立体构型为_____ ;共价化合物B中Sn的杂化方式为_____ 。化合物A中Te与下列化合物中S的杂化方式相同的是_____ (填序号)。
①H2S ②SO2③SO3④SF6
(3)用一个溴原子和一个氯原子取代有机碲酸A中与Te相连的两个羟基,结构仍为八面体,取代后的有机碲酸可能有_____ 种。
(4)有机化合物C核磁共振氢谱显示等效氢的个数比为_____ 。
(5)化合物B可以用SnI4合成,α-SnI4为立方晶体,其晶胞沿面对角线的投影如图所示:
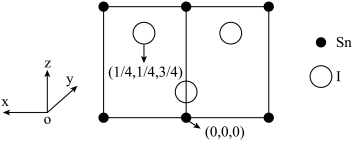
①晶胞中Sn和I之间的最近距离为apm,α-SnI4的密度的计算式为_____ g/cm3(设阿伏加德罗常数为NA);晶胞中由碘原子所围成的空隙中心坐标为_____ 。
②常温常压下SiF4为气态而SiCl4为液态,原因____ ,SnF4和SnCl4都为离子晶体,而SnF4为固体,SiCl4为液体,这是由于F到Cl的变化使得与Sn的卤化物中化学键的离子性____ 、共价性____ 。(填“增强”“不变”或“减弱”)

(1)Te原子的最高能层理论上所具有的轨道数为
(2)气态TeO3分子的立体构型为
①H2S ②SO2③SO3④SF6
(3)用一个溴原子和一个氯原子取代有机碲酸A中与Te相连的两个羟基,结构仍为八面体,取代后的有机碲酸可能有
(4)有机化合物C核磁共振氢谱显示等效氢的个数比为
(5)化合物B可以用SnI4合成,α-SnI4为立方晶体,其晶胞沿面对角线的投影如图所示:

①晶胞中Sn和I之间的最近距离为apm,α-SnI4的密度的计算式为
②常温常压下SiF4为气态而SiCl4为液态,原因
您最近一年使用:0次
名校
解题方法
8 . 铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域。回答下列问题:
(1)铜原子基态价电子排布式为_______ ;
(2) 和
和 都是离子晶体,两种晶体熔点较低的是
都是离子晶体,两种晶体熔点较低的是_______ ,原因是_______ ;
(3)铜镍合金的立方晶胞结构如下图所示:

①原子B的分数坐标为_______ ;
②若该晶体密度为 ,以
,以 表示阿伏加德罗常数,则铜镍原子间最短距离为
表示阿伏加德罗常数,则铜镍原子间最短距离为_______ cm。
(1)铜原子基态价电子排布式为
(2)
 和
和 都是离子晶体,两种晶体熔点较低的是
都是离子晶体,两种晶体熔点较低的是(3)铜镍合金的立方晶胞结构如下图所示:

①原子B的分数坐标为
②若该晶体密度为
 ,以
,以 表示阿伏加德罗常数,则铜镍原子间最短距离为
表示阿伏加德罗常数,则铜镍原子间最短距离为
您最近一年使用:0次
名校
9 . 某水性钠离子电池电极材料由Na+、Fe2+、Fe3+、CN-组成,其立方晶胞嵌入和嵌出Na+过程中,Fe2与Fe3+含量发生变化,依次变为格林绿、普鲁士蓝、普鲁士白三种物质,其过程如图所示。下列说法错误的是
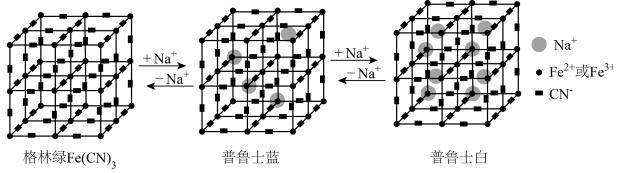

| A.基态Fe原子的价电子排布式为3d64s2,失去4s电子转化为Fe2+ |
| B.导电能力普鲁士蓝小于普鲁士白 |
| C.普鲁士蓝中Fe2+与Fe3+个数比为1:2 |
D.若普鲁士白的晶胞棱长为apm,则其晶体的密度为 |
您最近一年使用:0次
2023-01-13更新
|
698次组卷
|
2卷引用:吉林省通化市梅河口市第五中学2022-2023学年高二上学期期末考试化学试题
名校
10 . 下表是元素周期表一部分,表中每一个字母分别代表一种元素,请选择适当的元素回答下列问题。

(1)e、g、i、l的离子半径由大到小的顺序为_______ 。(用对应元素的离子符号表示);c、j、k的最高价含氧酸的酸性由强到弱的顺序是_______ 。(用化学式表示)
(2)b在空气中燃烧,除了生成_______ 外,也生成微量的_______ 。
(3)k的氧化物与l的单质溶于水反应生成两种强酸的化学反应方程式_______ 。
(4)g与d形成的gd3可用于汽车的安全气囊中,其中阴离子的空间结构为_______ ,g在空气中燃烧发出黄色火焰,这种黄色焰色用光谱仪摄取的光谱为_______ 光谱(填“发射”或“吸收”)。
(5)第三周期元素中,按第一电离能大小排序,第一电离能在i和l之间的元素_______ 种。
(6)气态o2+再失去一个电子比气态p2+再失去一个电子难,其原因是:_______ 。

(1)e、g、i、l的离子半径由大到小的顺序为
(2)b在空气中燃烧,除了生成
(3)k的氧化物与l的单质溶于水反应生成两种强酸的化学反应方程式
(4)g与d形成的gd3可用于汽车的安全气囊中,其中阴离子的空间结构为
(5)第三周期元素中,按第一电离能大小排序,第一电离能在i和l之间的元素
(6)气态o2+再失去一个电子比气态p2+再失去一个电子难,其原因是:
您最近一年使用:0次



