解题方法
1 . 第二周期非金属元素的单质及其化合物是生命活动的重要物质基础。请回答:
(1)下列说法正确的是_______。
(2)有机物转化及相应产率: ,所有有机物中碳原子的杂化方式为
,所有有机物中碳原子的杂化方式为_______ ,后者产物的产率低的原因是_______ 。
(3)当负电荷位于电负性大的原子时,结构较稳定。 结合
结合 ,通过电子转移可得到下列粒子,稳定性最弱的粒子是_______。
,通过电子转移可得到下列粒子,稳定性最弱的粒子是_______。
(4)某新型电池的正极材料由F、K、Ni三种元素组成,其晶胞如图所示:

①基态Ni的核外电子排布式为_______ 。
②K与F间的化学键的离子键百分率_______ Ni与F间的化学键(选填“大于”或“小于”)。
③该材料中,Ni元素的化合价为_______ 。
(1)下列说法正确的是_______。
A. 三种分子的键角逐渐减小 三种分子的键角逐渐减小 |
| B.第二周期非金属元素的最高正价逐渐升高 |
C. 最外层电子排布为 最外层电子排布为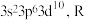 与硼元素同主族 与硼元素同主族 |
D.结合质子趋势: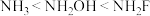 |
(2)有机物转化及相应产率:
 ,所有有机物中碳原子的杂化方式为
,所有有机物中碳原子的杂化方式为(3)当负电荷位于电负性大的原子时,结构较稳定。
 结合
结合 ,通过电子转移可得到下列粒子,稳定性最弱的粒子是_______。
,通过电子转移可得到下列粒子,稳定性最弱的粒子是_______。A. | B. | C. | D. |
(4)某新型电池的正极材料由F、K、Ni三种元素组成,其晶胞如图所示:

①基态Ni的核外电子排布式为
②K与F间的化学键的离子键百分率
③该材料中,Ni元素的化合价为
您最近一年使用:0次
名校
2 . 下列化学用语表示不正确 的是
A.铬的基态原子的电子排布式: |
B. 的VSEPR模型: 的VSEPR模型: |
C. 分子中 分子中 键的形成: 键的形成: |
D.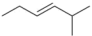 :2-甲基-3-己烯 :2-甲基-3-己烯 |
您最近一年使用:0次
3 . 硼族元素可形成许多结构和性质特殊的化合物。回答下列问题
(1)基态Ga原子的电子排布式为___________ 。
(2)常温下,F2与硼单质反应生成BF3,BF3为缺电子结构,通入水中产生三种酸分别为HBF4、HF和___________ (填化学式)。NF3和NF3BF3中F-N-F的键角大小是NF3___________ NF3BF3(填“>”、“<”或“=”)。
(3)一定条件下,NH4F、NaF和NaAlO2反应生成NH3、H2O和化合物X。X晶胞及晶胞中某一原子的俯视投影如图所示。___________ 。
②X晶体内含有的作用力有___________ (填字母)。
a.配位键 b.离子键 c.氢键 d.金属键
(4)解释H2N-NH2,HO-OH,H3C-CH3中,N-N,O-O,C-C的键能O-O<N-N<C-C___________ 。
(1)基态Ga原子的电子排布式为
(2)常温下,F2与硼单质反应生成BF3,BF3为缺电子结构,通入水中产生三种酸分别为HBF4、HF和
(3)一定条件下,NH4F、NaF和NaAlO2反应生成NH3、H2O和化合物X。X晶胞及晶胞中某一原子的俯视投影如图所示。
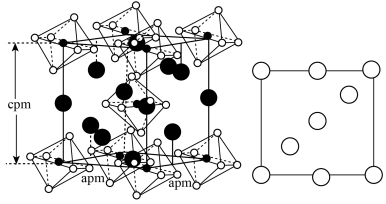
②X晶体内含有的作用力有
a.配位键 b.离子键 c.氢键 d.金属键
(4)解释H2N-NH2,HO-OH,H3C-CH3中,N-N,O-O,C-C的键能O-O<N-N<C-C
您最近一年使用:0次
解题方法
4 . 铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
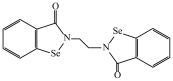
①已知Se与S在同一主族,基态Se原子的核外电子排布式为[Ar]_______ 。
②比较键角的大小:气态 分子
分子_______  离子(填“>”、“<”或“=”),原因是
离子(填“>”、“<”或“=”),原因是_______ 。
(2)富马酸亚铁(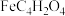 )是一种补铁剂。富马酸分子的结构模型如图所示:
)是一种补铁剂。富马酸分子的结构模型如图所示:
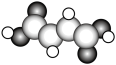
下列相关说法正确的是_______。
(3)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:

①该超导材料的最简化学式为_______ 。
②Fe原子的配位数为_______ 。
③该晶胞参数a=b=0.4nm,c=1.4nm。阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为_______  (列出计算式)。
(列出计算式)。
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

①已知Se与S在同一主族,基态Se原子的核外电子排布式为[Ar]
②比较键角的大小:气态
 分子
分子 离子(填“>”、“<”或“=”),原因是
离子(填“>”、“<”或“=”),原因是(2)富马酸亚铁(
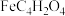 )是一种补铁剂。富马酸分子的结构模型如图所示:
)是一种补铁剂。富马酸分子的结构模型如图所示:
下列相关说法正确的是_______。
| A.富马酸分子中σ键和π键的数目比是10:3 |
B.富马酸分子中C的杂化方式有 、 、 |
| C.富马酸分子可以形成分子内氢键,使得富马酸一级和二级电离常数变大 |
| D.富马酸亚铁中各元素的电负性由大到小的顺序为O>C>H>Fe |
(3)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:

①该超导材料的最简化学式为
②Fe原子的配位数为
③该晶胞参数a=b=0.4nm,c=1.4nm。阿伏加德罗常数的值为
 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
5 . 氮元素可形成多种结构和性质特殊的化合物。回答下列问题:
(1)As和氮同主族,基态As原子的核外电子排布式为______ 。
(2)聚吡咯作柔性电极材料,其单体为吡咯(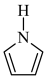 )。吡咯、呋喃(
)。吡咯、呋喃(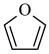 )、噻吩(
)、噻吩(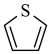 )都是杂环化合物,沸点:吡咯>噻吩>呋喃,原因是
)都是杂环化合物,沸点:吡咯>噻吩>呋喃,原因是______ 。
(3)我国科学家用激光将置于铁室中石墨靶上的碳原子炸松,再用射频电火花喷射氮气,获得超硬新材料 -氮化碳薄膜,结构如图。下列有关
-氮化碳薄膜,结构如图。下列有关 -氮化碳的说法错误的是______。
-氮化碳的说法错误的是______。
(4)一定条件下, 和
和 反应生成碳单质和化合物X。已知X属于六方晶系,晶胞结构如右图所示,其中碳的化合价为+4价。X的化学式为
反应生成碳单质和化合物X。已知X属于六方晶系,晶胞结构如右图所示,其中碳的化合价为+4价。X的化学式为______ 。 的配位数为
的配位数为______ 。若阿伏加德罗常数的值为 ,该晶体的摩尔体积
,该晶体的摩尔体积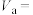
______  (列出算式)。
(列出算式)。
(1)As和氮同主族,基态As原子的核外电子排布式为
(2)聚吡咯作柔性电极材料,其单体为吡咯(
 )。吡咯、呋喃(
)。吡咯、呋喃( )、噻吩(
)、噻吩( )都是杂环化合物,沸点:吡咯>噻吩>呋喃,原因是
)都是杂环化合物,沸点:吡咯>噻吩>呋喃,原因是(3)我国科学家用激光将置于铁室中石墨靶上的碳原子炸松,再用射频电火花喷射氮气,获得超硬新材料
 -氮化碳薄膜,结构如图。下列有关
-氮化碳薄膜,结构如图。下列有关 -氮化碳的说法错误的是______。
-氮化碳的说法错误的是______。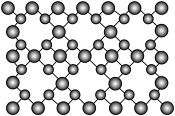
A.与石墨相比, -氮化碳导电性增强 -氮化碳导电性增强 |
B.与金刚石相比, -氮化碳的熔点更高 -氮化碳的熔点更高 |
C. -氮化碳中C、N的杂化方式相同 -氮化碳中C、N的杂化方式相同 |
D. -氮化碳中C原子数与C-N键之比为1∶2 -氮化碳中C原子数与C-N键之比为1∶2 |
(4)一定条件下,
 和
和 反应生成碳单质和化合物X。已知X属于六方晶系,晶胞结构如右图所示,其中碳的化合价为+4价。X的化学式为
反应生成碳单质和化合物X。已知X属于六方晶系,晶胞结构如右图所示,其中碳的化合价为+4价。X的化学式为 的配位数为
的配位数为 ,该晶体的摩尔体积
,该晶体的摩尔体积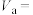
 (列出算式)。
(列出算式)。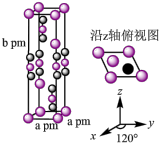
您最近一年使用:0次
解题方法
6 . 磷酸铁锂电池是以磷酸铁锂(LiFePO4)为正极材料的锂离子电池,具有循环寿命长、安全性能好、无环境污染等特点。
(1)磷酸铁锂具有橄榄石结构,空间骨架结构不易发生形变,化学性质稳定。
①基态 的价层电子排布式为
的价层电子排布式为_______ 。
②Li、P、O三种元素的电负性由大到小的顺序是_______ 。
(2)硫酸亚铁(FeSO4)可用于制备磷酸铁锂。
①根据价层电子对互斥理论可知, 的空间结构为
的空间结构为_______ 。
②比较S原子和O原子的第一电离能大小,并从原子结构的角度说明理由:_______ 。
(3)草酸亚铁(FeC2O4)也可用于制备磷酸铁锂。草酸根离子的结构简式为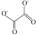 ,其中碳原子的杂化轨道类型为
,其中碳原子的杂化轨道类型为_______ 。
(4)磷酸铁(FePO4)与磷酸铁锂结构相似,其中 围绕
围绕 和
和 分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,
分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,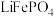 中的
中的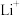 会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
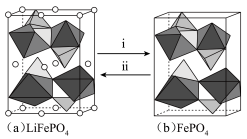
①i表示_______ (填“充电”或“放电”)过程。
②已知Li+的脱嵌率= 。某时刻,若正极材料中Li+的脱嵌率为
。某时刻,若正极材料中Li+的脱嵌率为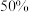 ,则其中
,则其中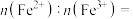
_______ 。
(1)磷酸铁锂具有橄榄石结构,空间骨架结构不易发生形变,化学性质稳定。
①基态
 的价层电子排布式为
的价层电子排布式为②Li、P、O三种元素的电负性由大到小的顺序是
(2)硫酸亚铁(FeSO4)可用于制备磷酸铁锂。
①根据价层电子对互斥理论可知,
 的空间结构为
的空间结构为②比较S原子和O原子的第一电离能大小,并从原子结构的角度说明理由:
(3)草酸亚铁(FeC2O4)也可用于制备磷酸铁锂。草酸根离子的结构简式为
 ,其中碳原子的杂化轨道类型为
,其中碳原子的杂化轨道类型为(4)磷酸铁(FePO4)与磷酸铁锂结构相似,其中
 围绕
围绕 和
和 分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,
分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,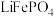 中的
中的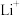 会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
①i表示
②已知Li+的脱嵌率=
 。某时刻,若正极材料中Li+的脱嵌率为
。某时刻,若正极材料中Li+的脱嵌率为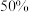 ,则其中
,则其中
您最近一年使用:0次
7 . 锰的化合物种类繁多,应用广泛。请回答.
(1)基态Mn原子的简化电子排布式是__________ 。
(2)锰的一种配合物可用于催化单键迁移重排,结构如图所示。该配合物中,第二周期非金属元素第一电离能由大到小顺序为__________ ,该配合物中Mn的配位数是__________ 。 、
、 等。酸性:
等。酸性:
______  (填“>”或“<”),理由是
(填“>”或“<”),理由是__________ 。
(4)某晶体化学式为 ,如图为其晶胞结构(
,如图为其晶胞结构( 未标出),Mn(Ⅱ)位于
未标出),Mn(Ⅱ)位于 围成的八面体空隙中,形成无限螺旋链的配离子,同一条链内原子作用很强,其形成晶胞结构图沿x、y晶轴方向投影如图a所示,晶胞沿z晶轴方向投影如图b所示,晶胞参数为a nm、a nm和b nm,则该晶胞中
围成的八面体空隙中,形成无限螺旋链的配离子,同一条链内原子作用很强,其形成晶胞结构图沿x、y晶轴方向投影如图a所示,晶胞沿z晶轴方向投影如图b所示,晶胞参数为a nm、a nm和b nm,则该晶胞中 个数
个数__________ ,阿伏加德罗常数的值为 ,该晶体的密度为
,该晶体的密度为__________  (用含
(用含 、a、b的式子表示)。
、a、b的式子表示)。
(1)基态Mn原子的简化电子排布式是
(2)锰的一种配合物可用于催化单键迁移重排,结构如图所示。该配合物中,第二周期非金属元素第一电离能由大到小顺序为

 、
、 等。酸性:
等。酸性:
 (填“>”或“<”),理由是
(填“>”或“<”),理由是(4)某晶体化学式为
 ,如图为其晶胞结构(
,如图为其晶胞结构( 未标出),Mn(Ⅱ)位于
未标出),Mn(Ⅱ)位于 围成的八面体空隙中,形成无限螺旋链的配离子,同一条链内原子作用很强,其形成晶胞结构图沿x、y晶轴方向投影如图a所示,晶胞沿z晶轴方向投影如图b所示,晶胞参数为a nm、a nm和b nm,则该晶胞中
围成的八面体空隙中,形成无限螺旋链的配离子,同一条链内原子作用很强,其形成晶胞结构图沿x、y晶轴方向投影如图a所示,晶胞沿z晶轴方向投影如图b所示,晶胞参数为a nm、a nm和b nm,则该晶胞中 个数
个数 ,该晶体的密度为
,该晶体的密度为 (用含
(用含 、a、b的式子表示)。
、a、b的式子表示)。
您最近一年使用:0次
名校
解题方法
8 . 铜及其化合物具有广泛的应用。请回答:
(1)Cu元素位于周期表___________ 区。
(2)下列说法不正确 的是___________。
(3)高温下固体中 比
比 稳定,常温下水溶液中
稳定,常温下水溶液中 离子比
离子比 离子稳定(水溶液中
离子稳定(水溶液中 易发生歧化反应生成
易发生歧化反应生成 ),原因是
),原因是___________ 。(已知:金属阳离子在水溶液中易与水分子发生络合形成水合离子,对应的热效应称为水合能, 的水合能为
的水合能为 ,
, 的水合能为
的水合能为 ,Cu的第二电离能为
,Cu的第二电离能为 。)
。)
(4) 可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶(
可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶( )、苯酚(
)、苯酚( )含有与苯类似的
)含有与苯类似的 、
、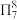 大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是
大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是___________ (填标号);1mol配合物中含配位键个数为___________ 。___________ 个。
②该晶胞中距离最近的Cu原子的核间距为apm,则该晶胞的密度为___________  (用含a、
(用含a、 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, )。
)。
(1)Cu元素位于周期表
(2)下列说法
| A.基态铜原子的核外电子有29种不同的空间运动状态 |
B.铜催化烯烃硝化反应时会产生 , , 的键角比 的键角比 大 大 |
C. 中非金属元素电负性: 中非金属元素电负性: |
D.配位键的强度: 大于 大于 |
(3)高温下固体中
 比
比 稳定,常温下水溶液中
稳定,常温下水溶液中 离子比
离子比 离子稳定(水溶液中
离子稳定(水溶液中 易发生歧化反应生成
易发生歧化反应生成 ),原因是
),原因是 的水合能为
的水合能为 ,
, 的水合能为
的水合能为 ,Cu的第二电离能为
,Cu的第二电离能为 。)
。)(4)
 可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶(
可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。已知:吡啶( )、苯酚(
)、苯酚( )含有与苯类似的
)含有与苯类似的 、
、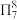 大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是
大π键,所有原子共平面。有机多齿配体中p轨道能提供一对电子的原子是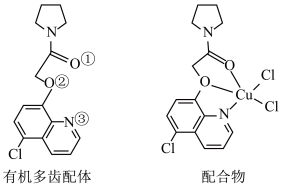
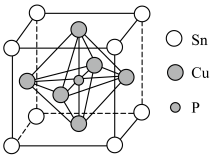
②该晶胞中距离最近的Cu原子的核间距为apm,则该晶胞的密度为
 (用含a、
(用含a、 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, )。
)。
您最近一年使用:0次
2023-11-26更新
|
337次组卷
|
4卷引用:浙江省9+1高中联盟2023-2024学年高三上学期期中考试化学试题
浙江省9+1高中联盟2023-2024学年高三上学期期中考试化学试题 (已下线)专题04 物质结构与性质(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)(已下线)压轴题10 物质结构与性质综合题(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)江西省上饶市婺源县天佑中学2023-2024学年高三上学期期中考试化学试卷
9 . 氟及其化合物种类繁多,应用广泛。请回答:
(1)基态F原子的价层电子排布式是_______ 。
(2)下列说法不正确的是_______。
(3)OF2分子的空间构型为_______ ;其分子极性_______ H2O(填“>”或“<”)。
(4)氟化氢是弱酸,在水溶液中存在 ;但
;但 ,当HF浓度大于5mol
,当HF浓度大于5mol L-1时,氢氟酸是一种相当强的酸,请解释原因:
L-1时,氢氟酸是一种相当强的酸,请解释原因:_______ 。
(5)某含氟化合物晶胞如图,其化学式为_______ ,设NA为阿伏加德罗常数的值,则该晶体的密度为_______ g/cm3
(1)基态F原子的价层电子排布式是
(2)下列说法不正确的是_______。
| A.第三电离能大小:F>O>N>C |
| B.冰晶石(Na3AlF6)中含有极性共价键、配位键、离子键 |
| C.SO2F2的结构类似H2SO4,SO2F2中的键角∠OSO<∠FSF |
| D.熔点大小:AlF3>AlBr3>AlCl3,推测AlF3为离子化合物 |
(3)OF2分子的空间构型为
(4)氟化氢是弱酸,在水溶液中存在
 ;但
;但 ,当HF浓度大于5mol
,当HF浓度大于5mol L-1时,氢氟酸是一种相当强的酸,请解释原因:
L-1时,氢氟酸是一种相当强的酸,请解释原因:(5)某含氟化合物晶胞如图,其化学式为

您最近一年使用:0次
10 . 自然界原生铜硫化合物经氧化、淋滤后变成 CuSO4溶液,遇到闪锌矿(ZnS)可慢慢转变为铜蓝(CuS)。已知: 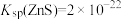 ,
,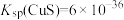 。下列说法正确的是
。下列说法正确的是
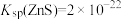 ,
,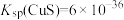 。下列说法正确的是
。下列说法正确的是| A.基态 Cu 核外电子排布式为[Ar]3d94s2 |
B.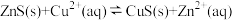 正向进行,需满足 正向进行,需满足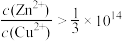 |
C.CuSO4溶液遇 ZnS 后生成 CuS 后的溶液中存在: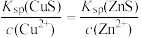 |
| D.将 CuS 固体加入无色饱和硫酸锌溶液(约 3 mol/L)中,溶液会变蓝色 |
您最近一年使用:0次



