解题方法
1 . 我国化学家研究发现,十八胺在较高温度下具有一定的还原性,由于不同的金属盐从十八胺中获得电子的能力不同,在十八胺体系中反应可以得到不同的产物:当以两种非贵金属盐为原料时得到混合金属氧化物(如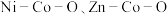 等),以
等),以 和一种非贵金属盐为原料时得到金属与金属氧化物异质结构(如
和一种非贵金属盐为原料时得到金属与金属氧化物异质结构(如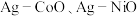 等),除
等),除 之外的其他贵金属盐和一种非贵金属盐为原料时得到合金或金属间化合物(如
之外的其他贵金属盐和一种非贵金属盐为原料时得到合金或金属间化合物(如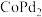 等)。
等)。
回答下列问题:
(1)十八胺中含有氮元素,含氮元素的三种离子 的键角由大到小的顺序是
的键角由大到小的顺序是___________ 。
(2) 与
与 相比,第二电离能与第一电离能差值更大的是
相比,第二电离能与第一电离能差值更大的是___________ 。
(3)以 和钴盐为原料时得到的产物
和钴盐为原料时得到的产物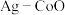 而非
而非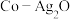 的原因是
的原因是___________ 。
(4)推测 盐和一种非贵金属盐混合后在十八胺体系中发生反应所得产物类别为
盐和一种非贵金属盐混合后在十八胺体系中发生反应所得产物类别为___________ 。
(5)一种含钴的离子结构如图所示: 的价电子轨道表示式是
的价电子轨道表示式是___________ 。已知磁矩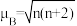 (n表示未成对电子数),则
(n表示未成对电子数),则 的磁矩
的磁矩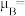
___________ 。
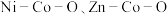 等),以
等),以 和一种非贵金属盐为原料时得到金属与金属氧化物异质结构(如
和一种非贵金属盐为原料时得到金属与金属氧化物异质结构(如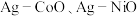 等),除
等),除 之外的其他贵金属盐和一种非贵金属盐为原料时得到合金或金属间化合物(如
之外的其他贵金属盐和一种非贵金属盐为原料时得到合金或金属间化合物(如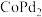 等)。
等)。
| 元素 |  |  |  |  |  |  |  |
| 电负性(鲍林标度) | 1.6 | 1.8 | 1.8 | 1.9 | 2.2 | 2.2 | 2.4 |
(1)十八胺中含有氮元素,含氮元素的三种离子
 的键角由大到小的顺序是
的键角由大到小的顺序是(2)
 与
与 相比,第二电离能与第一电离能差值更大的是
相比,第二电离能与第一电离能差值更大的是(3)以
 和钴盐为原料时得到的产物
和钴盐为原料时得到的产物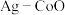 而非
而非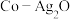 的原因是
的原因是(4)推测
 盐和一种非贵金属盐混合后在十八胺体系中发生反应所得产物类别为
盐和一种非贵金属盐混合后在十八胺体系中发生反应所得产物类别为(5)一种含钴的离子结构如图所示:
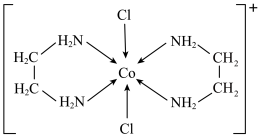
 的价电子轨道表示式是
的价电子轨道表示式是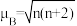 (n表示未成对电子数),则
(n表示未成对电子数),则 的磁矩
的磁矩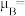
您最近一年使用:0次
2 . A、B、C、D、E、F均为36号以前的元素,原子序数依次增大。A的最外层电子数与次外层电子数相等。B元素的价层电子排布是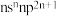 ,C元素
,C元素 价离子与B的离子电子层结构相同,D元素基态原子的最高能级有一个未成对电子且电子云为哑铃形,E元素基态的
价离子与B的离子电子层结构相同,D元素基态原子的最高能级有一个未成对电子且电子云为哑铃形,E元素基态的 价离子的
价离子的 轨道为半充满,F元素基态原子的最外层只有一个电子。回答下列问题:
轨道为半充满,F元素基态原子的最外层只有一个电子。回答下列问题:
(1)C的元素符号是______ 。上述六种元素中,位于周期表d区、 区的分别是
区的分别是___________ 、______ (填元素符号)。
(2)基态D原子的电子排布式是______ ,A、B、D电负性由大到小的顺序是______ (填元素符号)。
(3)向含 价F离子的水溶液中滴加氨水至过量,产生的现象是
价F离子的水溶液中滴加氨水至过量,产生的现象是___________ ,发生反应的离子方程式为___________ 、___________ 。
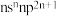 ,C元素
,C元素 价离子与B的离子电子层结构相同,D元素基态原子的最高能级有一个未成对电子且电子云为哑铃形,E元素基态的
价离子与B的离子电子层结构相同,D元素基态原子的最高能级有一个未成对电子且电子云为哑铃形,E元素基态的 价离子的
价离子的 轨道为半充满,F元素基态原子的最外层只有一个电子。回答下列问题:
轨道为半充满,F元素基态原子的最外层只有一个电子。回答下列问题:(1)C的元素符号是
 区的分别是
区的分别是(2)基态D原子的电子排布式是
(3)向含
 价F离子的水溶液中滴加氨水至过量,产生的现象是
价F离子的水溶液中滴加氨水至过量,产生的现象是
您最近一年使用:0次
解题方法
3 . 2022年诺贝尔化学奖颁给了在“点击化学”领域做出贡献的科学家。一种“点击化学”试剂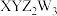 是由四种短周期主族元素组成,其中X、Z、W的原子序数依次递减,三者基态原子核外电子的空间运动状态数相同,Y的原子序数是Z的两倍。下列说法错误的是
是由四种短周期主族元素组成,其中X、Z、W的原子序数依次递减,三者基态原子核外电子的空间运动状态数相同,Y的原子序数是Z的两倍。下列说法错误的是
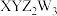 是由四种短周期主族元素组成,其中X、Z、W的原子序数依次递减,三者基态原子核外电子的空间运动状态数相同,Y的原子序数是Z的两倍。下列说法错误的是
是由四种短周期主族元素组成,其中X、Z、W的原子序数依次递减,三者基态原子核外电子的空间运动状态数相同,Y的原子序数是Z的两倍。下列说法错误的是A.简单气态氢化物的稳定性为 |
B.电负性和第一电离能均有 |
| C.同周期元素形成的简单氢化物中X的还原性最弱 |
| D.同周期主族元素基态原子未成对电子数少于Y的有3种 |
您最近一年使用:0次
4 . 铬元素是哺乳类代谢过程中必须的微量元素,目前六氟代乙酰丙酮铬(Ⅲ)螯合物(其结构如图)的检出极限已达到 。回答下列问题:
。回答下列问题:
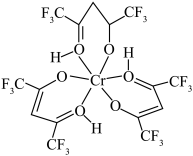
(1)基态铬原子的价电子排布式为___________ ,H、C、O、F的电负性由大到小的顺序为___________ 。
(2)与 具有相同未成对电子数的同周期基态原子的元素有
具有相同未成对电子数的同周期基态原子的元素有___________ 种,其中原子序数最大的元素在周期表中的位置是___________ 。
(3)六氟代乙酰丙酮铬(Ⅲ)螯合物中含有的化学键有___________ 。
a.极性共价键 b.非极性共价键 c.离子键 d.配位键
(4)六氟代乙酰丙酮(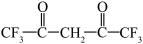 )中
)中 键有
键有___________ 个。
(5)分子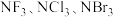 中键角由小到大的顺序是
中键角由小到大的顺序是___________ ,其原因是___________ 。
 。回答下列问题:
。回答下列问题:
(1)基态铬原子的价电子排布式为
(2)与
 具有相同未成对电子数的同周期基态原子的元素有
具有相同未成对电子数的同周期基态原子的元素有(3)六氟代乙酰丙酮铬(Ⅲ)螯合物中含有的化学键有
a.极性共价键 b.非极性共价键 c.离子键 d.配位键
(4)六氟代乙酰丙酮(
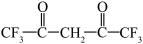 )中
)中 键有
键有(5)分子
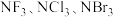 中键角由小到大的顺序是
中键角由小到大的顺序是
您最近一年使用:0次
解题方法
5 . 第四周期中的18种元素具有重要的用途。
(1)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价电子排布式为_______ 。
(2)第四周期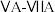 族的元素中,电负性由大到小的顺序为(用元素符号表示)
族的元素中,电负性由大到小的顺序为(用元素符号表示)_______ 。
(3)已知四溴化锗是电子工业中的一种常用试剂,其熔点为26.1℃,沸点为186℃,则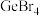 晶体类型为
晶体类型为_______ ,中心原子的杂化类型为_______ 。
(4) 的结构如图所示。
的结构如图所示。
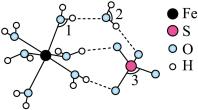
 中
中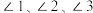 由大到小的顺序是
由大到小的顺序是_______ 。(用“1”“2”“3”表示)
(5)普鲁士蓝晶体属立方晶系,晶胞棱长为 。铁氰骨架组成晶胞中的8个小立方体,
。铁氰骨架组成晶胞中的8个小立方体, 粒子在小立方体顶点,
粒子在小立方体顶点, 在小立方体的棱上,两端均与
在小立方体的棱上,两端均与 相连,小立方体中心空隙可容纳
相连,小立方体中心空隙可容纳 ,如图所示(
,如图所示( 在图中省略)
在图中省略)
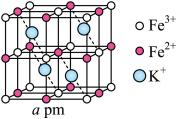
①普鲁士蓝中 与
与 个数之比为
个数之比为_______ ;
②若所有铁粒子为等径小球,则 与
与 之间最近距离为
之间最近距离为_______  。
。
(1)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价电子排布式为
(2)第四周期
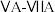 族的元素中,电负性由大到小的顺序为(用元素符号表示)
族的元素中,电负性由大到小的顺序为(用元素符号表示)(3)已知四溴化锗是电子工业中的一种常用试剂,其熔点为26.1℃,沸点为186℃,则
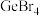 晶体类型为
晶体类型为(4)
 的结构如图所示。
的结构如图所示。
 中
中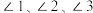 由大到小的顺序是
由大到小的顺序是(5)普鲁士蓝晶体属立方晶系,晶胞棱长为
 。铁氰骨架组成晶胞中的8个小立方体,
。铁氰骨架组成晶胞中的8个小立方体, 粒子在小立方体顶点,
粒子在小立方体顶点, 在小立方体的棱上,两端均与
在小立方体的棱上,两端均与 相连,小立方体中心空隙可容纳
相连,小立方体中心空隙可容纳 ,如图所示(
,如图所示( 在图中省略)
在图中省略)
①普鲁士蓝中
 与
与 个数之比为
个数之比为②若所有铁粒子为等径小球,则
 与
与 之间最近距离为
之间最近距离为 。
。
您最近一年使用:0次
6 . 某种锂盐结构如图所示,X、Y、Z、W为原子序数依次增大的短周期主族元素,基态W原子的s和p能级电子数之比为2∶3,下列说法正确的是
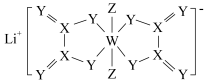

| A.简单离子半径:W> Z> Y |
| B.电负性:X> Y> Z |
| C.X与Y或Z元素均可构成非极性分子 |
| D.氢键的作用使得氢化物的稳定性:Z> W |
您最近一年使用:0次
名校
解题方法
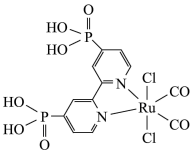
7 . 近年来,光催化剂的研究是材料领域的热点。一种 配合物(如图所示)复合光催化剂可将
配合物(如图所示)复合光催化剂可将 转化为
转化为 。下列说法错误的是
。下列说法错误的是
 配合物(如图所示)复合光催化剂可将
配合物(如图所示)复合光催化剂可将 转化为
转化为 。下列说法错误的是
。下列说法错误的是
A.基态 原子的核外电子的空间运动状态有5种 原子的核外电子的空间运动状态有5种 |
B. 中 中 键与 键与 键个数比为 键个数比为 |
C.该配合物中的配位原子的配位能力 |
D.P可以与氯气反应生成 和 和 两种非极性分子 两种非极性分子 |
您最近一年使用:0次
2023-07-12更新
|
90次组卷
|
2卷引用:山东省济宁市2022-2023学年高二下学期期末考试化学试题
解题方法
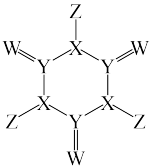
8 . 以尿素 为原料制得的某化合物的结构如图所示,下列说法错误的是
为原料制得的某化合物的结构如图所示,下列说法错误的是
 为原料制得的某化合物的结构如图所示,下列说法错误的是
为原料制得的某化合物的结构如图所示,下列说法错误的是
A.电负性: |
B. 与 与 形成的分子都是极性分子 形成的分子都是极性分子 |
C.原子半径: |
D.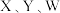 元素的简单气态氢化物中,沸点最高的是 元素的简单气态氢化物中,沸点最高的是 的气态氢化物 的气态氢化物 |
您最近一年使用:0次
9 . 下列有关化合物结构与性质的论述错误的是
A.F的电负性大于Cl,因此 酸性强于 酸性强于 |
B.键能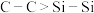 、 、 ,因此 ,因此 稳定性大于 稳定性大于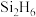 |
C. 的结构与苯相似,每个B、N各提供1个电子形成大 的结构与苯相似,每个B、N各提供1个电子形成大 键 键 |
| D.Si—C键的键长大于C—C键的键长,因此SiC的熔点和硬度低于金刚石 |
您最近一年使用:0次
10 . 有机物种类繁多,应用广泛。
(1)邻氨基吡啶(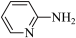 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为_______ (填元素符号)。 能溶于水的原因是
能溶于水的原因是_______ 。
(2)鸟嘌呤和吡咯的结构如下图所示。
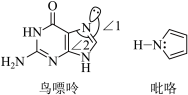
①鸟嘌呤中N原子的杂化方式为_______ ,夹角∠1_______ ∠2(填“>”或“<”)。
②分子中的大 键可以用符号
键可以用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数,吡咯中的大
键的电子数,吡咯中的大 键可表示为
键可表示为_______ 。
(3)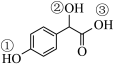 分子中3个-OH的电离能力由强到弱的顺序是
分子中3个-OH的电离能力由强到弱的顺序是_______ (用①、②、③表示)。
(4)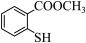 与
与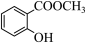 相比,前者的水溶性更
相比,前者的水溶性更_______ (填“大”或“小”)。—SH与—OH性质相似,写出与NaOH溶液反应的化学方程式_______ 。
(1)邻氨基吡啶(
 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为 能溶于水的原因是
能溶于水的原因是(2)鸟嘌呤和吡咯的结构如下图所示。

①鸟嘌呤中N原子的杂化方式为
②分子中的大
 键可以用符号
键可以用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数,吡咯中的大
键的电子数,吡咯中的大 键可表示为
键可表示为(3)
 分子中3个-OH的电离能力由强到弱的顺序是
分子中3个-OH的电离能力由强到弱的顺序是(4)
 与
与 相比,前者的水溶性更
相比,前者的水溶性更
您最近一年使用:0次
2023-07-11更新
|
352次组卷
|
2卷引用:山东省泰安市2022-2023学年高二下学期期末考试化学试题



