1 . 氢叠氮酸( )属于叠氮化物,是一种弱酸,其酸性类似于醋酸,能微弱电离出
)属于叠氮化物,是一种弱酸,其酸性类似于醋酸,能微弱电离出 和
和 。分子结构示意图如图所示。回答下列问题:
。分子结构示意图如图所示。回答下列问题:
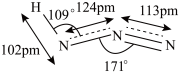
(1)下列有关说法正确的是_____(填字母符号)。
(2)叠氮酸根可作为一种配体,在 中钴显
中钴显_____ 价,基态钴原子的价电子排布式为_____ 。 空间形状为
空间形状为_______ 。
(3) 与
与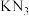 结构类似,前者晶格能比后者
结构类似,前者晶格能比后者_____ (填“大”或“小”), 中氮原子的第一电离能比氧原子
中氮原子的第一电离能比氧原子______ (填“大”或“小”)。
(4)与 互为等电子体的分子有
互为等电子体的分子有______ (写出两种即可)。
(5)人造立方氮化硼是超硬材料,其晶胞如图所示。

①晶体中硼原子的配位数为____ 。
②设该晶体的摩尔质量为 ,晶体的密度为
,晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶体中的距离最近的硼原子之间的距离为
,则晶体中的距离最近的硼原子之间的距离为______ cm。
 )属于叠氮化物,是一种弱酸,其酸性类似于醋酸,能微弱电离出
)属于叠氮化物,是一种弱酸,其酸性类似于醋酸,能微弱电离出 和
和 。分子结构示意图如图所示。回答下列问题:
。分子结构示意图如图所示。回答下列问题:
(1)下列有关说法正确的是_____(填字母符号)。
A. 中含有5个 中含有5个 键 键 | B. 中三个氮原子采用的都是 中三个氮原子采用的都是 杂化 杂化 |
C. 、 、 都是极性分子 都是极性分子 | D. 、 、 、 、 分子间都可以形成氢键 分子间都可以形成氢键 |
(2)叠氮酸根可作为一种配体,在
 中钴显
中钴显 空间形状为
空间形状为(3)
 与
与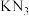 结构类似,前者晶格能比后者
结构类似,前者晶格能比后者 中氮原子的第一电离能比氧原子
中氮原子的第一电离能比氧原子(4)与
 互为等电子体的分子有
互为等电子体的分子有(5)人造立方氮化硼是超硬材料,其晶胞如图所示。

①晶体中硼原子的配位数为
②设该晶体的摩尔质量为
 ,晶体的密度为
,晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶体中的距离最近的硼原子之间的距离为
,则晶体中的距离最近的硼原子之间的距离为
您最近一年使用:0次
名校
解题方法
2 . 氢、碳、氮、氧元素的单质及化合物在很多领域有着广泛的应用。回答下列问题:
(1)画出基态N原子的轨道表示式___________ 。
(2)下列分子中,① ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ ,⑥
,⑥ ,⑦
,⑦ 既有
既有 键又有
键又有 键的是
键的是___________ (填序号,下同);以极性键结合,具有直线形结构的非极性分子是___________ ; 分子中N原子的杂化轨道类型是
分子中N原子的杂化轨道类型是___________ 。
(3) (二氟氮烯)分子中的氮原子采用
(二氟氮烯)分子中的氮原子采用 杂化,则
杂化,则 的结构式为
的结构式为_________ 。
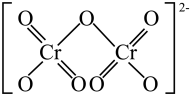
(4)重铬酸铵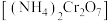 常用作有机合成催化剂,
常用作有机合成催化剂, 的结构如图。
的结构如图。 中
中 键数目为
键数目为___________  。
。
(5)利用皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管可以合成T-碳,T-碳的晶体结构可看成金刚石晶体中每个碳原子被正四面体结构单元(由四个碳原子组成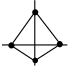 )替代,图a、b分别为T-碳的晶胞和俯视图,图c为金刚石晶胞。
)替代,图a、b分别为T-碳的晶胞和俯视图,图c为金刚石晶胞。
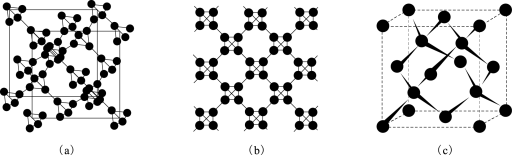
一个T-碳晶胞中含有___________ 个碳原子,T-碳的密度为金刚石的一半,则T-碳晶胞和金刚石晶胞的棱长之比为___________ 。
(1)画出基态N原子的轨道表示式
(2)下列分子中,①
 ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ ,⑥
,⑥ ,⑦
,⑦ 既有
既有 键又有
键又有 键的是
键的是 分子中N原子的杂化轨道类型是
分子中N原子的杂化轨道类型是(3)
 (二氟氮烯)分子中的氮原子采用
(二氟氮烯)分子中的氮原子采用 杂化,则
杂化,则 的结构式为
的结构式为(4)重铬酸铵
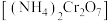 常用作有机合成催化剂,
常用作有机合成催化剂, 的结构如图。
的结构如图。 中
中 键数目为
键数目为 。
。
(5)利用皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管可以合成T-碳,T-碳的晶体结构可看成金刚石晶体中每个碳原子被正四面体结构单元(由四个碳原子组成
 )替代,图a、b分别为T-碳的晶胞和俯视图,图c为金刚石晶胞。
)替代,图a、b分别为T-碳的晶胞和俯视图,图c为金刚石晶胞。
一个T-碳晶胞中含有
您最近一年使用:0次
名校
解题方法
3 . 葡酚酮是由葡萄籽提取的一种花青素类衍生物(结构简式如图)具有良好的抗氧化活性。下列关于葡酚酮叙述错误的是


| A.基态氧原子的电子有5种空间运动状态 |
| B.分子中含有两种杂化轨道类型的碳原子 |
| C.分子中含有2个手性碳原子 |
| D.该分子可形成分子间氢键 |
您最近一年使用:0次
2023-08-29更新
|
247次组卷
|
2卷引用:重庆市长寿中学校2022-2023学年高二下学期4月期中考试化学试题
名校
4 .  是阿伏伽德罗常数的值,下列说法正确的是
是阿伏伽德罗常数的值,下列说法正确的是
 是阿伏伽德罗常数的值,下列说法正确的是
是阿伏伽德罗常数的值,下列说法正确的是A. 白磷 白磷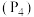 含有 含有 个P—P键 个P—P键 |
B.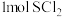 分子中,S原子的价层电子对数目为 分子中,S原子的价层电子对数目为 |
C. 乙酸含 乙酸含 键数目为 键数目为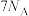 |
D. 晶体Si中的Si—Si键数目为 晶体Si中的Si—Si键数目为 |
您最近一年使用:0次
名校
解题方法
5 . 二氟化氧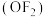 的键角为
的键角为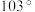 ,是一种无色的剧毒气体,能发生反应:
,是一种无色的剧毒气体,能发生反应: ,下列有关说法正确的是。
,下列有关说法正确的是。
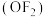 的键角为
的键角为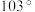 ,是一种无色的剧毒气体,能发生反应:
,是一种无色的剧毒气体,能发生反应: ,下列有关说法正确的是。
,下列有关说法正确的是。A. 难溶于 难溶于 | B. 的键角大于 的键角大于 |
C. 分子中O与F之间存在的是氢键 分子中O与F之间存在的是氢键 | D. 的VSEPR模型名称为正四面体形 的VSEPR模型名称为正四面体形 |
您最近一年使用:0次
名校
解题方法
6 . 金属在史前就为人们所知,金属单质及其化合物的使用推动了人类文明的发展。回答下列问题:
(1)基态As原子价电子排布图为_______ ,电子占据最高能级的电子云轮廓图形状为_______ 。
(2)AsH3的空间构型为_______ 。
(3)绿矾(FeSO4⋅7H2O)结构如下图。
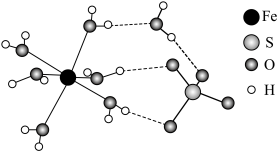
①H2O分别与Fe2+、SO 的相互作用分别为
的相互作用分别为_______ 、_______ 。
②比较SO 中的∠O—S—O
中的∠O—S—O_______ H2O中的∠H—O—H。(填“<”“>”或“=”)
(4)现在国家大力推行新能源,其中锂电池得到了巨大的发展。为了增强钴酸锂电池的安全性,科学家根据铁与钴性质的相似性,又研发出了磷酸亚铁锂电池。
①Fe在元素周期表中的位置是_______ 。
②磷青铜晶体的晶胞结构如图所示。
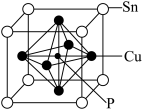
该晶体的化学式为_______ 。
(1)基态As原子价电子排布图为
(2)AsH3的空间构型为
(3)绿矾(FeSO4⋅7H2O)结构如下图。

①H2O分别与Fe2+、SO
 的相互作用分别为
的相互作用分别为②比较SO
 中的∠O—S—O
中的∠O—S—O(4)现在国家大力推行新能源,其中锂电池得到了巨大的发展。为了增强钴酸锂电池的安全性,科学家根据铁与钴性质的相似性,又研发出了磷酸亚铁锂电池。
①Fe在元素周期表中的位置是
②磷青铜晶体的晶胞结构如图所示。

该晶体的化学式为
您最近一年使用:0次
名校
7 . 离子液体是一种由离子构成的液体,在低温下也能以液态存在,是一种很有研究价值的溶剂。研究显示最常见的离子液体主要由如图所示正离子和负离子构成,图中正离子有令人惊奇的稳定性,它的电子在其环外结构中高度离域。下列说法错误的是


| A.图中负离子的空间结构为正四面体形 |
| B.该化合物中存在配位键和氢键 |
| C.离子液体可用作溶剂,且具有良好的导电性 |
| D.图中正离子中碳原子的杂化方式为sp2、sp3 |
您最近一年使用:0次
名校
解题方法
8 . 我国科学家最近开发了α- B26C@ TiO2/Ti催化剂实现NO制NH3,为资源回收利用提供新思路。请回答下列问题:
(1)基态N原子的价层电子排布图为_______ 。
(2)上述物质中所含第二周期元素的第一电离能由大到小的顺序为_______ (填元素符号,下同),电负性由大到小的顺序为_______ 。
(3)氨硼烷(NH3·BH3)是一种具有潜力的固体储氢材料。NH3·BH3分子中属于sp3杂化的原子有_______ (填元素符号)。H—N—H键角:NH3_______ NH3·BH3(填“>”“<”或“=”),理由是_______ 。
(4)已知:BC(碳化硼)、BN(氮化硼)的熔点依次为2450℃、3000℃, BN的熔点较高的主要原因是_______ 。
(5)已知TiO2的晶胞如图1所示,“黑球”代表_______ (填“钛”或“氧")。
(6)钛晶体有两种结构,如图2和图3所示。
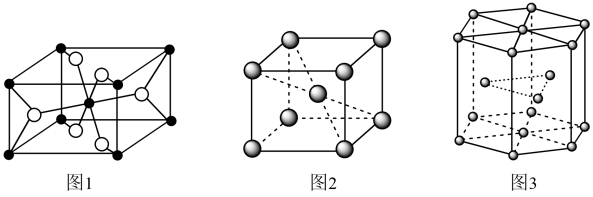
图2结构中空间利用率(φ)为_______ (用含π的代数式表示);已知图3结构中底边长为a nm,高为c nm,NA代表阿伏加德罗常数的值,则该钛晶体的密度为_______ g·cm-3(用含a、c、NA的代数式表示)。
(1)基态N原子的价层电子排布图为
(2)上述物质中所含第二周期元素的第一电离能由大到小的顺序为
(3)氨硼烷(NH3·BH3)是一种具有潜力的固体储氢材料。NH3·BH3分子中属于sp3杂化的原子有
(4)已知:BC(碳化硼)、BN(氮化硼)的熔点依次为2450℃、3000℃, BN的熔点较高的主要原因是
(5)已知TiO2的晶胞如图1所示,“黑球”代表
(6)钛晶体有两种结构,如图2和图3所示。

图2结构中空间利用率(φ)为
您最近一年使用:0次
2022-04-26更新
|
590次组卷
|
3卷引用:重庆市长寿中学校2022-2023学年高三上学期12月月考化学试题
重庆市长寿中学校2022-2023学年高三上学期12月月考化学试题安徽省河南省皖豫名校联盟体2022届高三下学期第三次考试理综化学试题(已下线)押全国卷理综第35题 物质结构与性质-备战2022年高考化学临考题号押题(课标全国卷)
名校
解题方法
9 . 氮、磷、砷、锑为元素周期表中原子序数依次增大的同族元素。
(1)锑在元素周期表中的位置_______ 。
(2)除 外,科学家还先后研究出了
外,科学家还先后研究出了 、
、 、
、 、高聚氮等氮的单质。
、高聚氮等氮的单质。 为正四面体结构,高聚氮具有空间网状结构,如图所示。
为正四面体结构,高聚氮具有空间网状结构,如图所示。
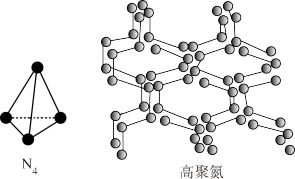
① 分子是一种
分子是一种_______ (填“极性”或“非极性”)分子。
② 的沸点
的沸点_______ (填“>”、“<”或“=”)高聚氮的沸点,原因是_______ 。
(3)热稳定性:
_______  (填“>”“<”),判断依据是
(填“>”“<”),判断依据是_______ 。
(4) 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为_______ ,C原子的杂化类型为_______ 。
(1)锑在元素周期表中的位置
(2)除
 外,科学家还先后研究出了
外,科学家还先后研究出了 、
、 、
、 、高聚氮等氮的单质。
、高聚氮等氮的单质。 为正四面体结构,高聚氮具有空间网状结构,如图所示。
为正四面体结构,高聚氮具有空间网状结构,如图所示。
①
 分子是一种
分子是一种②
 的沸点
的沸点(3)热稳定性:

 (填“>”“<”),判断依据是
(填“>”“<”),判断依据是(4)
 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为
您最近一年使用:0次
名校
10 . 按要求填空。
(1) 中心原子价层电子对互斥模型为
中心原子价层电子对互斥模型为_______ 。
(2)等电子体是具有相同的价电子数和原子数的分子或离子,它们通常具有相似的空间结构。CO的结构式为_______ , 的空间结构为
的空间结构为_______ 。
(3)根据对角线规则,铍(Be)的性质_______ (填化学式)相似,能与氢氧化钠溶液反应。写出氢氧化铍与氢氧化钠溶液反应的化学方程式_______ 。
(4)某有机物结构简式为 ,该分子中含有
,该分子中含有_______ 个手性碳原子。
(1)
 中心原子价层电子对互斥模型为
中心原子价层电子对互斥模型为(2)等电子体是具有相同的价电子数和原子数的分子或离子,它们通常具有相似的空间结构。CO的结构式为
 的空间结构为
的空间结构为(3)根据对角线规则,铍(Be)的性质
(4)某有机物结构简式为
 ,该分子中含有
,该分子中含有
您最近一年使用:0次



