1 .  和
和 均属于稀有金属,在生产、科技和军事领域均有重要的研究和应用价值。回答下列问题:
均属于稀有金属,在生产、科技和军事领域均有重要的研究和应用价值。回答下列问题:
(1)基态 原子的价电子排布式为
原子的价电子排布式为_______ ;基态 原子占据最高能层的核外电子的电子云轮廓图的形状为
原子占据最高能层的核外电子的电子云轮廓图的形状为_______ 。
(2) 和
和 处于同一周期,且核外最高能层电子构型相同。金属
处于同一周期,且核外最高能层电子构型相同。金属 的熔点
的熔点_______ (填“高于”或“低于”)金属 ,原因为
,原因为_______ 。
(3) 能形成多种重要配合物,如
能形成多种重要配合物,如 能形成
能形成 能形成
能形成 、
、 等。
等。
 ①中所含阴离子的每个原子最外层均满足
①中所含阴离子的每个原子最外层均满足 结构。该阴离子的立体构型为
结构。该阴离子的立体构型为_______ ,其中心原子的杂化形式为_______ 。
② 中含有
中含有 键的数目为
键的数目为_______ 。
(4) 能形成多种化合物,如
能形成多种化合物,如 、
、 。基态
。基态 原子的第一电离能
原子的第一电离能_______  填“大于”或“小于”
填“大于”或“小于” 基态
基态 原子。
原子。
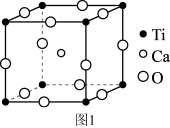
(5)钛酸钙晶胞结构如图1所示。钛酸钙的化学式为_______ ; 个钛离子与
个钛离子与_______ 个氧离子等距离且最近,连接这些氧离子构成正八面体,钛离子位于该正八面体的体心。
(6)铁和氮可组成一种过渡金属氮化物,其晶胞结构如图2所示。六棱柱底边边长为 ,高为
,高为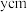 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则它的密度为
,则它的密度为_______  (列算式即可) 。
(列算式即可) 。
 和
和 均属于稀有金属,在生产、科技和军事领域均有重要的研究和应用价值。回答下列问题:
均属于稀有金属,在生产、科技和军事领域均有重要的研究和应用价值。回答下列问题:(1)基态
 原子的价电子排布式为
原子的价电子排布式为 原子占据最高能层的核外电子的电子云轮廓图的形状为
原子占据最高能层的核外电子的电子云轮廓图的形状为(2)
 和
和 处于同一周期,且核外最高能层电子构型相同。金属
处于同一周期,且核外最高能层电子构型相同。金属 的熔点
的熔点 ,原因为
,原因为(3)
 能形成多种重要配合物,如
能形成多种重要配合物,如 能形成
能形成 能形成
能形成 、
、 等。
等。 ①中所含阴离子的每个原子最外层均满足
①中所含阴离子的每个原子最外层均满足 结构。该阴离子的立体构型为
结构。该阴离子的立体构型为②
 中含有
中含有 键的数目为
键的数目为(4)
 能形成多种化合物,如
能形成多种化合物,如 、
、 。基态
。基态 原子的第一电离能
原子的第一电离能 填“大于”或“小于”
填“大于”或“小于” 基态
基态 原子。
原子。(5)钛酸钙晶胞结构如图1所示。钛酸钙的化学式为
 个钛离子与
个钛离子与
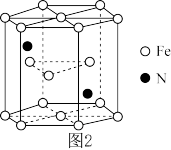
(6)铁和氮可组成一种过渡金属氮化物,其晶胞结构如图2所示。六棱柱底边边长为
 ,高为
,高为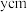 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则它的密度为
,则它的密度为 (列算式即可) 。
(列算式即可) 。
您最近一年使用:0次
名校
2 . 铬铁合金作为钢的添加料生产多种具有高强度、耐高温、耐腐蚀等优良性能的特种钢,这类特种钢中含有碳、硅、氧、氮、磷等元素。
(1)基态Fe原子的价电子排布式为_______ 。
(2)第二周期中第一电离能介于B与N之间的元素有_______ 种。
(3)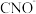 的空间构型为
的空间构型为_______ ,C的杂化方式为_______ 。
(4) 分子在独立存在时
分子在独立存在时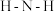 键角为
键角为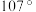 。如图是
。如图是 离子的部分结构以及
离子的部分结构以及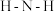 键角的测量值。解释
键角的测量值。解释 形成如图配合物后
形成如图配合物后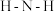 键角变大的原因:
键角变大的原因:_______ 。
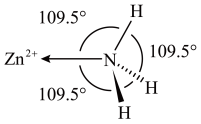
(5)有机铁肥 中不存在的化学键有
中不存在的化学键有_______ 。(填字母)
A.离子键 B.金属键 C.配位键 D. 键 E.氢键
键 E.氢键
(6)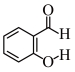 和
和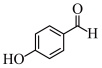 两种物质中,沸点更高的是
两种物质中,沸点更高的是 _______ (填名称)
(7)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色,该反应中有时用Fe(SCN)3表示形成的配合物,经研究表明Fe3+与SCN-不仅能以1:3的个数比配合,还可以以其他个数比配合。
请按要求填空:
①Fe3+与SCN-反应时,Fe3+提供_______ ,SCN-提供_______ ,二者通过配位键结合。
②所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合,所得离子显红色,含该离子的配合物化学式是_______ 。
(1)基态Fe原子的价电子排布式为
(2)第二周期中第一电离能介于B与N之间的元素有
(3)
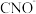 的空间构型为
的空间构型为(4)
 分子在独立存在时
分子在独立存在时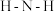 键角为
键角为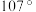 。如图是
。如图是 离子的部分结构以及
离子的部分结构以及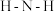 键角的测量值。解释
键角的测量值。解释 形成如图配合物后
形成如图配合物后 键角变大的原因:
键角变大的原因:
(5)有机铁肥
 中不存在的化学键有
中不存在的化学键有A.离子键 B.金属键 C.配位键 D.
 键 E.氢键
键 E.氢键(6)
 和
和 两种物质中,沸点更高的是
两种物质中,沸点更高的是 (7)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色,该反应中有时用Fe(SCN)3表示形成的配合物,经研究表明Fe3+与SCN-不仅能以1:3的个数比配合,还可以以其他个数比配合。
请按要求填空:
①Fe3+与SCN-反应时,Fe3+提供
②所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合,所得离子显红色,含该离子的配合物化学式是
您最近一年使用:0次
名校
解题方法
3 . Ⅰ. 有下列物质:①
有下列物质:① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦SiO2、⑧PCl3
、⑦SiO2、⑧PCl3
(1)常温下为共价晶体是_______ (填序号,下同)。
(2)既有 键又有
键又有 键的非极性分子是
键的非极性分子是_______ 。
(3) 模型是四面体形的极性分子是
模型是四面体形的极性分子是_______ 。
(4)分子空间构型三角锥形的是_______ 。
(5)中心原子发生 杂化的是
杂化的是_______ ,与甲烷分子空间结构相同的是_______ 。
Ⅱ.回答下列问题
(6) 中碳原子的杂化方式为
中碳原子的杂化方式为_______ 。 分子中
分子中 原子的杂化方式为
原子的杂化方式为_______ 。
(7)从结构角度分析, 的空间构型为
的空间构型为_______ 。 和
和 两种阳离子的相同之处为
两种阳离子的相同之处为_______ (填字母)。
A.中心原子的杂化轨道类型 B.中心原子的价层电子对数 C.立体构型 D.共价键类型
(8)X射线衍射测定发现,I3AsF6中存在I 。I
。I 的立体构型为
的立体构型为_______ ,中心原子的杂化方式为_______ 。
 有下列物质:①
有下列物质:① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦SiO2、⑧PCl3
、⑦SiO2、⑧PCl3(1)常温下为共价晶体是
(2)既有
 键又有
键又有 键的非极性分子是
键的非极性分子是(3)
 模型是四面体形的极性分子是
模型是四面体形的极性分子是(4)分子空间构型三角锥形的是
(5)中心原子发生
 杂化的是
杂化的是Ⅱ.回答下列问题
(6)
 中碳原子的杂化方式为
中碳原子的杂化方式为 分子中
分子中 原子的杂化方式为
原子的杂化方式为(7)从结构角度分析,
 的空间构型为
的空间构型为 和
和 两种阳离子的相同之处为
两种阳离子的相同之处为A.中心原子的杂化轨道类型 B.中心原子的价层电子对数 C.立体构型 D.共价键类型
(8)X射线衍射测定发现,I3AsF6中存在I
 。I
。I 的立体构型为
的立体构型为
您最近一年使用:0次
名校
4 . 已知某紫色配合物的组成为CoCl3·5NH3·H2O,其水溶液显弱酸性,加入强碱并加热至沸腾有NH3放出,同时产生Co2O3沉淀;向一定量该配合物溶液中加过量AgNO3溶液,有AgCl沉淀生成,待沉淀完全后过滤,再加过量AgNO3溶液于滤液中,无明显变化,但加热至沸腾又有AgCl沉淀生成,且第二次沉淀量为第一次沉淀量的二分之一,则该配合物的化学式最可能为
| A.[CoCl2(NH3)4]Cl·NH3·H2O | B.[Co(NH3)5(H2O)]Cl3 |
| C.[CoCl2(NH3)3(H2O)]Cl·2NH3 | D.[CoCl(NH3)5]Cl2·H2O |
您最近一年使用:0次
2022-08-20更新
|
395次组卷
|
6卷引用:重庆市清华中学2021-2022学年高二下学期期第一次月考化学试题
重庆市清华中学2021-2022学年高二下学期期第一次月考化学试题(已下线)同步君 选修3 第二章 第二节 配合物理论高中化学人教版 选修三 第2章 分子结构与性质 配合物理论(已下线)微项目 补铁剂中铁元素的检验-应用配合物进行物质检验-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)吉林省通化市梅河口市第五中学2022-2023学年高二上学期期末考试化学试题(已下线)3.4 配合物与超分子-同步学习必备知识
名校
解题方法
5 . 下列描述中,正确的是
| A.CS2是空间结构为V形的极性分子 |
B.ClO 和ClO 和ClO 的VSEPR模型相同,但离子空间结构不同 的VSEPR模型相同,但离子空间结构不同 |
C.NO 和NH3的空间结构均为三角锥形 和NH3的空间结构均为三角锥形 |
D.SiF4和CO 的中心原子的杂化轨道类型均为sp3杂化 的中心原子的杂化轨道类型均为sp3杂化 |
您最近一年使用:0次
名校
解题方法
6 . 硒( )被科学家称为人体微量元素中的“抗癌之王”,硒(
)被科学家称为人体微量元素中的“抗癌之王”,硒( )与氧(O)、硫(S)位于元素周期表中第ⅥA族。回答下列问题:
)与氧(O)、硫(S)位于元素周期表中第ⅥA族。回答下列问题:
(1)基态氧原子的价电子排布图为___________ ,第二周期元素的第一电离能比氧元素大的主族元素有___________ (填元素符号)。
(2)单质硫最稳定的结构是由八个原子组成的环—— ,其中S原子的杂化方式为
,其中S原子的杂化方式为___________ 。
(3)酸性:
___________  (填“强于”或“弱于”),
(填“强于”或“弱于”), 的空间构型为
的空间构型为___________ ,写出一种与 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:___________ 。
(4) 、
、 均为离子化合物,其熔点由高到低的顺序为
均为离子化合物,其熔点由高到低的顺序为___________ (用化学式表示),原因为___________ 。
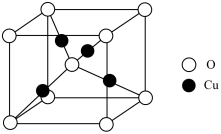
(5) 的立方晶胞结构如图所示,晶胞参数为
的立方晶胞结构如图所示,晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为___________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
 )被科学家称为人体微量元素中的“抗癌之王”,硒(
)被科学家称为人体微量元素中的“抗癌之王”,硒( )与氧(O)、硫(S)位于元素周期表中第ⅥA族。回答下列问题:
)与氧(O)、硫(S)位于元素周期表中第ⅥA族。回答下列问题:(1)基态氧原子的价电子排布图为
(2)单质硫最稳定的结构是由八个原子组成的环——
 ,其中S原子的杂化方式为
,其中S原子的杂化方式为(3)酸性:

 (填“强于”或“弱于”),
(填“强于”或“弱于”), 的空间构型为
的空间构型为 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:(4)
 、
、 均为离子化合物,其熔点由高到低的顺序为
均为离子化合物,其熔点由高到低的顺序为(5)
 的立方晶胞结构如图所示,晶胞参数为
的立方晶胞结构如图所示,晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
7 . A、B、C、D、E、F六种元素均位于元素周期表的前四周期,且原子序数依次增大。元素A是原子半径最小的元素;B元素基态原子的核外电子占据四个原子轨道;D元素原子的成对电子总数是未成对电子总数的3倍;E与D位于同一主族;F位于ds区,且原子的最外层只有1个电子。
(1)基态F原子的核外电子排布式是_______ 。
(2)B、C、D元素的第一电离能由大到小的顺序是_______ (用元素符号表示)。
(3)B、C元素的某些氢化物的分子中均含有18个电子,则B元素的这种氢化物的化学式是_______ ;B、C元素的这些氢化物的熔、沸点相差较大的主要原因是_______ 。
(4)A、B、D可形成分子式为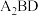 的某化合物,则该化合物分子中B原子的杂化轨道类型是
的某化合物,则该化合物分子中B原子的杂化轨道类型是_______ ;1mol该分子中含有π键的数目是_______ 。
(5)由A、D、E三种元素组成的两种常见化合物的酸性由强到弱的顺序为_______ (用化学式表示)。
(1)基态F原子的核外电子排布式是
(2)B、C、D元素的第一电离能由大到小的顺序是
(3)B、C元素的某些氢化物的分子中均含有18个电子,则B元素的这种氢化物的化学式是
(4)A、B、D可形成分子式为
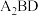 的某化合物,则该化合物分子中B原子的杂化轨道类型是
的某化合物,则该化合物分子中B原子的杂化轨道类型是(5)由A、D、E三种元素组成的两种常见化合物的酸性由强到弱的顺序为
您最近一年使用:0次
名校
解题方法
8 . 填空。
(1)下列分子中含有手性碳的是_______
(2)下列分子具有极性的是_______
A、NH3 B、CCl4 C、H2O D、CS2 E、BF3
(3)秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料。人们对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(BaCuSixOy)。“中国蓝”的发色中心是以Cu2+为中心的配位化合物,形成该配位键,Cu2+提供_______ ,若“中国蓝”的化学组成中x∶y=2∶5,则其化学式为_______ 。
(4)BaO的熔沸点_______ MgO,金刚石的熔点_______ SiC(均填“>”或“<”或“=”)
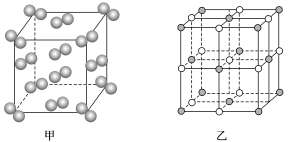
(5)131I2晶体的晶胞结构如图甲所示,该晶胞中含有_______ 个131I2分子;KI的晶胞结构如图乙所示,每个K+紧邻_______ 个I-。
(1)下列分子中含有手性碳的是_______
| A.乙醇 | B.苯 | C.一氯甲烷 | D.乳酸CH3CH(OH)COOH |
A、NH3 B、CCl4 C、H2O D、CS2 E、BF3
(3)秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料。人们对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(BaCuSixOy)。“中国蓝”的发色中心是以Cu2+为中心的配位化合物,形成该配位键,Cu2+提供
(4)BaO的熔沸点
(5)131I2晶体的晶胞结构如图甲所示,该晶胞中含有
您最近一年使用:0次
2022-04-01更新
|
314次组卷
|
3卷引用:重庆市实验中学校2021-2022学年高二下学期第一次月考化学试题
名校
9 . 从微粒结构角度分析,下列说法错误的是
A.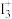 的空间结构为V形,中心原子的杂化方式为sp3 的空间结构为V形,中心原子的杂化方式为sp3 |
| B.ZnCO3中阴离子空间结构为平面三角形,C原子的杂化方式为sp2 |
| C.根据价层电子对互斥模型,H2S、SO2、SO3的气态分子中,H2S的中心原子价层电子对数与其他分子不同 |
D.三氧化硫有单分子气体和三聚分子固体(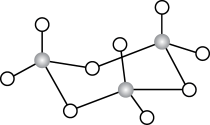 )两种存在形式,两种形式中S原子的杂化轨道类型相同 )两种存在形式,两种形式中S原子的杂化轨道类型相同 |
您最近一年使用:0次
2022-04-01更新
|
424次组卷
|
5卷引用:重庆市实验中学校2021-2022学年高二下学期第一次月考化学试题
名校
解题方法
10 . 锰单质及其化合物应用十分广泛。回答下列问题:
(1)基态锰原子的核外电子排布式为___________ 。
(2)MnO和MnS的熔点分别为1650℃和1610℃,前者熔点较高的原因是___________ 。
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。

BH 的空间构型为
的空间构型为___________ ,写出两种与BH 互为等电子体的分子或离子
互为等电子体的分子或离子___________ 。
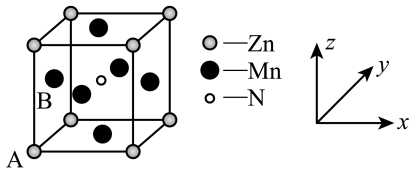
(4)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为___________ ;其中原子坐标参数A为(0,0,0),B为(0, ,
, ),则晶胞中氮原子的坐标参数为
),则晶胞中氮原子的坐标参数为___________ 。
(5)金属锰有多种晶型,其中δ-Mn的结构为体心立方堆积,晶胞参数为apm。已知阿伏加德罗常数的值为NA,δ-Mn的理论密度ρ=___________ g•cm-3(列出计算式)。
(1)基态锰原子的核外电子排布式为
(2)MnO和MnS的熔点分别为1650℃和1610℃,前者熔点较高的原因是
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。

BH
 的空间构型为
的空间构型为 互为等电子体的分子或离子
互为等电子体的分子或离子(4)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为
 ,
, ),则晶胞中氮原子的坐标参数为
),则晶胞中氮原子的坐标参数为
(5)金属锰有多种晶型,其中δ-Mn的结构为体心立方堆积,晶胞参数为apm。已知阿伏加德罗常数的值为NA,δ-Mn的理论密度ρ=
您最近一年使用:0次



