名校
解题方法
1 . 下列说法正确的是
A.乙二胺(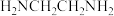 )的沸点低于 )的沸点低于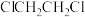 |
B.金刚石晶体中,碳原子数目与碳碳键数目之比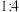 |
C. 的空间结构为V形,中心原子的杂化方式为 的空间结构为V形,中心原子的杂化方式为 |
D.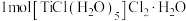 和足量 和足量 溶液反应,能产 溶液反应,能产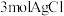 |
您最近一年使用:0次
2 . 回答下列问题:
(1)固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为___________ 。

(2)乙烯酮在室温下可聚合成二聚乙烯酮(结构简式为 ),二聚乙烯酮分子中含有的
),二聚乙烯酮分子中含有的 键与
键与 键的数目之比为
键的数目之比为__________ 。如图中表示的碳原子能量最高的是__________ (填字母)。
A. B.
B.
C. D.
D.
(3)三甲胺 和乙二胺
和乙二胺 均属于胺,但三甲胺比乙二胺的沸点低得多,原因是
均属于胺,但三甲胺比乙二胺的沸点低得多,原因是_______ 。
(4) 的三种结构:①
的三种结构:① 、②
、②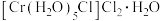 、③
、③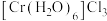 ,下列说法正确的是
,下列说法正确的是___ 。
A.①②③中 的配位数都是6
的配位数都是6
B.②中存在的化学键有离子键、共价键、配位键和氢键
C.等物质的量的①②③分别与足量 溶液反应,得到
溶液反应,得到 物质的量也相等
物质的量也相等
(5)对配合物 进行加热时,比更容易失去的配体
进行加热时,比更容易失去的配体___________ 。
(1)固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为

(2)乙烯酮在室温下可聚合成二聚乙烯酮(结构简式为
 ),二聚乙烯酮分子中含有的
),二聚乙烯酮分子中含有的 键与
键与 键的数目之比为
键的数目之比为A.
 B.
B.
C.
 D.
D.
(3)三甲胺
 和乙二胺
和乙二胺 均属于胺,但三甲胺比乙二胺的沸点低得多,原因是
均属于胺,但三甲胺比乙二胺的沸点低得多,原因是(4)
 的三种结构:①
的三种结构:① 、②
、②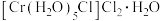 、③
、③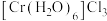 ,下列说法正确的是
,下列说法正确的是A.①②③中
 的配位数都是6
的配位数都是6B.②中存在的化学键有离子键、共价键、配位键和氢键
C.等物质的量的①②③分别与足量
 溶液反应,得到
溶液反应,得到 物质的量也相等
物质的量也相等(5)对配合物
 进行加热时,比更容易失去的配体
进行加热时,比更容易失去的配体
您最近一年使用:0次
名校
解题方法
3 . 下列实验操作、现象和结论均正确的是选项
选项 | 操作 | 现象 | 结论 |
A |  和 和 按 按 混合,光照 混合,光照 | 试管壁出现油状液滴 | 油状液滴为 |
B | 在酸性 溶液中加入甲苯 溶液中加入甲苯 | 溶液褪色 | 甲苯中有碳碳双键 |
C | 在2-溴丁烷水解产物中直接加入 溶液 溶液 | 产生浅黄色沉淀 | 2-溴丁烷含溴元素 |
D |  溶液中逐渐滴加氨水 溶液中逐渐滴加氨水 | 先生成天蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色溶液 | 天蓝色沉淀为 ,继续滴加氨水时: ,继续滴加氨水时: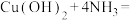 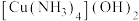 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 下列表述不正确的是
A.键角: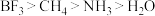 | B. 空间结构为平面正三角形 空间结构为平面正三角形 |
C. 不能作为配合物的配位体 不能作为配合物的配位体 | D.等质量的甲烷和乙烯完全燃烧,乙烯的耗氧量更多 |
您最近一年使用:0次
名校
解题方法
5 . 光刻胶主要应用于显示面板、集成电路等细微图形加工,其合成路线如图(部分试剂和产物略)。

已知: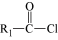 + R2OH
+ R2OH
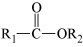 + HCl
+ HCl
(1)A的化学名称为__________ ,C中含氧官能团的名称为____________ 。
(2)CH≡CH中C的杂化方式为_______ ,生成E的反应类型为____________ 。
(3)E物质不能发生的反应是_______ (填序号)。
a.加成反应 b.消去反应 c.取代反应 d.加聚反应 e.缩聚反应
(4)物质G常用作尿不湿的材料,这是因为________________________________ 。
(5)D和G反应生成光刻胶的化学反应方程式为______________________ 。
(6)满足下列条件的B的同分异构体有_______ 种。
①分子中含有苯环;②能发生银镜反应;③能使溴的四氯化碳溶液褪色。其中一种同分异构体的核磁共振氢谱峰面积之比为2∶2∶2∶1∶1,写出其可能的结构简式_____________________ 。

已知:
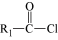 + R2OH
+ R2OH
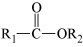 + HCl
+ HCl(1)A的化学名称为
(2)CH≡CH中C的杂化方式为
(3)E物质不能发生的反应是
a.加成反应 b.消去反应 c.取代反应 d.加聚反应 e.缩聚反应
(4)物质G常用作尿不湿的材料,这是因为
(5)D和G反应生成光刻胶的化学反应方程式为
(6)满足下列条件的B的同分异构体有
①分子中含有苯环;②能发生银镜反应;③能使溴的四氯化碳溶液褪色。其中一种同分异构体的核磁共振氢谱峰面积之比为2∶2∶2∶1∶1,写出其可能的结构简式
您最近一年使用:0次
名校
6 . 氮元素在农药生产及工业制造业等领域用途非常广泛。回答下列问题:
(1)NH3是重要的配体,其中H—N—H的键角为107.3°。
①NH3分子的VSEPR模型为___________ 。
②[Cu(NH3)4]2+中H—N—H的键角_____ 107.3°(填“大于”“小于”或“等于”)。
③甲基胺离子(CH3NH3+)的电子式为______________ 。
(2)已知氨在一定条件下可形成一种立方晶系,其立方晶胞沿x、y或z轴投影图均如图所示。已知晶胞的棱长为a pm,则该晶体的密度为______ g/cm3。(写出数学表达式,设NA为阿伏加德罗常数的值)。

(3)CO和H2可以合成简单有机物,已知CO、H2合成CH3OH、HCOOCH3的能量变化如图所示,计算:2CH3OH(g) HCOOCH3(g)+2H2(g) △H=
HCOOCH3(g)+2H2(g) △H=_____ 。

已知键能数据如下表,则C≡O的键能为__________ kJ•mol-1。
(4)利用电解原理,可将氨气转化为高纯氢气,其装置如图所示。
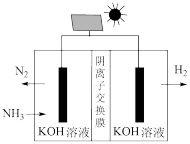
电解过程中OH—的移动方向为____ (填“从左往右”或“从右往左”);阳极的电极反应式为______________ 。
(1)NH3是重要的配体,其中H—N—H的键角为107.3°。
①NH3分子的VSEPR模型为
②[Cu(NH3)4]2+中H—N—H的键角
③甲基胺离子(CH3NH3+)的电子式为
(2)已知氨在一定条件下可形成一种立方晶系,其立方晶胞沿x、y或z轴投影图均如图所示。已知晶胞的棱长为a pm,则该晶体的密度为

(3)CO和H2可以合成简单有机物,已知CO、H2合成CH3OH、HCOOCH3的能量变化如图所示,计算:2CH3OH(g)
 HCOOCH3(g)+2H2(g) △H=
HCOOCH3(g)+2H2(g) △H=
已知键能数据如下表,则C≡O的键能为
化学键 | H-H | C-O | C≡O | H-O | C-H |
键能/(kJ•mol-1) | 436 | 326 | A | 464 | 414 |

电解过程中OH—的移动方向为
您最近一年使用:0次
名校
7 . 硼氢化钠(NaBH4)具有很强的还原性,被称为“万能还原剂”,它在催化剂钌(44Ru)表面与水反应的历程如图所示,下列说法不正确的是
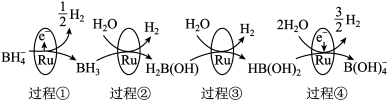
| A.元素钌(44Ru)在元素周期表中位于d区 |
| B.BH3分子中B原子为sp2杂化且不含孤对电子 |
| C.过程④中产生1 mol H2,转移电子的物质的量为2 mol |
| D.硼氢化钠中硼元素的化合价为+3价,反应过程中硼元素的化合价始终保持不变 |
您最近一年使用:0次
2023-01-17更新
|
504次组卷
|
6卷引用:重庆市第十一中学校2022-2023学年高三上学期12月月考化学试题
8 . 第三代半导体材料以碳化硅和氮化镓为主,广泛应用于新能源汽车、高铁等领域。
(1)基态Si原子的价电子排布图为_______ 。
(2)C、N、Si的第一电离能由大到小的顺序是_______ (填元素符号)。
(3) 的空间构型为
的空间构型为_______ ,其中碳原子的杂化轨道类型为_______ 。
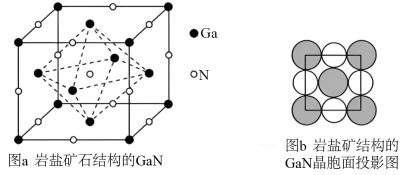
(4)岩盐矿结构的GaN晶体结构如图a、图b所示,Ga、N原子半径分别为 、
、 ,则Ga原子的配位数为
,则Ga原子的配位数为_______ ,设阿伏加德罗常数的值为NA,则该GaN的密度是_______  (列出算式)。
(列出算式)。
(5)煤的气化是一种重要的制氢途径。在一定温度下:向体积固定的密闭容器中加入足量的 和1mol
和1mol ,发生下列反应生成水煤气:
,发生下列反应生成水煤气:
Ⅰ.

Ⅱ.

反应平衡时, 的转化率为50%,CO的物质的量为0.1mol。
的转化率为50%,CO的物质的量为0.1mol。
①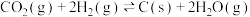

_______ 。
②下列说法正确的是_______ 。
A.将炭块粉碎,可加快反应速率
B.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
C.混合气体的密度保持不变时,说明反应体系已达到平衡
D.平衡时 的体积分数可能大于
的体积分数可能大于
③求反应Ⅱ的平衡常数K=_______ 。
(1)基态Si原子的价电子排布图为
(2)C、N、Si的第一电离能由大到小的顺序是
(3)
 的空间构型为
的空间构型为(4)岩盐矿结构的GaN晶体结构如图a、图b所示,Ga、N原子半径分别为
 、
、 ,则Ga原子的配位数为
,则Ga原子的配位数为 (列出算式)。
(列出算式)。
(5)煤的气化是一种重要的制氢途径。在一定温度下:向体积固定的密闭容器中加入足量的
 和1mol
和1mol ,发生下列反应生成水煤气:
,发生下列反应生成水煤气:Ⅰ.


Ⅱ.


反应平衡时,
 的转化率为50%,CO的物质的量为0.1mol。
的转化率为50%,CO的物质的量为0.1mol。①
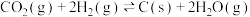

②下列说法正确的是
A.将炭块粉碎,可加快反应速率
B.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
C.混合气体的密度保持不变时,说明反应体系已达到平衡
D.平衡时
 的体积分数可能大于
的体积分数可能大于
③求反应Ⅱ的平衡常数K=
您最近一年使用:0次
名校
9 . Ⅰ.全球首次在350公里时速的奥运版复兴号高铁列车上依托5G技术打造的超高清直播演播室,实现了超高清信号的长时间稳定传输。请回答下列问题:
(1)5G芯片主要材质是高纯硅。基态Si原子价层电子的运动状态有_______ 种,若其电子排布式表示为[Ne]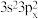 违背了
违背了_______ 。
(2)高纯硅制备过程中会有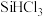 、
、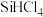 等中间产物生成。已知电负性;
等中间产物生成。已知电负性; ,则
,则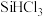 充分水解的化学方程式为
充分水解的化学方程式为_______ ,复兴号高铁车体材质用到Mn、Co等元素,Mn的一种配合物化学式为[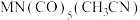 ],
], 中C原子的杂化类型为
中C原子的杂化类型为_______ 。
Ⅱ.碳及其化合物对人类的生产、生活有重大影响,一直是科技工作者的研究热点。回答下列问题:
已知:①部分化学键的键能数据如表:
②热化学反应方程及化学平衡常数如下:
反应i;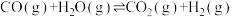
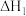
反应ii;
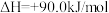
反应iii:
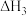
(3)则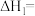
_______  ;化学平衡常数
;化学平衡常数 与
与 、
、 的关系为
的关系为_______ 。
(4)在恒温、恒压条件下,以22.4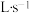 (已转化为标准状况)将CO(g)和
(已转化为标准状况)将CO(g)和 (g)的混合气体通入装有催化剂的连续反应器中发生反应:
(g)的混合气体通入装有催化剂的连续反应器中发生反应: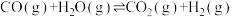 。
。
①0~5内测得CO的体积分数由25%变为20%则该时间段内用 表示的化学反应速率为
表示的化学反应速率为_______ 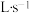 。
。
②该反应达到平衡后,若增大压强,平衡_______ 移动(填“向左”“向右”或“不”);若升高温度,CO的平衡转化率_______ (填“变大”“变小”或“不变”)。
(1)5G芯片主要材质是高纯硅。基态Si原子价层电子的运动状态有
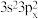 违背了
违背了(2)高纯硅制备过程中会有
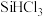 、
、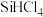 等中间产物生成。已知电负性;
等中间产物生成。已知电负性; ,则
,则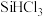 充分水解的化学方程式为
充分水解的化学方程式为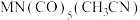 ],
], 中C原子的杂化类型为
中C原子的杂化类型为Ⅱ.碳及其化合物对人类的生产、生活有重大影响,一直是科技工作者的研究热点。回答下列问题:
已知:①部分化学键的键能数据如表:
| 化学键 | H-H | C=O | C≡O | O-H |
键能/( ) ) | 436 | 745 | 960 | 463 |
②热化学反应方程及化学平衡常数如下:
反应i;
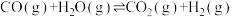
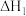
反应ii;

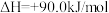
反应iii:

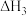
(3)则
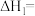
 ;化学平衡常数
;化学平衡常数 与
与 、
、 的关系为
的关系为(4)在恒温、恒压条件下,以22.4
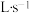 (已转化为标准状况)将CO(g)和
(已转化为标准状况)将CO(g)和 (g)的混合气体通入装有催化剂的连续反应器中发生反应:
(g)的混合气体通入装有催化剂的连续反应器中发生反应: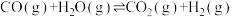 。
。①0~5内测得CO的体积分数由25%变为20%则该时间段内用
 表示的化学反应速率为
表示的化学反应速率为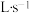 。
。②该反应达到平衡后,若增大压强,平衡
您最近一年使用:0次
名校
解题方法
10 . 在萜类天然产物中,氧化态升高与抗癌、抗病毒和免疫抑制的生物活性提高密切相关。某分子如图所示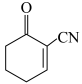 ,下列说法不正确的是
,下列说法不正确的是
 ,下列说法不正确的是
,下列说法不正确的是| A.该分子能发生氧化反应、还原反应、取代反应 |
| B.该分子所有原子不可能共面 |
| C.该分子中σ键与π键数目之比为16:4 |
| D.该分子中C原子有两种杂化方式 |
您最近一年使用:0次



