名校
解题方法
1 . 根据VSEPR模型判断下列各组分子或离子空间结构相同的是
A. 和 和 | B. 和 和 | C. 和 和 | D. 和 和 |
您最近一年使用:0次
2023-01-11更新
|
491次组卷
|
6卷引用:广东省佛山市顺德区第一中学2022-2023学年高二下学期4月期中考试化学试题
名校
2 . 氯元素有多种化合价,可形成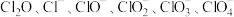 等微粒。下列说法错误的是
等微粒。下列说法错误的是
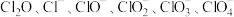 等微粒。下列说法错误的是
等微粒。下列说法错误的是A. 中Cl原子的杂化方式均为 中Cl原子的杂化方式均为 杂化 杂化 |
B.基态 原子核外电子的空间运动状态有9种 原子核外电子的空间运动状态有9种 |
C.键角: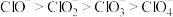 |
D. 的空间构型为V形,分子中的化学键的键长和键角可以通过X射线衍射实验获得 的空间构型为V形,分子中的化学键的键长和键角可以通过X射线衍射实验获得 |
您最近一年使用:0次
2023-01-10更新
|
827次组卷
|
5卷引用:广东省佛山市南海区狮山石门高级中学2022-2023学年高二下学期3月月考化学试题
名校
解题方法
3 . 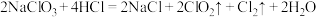 可用于制备含氯消毒剂。二氧化氯(
可用于制备含氯消毒剂。二氧化氯( )是一种黄绿色气体,易溶于水,在水中的溶解度约为
)是一种黄绿色气体,易溶于水,在水中的溶解度约为 的5倍,其水溶液在较高温度与光照下会生成
的5倍,其水溶液在较高温度与光照下会生成 与
与 。
。 是一种极易爆炸的强氧化性气体。下列关于
是一种极易爆炸的强氧化性气体。下列关于 、
、 和
和 的说法正确的是
的说法正确的是
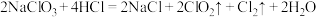 可用于制备含氯消毒剂。二氧化氯(
可用于制备含氯消毒剂。二氧化氯( )是一种黄绿色气体,易溶于水,在水中的溶解度约为
)是一种黄绿色气体,易溶于水,在水中的溶解度约为 的5倍,其水溶液在较高温度与光照下会生成
的5倍,其水溶液在较高温度与光照下会生成 与
与 。
。 是一种极易爆炸的强氧化性气体。下列关于
是一种极易爆炸的强氧化性气体。下列关于 、
、 和
和 的说法正确的是
的说法正确的是A. 为非极性分子 为非极性分子 | B. 中含有非极性键 中含有非极性键 |
C. 的空间结构为三角锥形 的空间结构为三角锥形 | D. 与 与 的键角相等 的键角相等 |
您最近一年使用:0次
2022-12-31更新
|
526次组卷
|
3卷引用:广东省梅州市名校2022-2023学年高三上学期期末考试化学试题
4 . 下列化学用语表示错误是
A.2-甲基戊烷的键线式: |
B.KCl的形成过程: |
C. 的VSEPR模型: 的VSEPR模型: |
D.基态Mg原子的核外电子排布图: |
您最近一年使用:0次
解题方法
5 . 用氨水吸收硫酸工厂尾气中的 ,发生的反应为:
,发生的反应为: 。下列说法正确的是
。下列说法正确的是
 ,发生的反应为:
,发生的反应为: 。下列说法正确的是
。下列说法正确的是A. 分子的空间结构呈V形 分子的空间结构呈V形 | B. 的电子式为 的电子式为 |
C. 是非极性分子 是非极性分子 | D. 的VSEPR模型为平面三角形 的VSEPR模型为平面三角形 |
您最近一年使用:0次
2022-12-28更新
|
415次组卷
|
3卷引用:广东省东莞市2022-2023学年高三上学期期末教学质量检查化学试题
广东省东莞市2022-2023学年高三上学期期末教学质量检查化学试题(已下线)广东省东莞市2022-2023学年高三上学期期末教学质量检查变式汇编(1-10)广东省普宁市勤建学校2022-2023学年高二下学期学科竞赛化学试题
名校
解题方法
6 . 由徐光宪院士发起院士学子同创的《分子共和国》科普读物生动形象地戏说了BF3、NH3、H2S、O3、CH3COOH、SOCl2等众多“分子共和国”中的明星。下列说法正确的是
| A.NH3中心原子为sp3杂化,BF3中心原子为sp2杂化 |
| B.BF3和NH3都属于非极性分子 |
C.所有分子都只存在 键,不存在 键,不存在 键 键 |
| D.H2S、O3分子的空间结构均为直线形 |
您最近一年使用:0次
名校
解题方法
7 . 某油脂厂废弃的油脂加氢镍催化剂的主要成分为Ni,还含有一定量Al、Fe及氧化铁、少量其他不溶性物质,回收废镍催化剂制备硫酸镍晶体( )的工艺流程如下:
)的工艺流程如下:
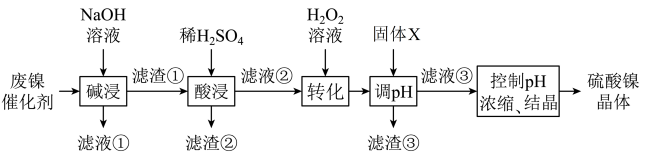
已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)下列状态的Ni微粒中,电离最外层一个电子所需能量最大的是_______(填标号)。
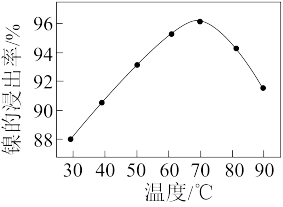
(2)“碱浸”中NaOH溶液的两个作用分别是_______ 。如图是“酸浸”时镍的浸出率与温度的关系,则酸浸时合适的浸出温度是_______ ℃。
(3)为回收金属,向“滤液①”中通入过量二氧化碳气体,反应的离子方程式为_______ 。
(4)“转化”步骤中反应的离子方程式是_____ 。“调pH”时,最适宜的pH范围是______ 。
(5)Ni可以形成多种多样的配合物。 、
、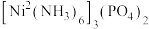 是镍的两种配合物,这两种配合物都存在的作用力是
是镍的两种配合物,这两种配合物都存在的作用力是_______ (填标号)。
a.范德华力 b.配位键 c.极性键 d.离子键 e.氢键 f.非极性键
(6) 中阴离子的空间构型为
中阴离子的空间构型为_______ 。
 )的工艺流程如下:
)的工艺流程如下:
已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |
开始沉淀的pH( ) ) | 2.2 | 7.5 | 7.2 |
沉淀完全的pH( ) ) | 3.2 | 9.0 | 8.7 |
回答下列问题:
(1)下列状态的Ni微粒中,电离最外层一个电子所需能量最大的是_______(填标号)。
A. | B.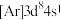 | C.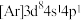 | D. |

(3)为回收金属,向“滤液①”中通入过量二氧化碳气体,反应的离子方程式为
(4)“转化”步骤中反应的离子方程式是
(5)Ni可以形成多种多样的配合物。
 、
、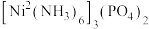 是镍的两种配合物,这两种配合物都存在的作用力是
是镍的两种配合物,这两种配合物都存在的作用力是a.范德华力 b.配位键 c.极性键 d.离子键 e.氢键 f.非极性键
(6)
 中阴离子的空间构型为
中阴离子的空间构型为
您最近一年使用:0次
名校
8 . 回答下列问题
(1)按要求填空:
①CO2的电子式为:____________________
②基态N原子的轨道表示为________________________________________ ;
③基态Ga原子价电子层的电子排布式为_____________________________ ;
(2)对于A.MgO B.He C.NH3 D.CaO E.干冰 F.Ar五种物质:
①熔沸点最低的是________ ;液态时能导电的是________ (填字母编号)。
②上述物质所含的元素中,基态原子含单电子最多的元素是______ (填元素符号)。
③上述物质的晶体中,属于离子晶体且熔点最高的是____________ (填字母编号)。
④上述物质的晶体熔化时,所克服的微粒间的作用力与冰熔化时所克服的作用力类型完全相同的是______ (填字母编号)。
(3)已知熔融的BeCl2不导电,则BeCl2属于_______ 晶体,中心原子的杂化类型为______ 。
(1)按要求填空:
①CO2的电子式为:
②基态N原子的轨道表示为
③基态Ga原子价电子层的电子排布式为
(2)对于A.MgO B.He C.NH3 D.CaO E.干冰 F.Ar五种物质:
①熔沸点最低的是
②上述物质所含的元素中,基态原子含单电子最多的元素是
③上述物质的晶体中,属于离子晶体且熔点最高的是
④上述物质的晶体熔化时,所克服的微粒间的作用力与冰熔化时所克服的作用力类型完全相同的是
(3)已知熔融的BeCl2不导电,则BeCl2属于
您最近一年使用:0次
2022-12-20更新
|
289次组卷
|
2卷引用:广东省梅州市大埔县实验中学2021-2022学年高二下学期第一次段考(4月)化学试题
名校
解题方法
9 . 根据杂化轨道理论和价层电子对互斥模型判断,下列结果错误的是
| 选项 | 分子或离子 | 价层电子对互斥模型 | 分子或离子的空间结构名称 |
| A | CO2 | 直线形 | 直线形 |
| B | HCHO | 平面三角形 | 平面三角形 |
| C | CO | 四面体 | 三角锥形 |
| D | H3O+ | 四面体 | 三角锥形 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-20更新
|
335次组卷
|
3卷引用:广东省广州市白云中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
10 . AlN具有耐高温、抗冲击等优良品质,广泛应用于电子工业、陶瓷工业,其晶胞结构如下图所示。下列说法错误的是


A.基态Al原子的价电子排布式为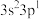 | B.Al原子位于N原子形成的四面体空隙 |
| C.AlN晶体中含有配位键 | D.AlN晶体属于离子晶体 |
您最近一年使用:0次
2022-11-30更新
|
565次组卷
|
2卷引用:广东省深圳市龙岗区2022-2023学年高三上学期期中考试化学试题



