名校
解题方法
1 . 一种含Pt催化剂催化甲烷中的碳氢键活化的反应机理如图所示。下列有关说法正确的是
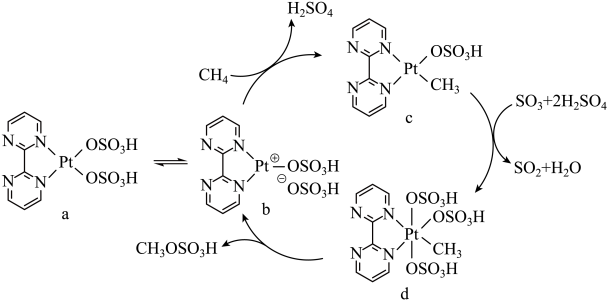
| A.SO2和SO3都是极性分子 | B.SO3是中间产物 |
| C.c→d的反应是氧化还原反应 | D.催化循环中Pt的配位数不改变 |
您最近一年使用:0次
7日内更新
|
133次组卷
|
3卷引用:云南省昆明市云南师范大学附属中学2023-2024学年高三下学期适应性月考(九)理综试卷-高中化学
2 . 中南大学刘又年、黄健涵、李嘉伟团队提出发展炔烃、醛、胺等工业大宗原料和炉烟二氧化碳的四组分串联反应,来实现恶唑烷酮及其衍生物的高效合成,反应历程如图所示,已知:Ph为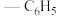 ,Bn为
,Bn为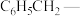 ,Path a为途径a。下列叙述正确的是
,Path a为途径a。下列叙述正确的是
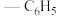 ,Bn为
,Bn为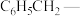 ,Path a为途径a。下列叙述正确的是
,Path a为途径a。下列叙述正确的是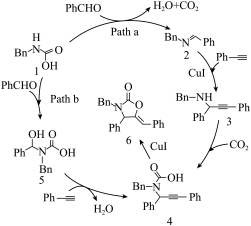
A.总反应的原子利用率为 | B.Path a中 是副产物 是副产物 |
C.Path b断裂了 键和 键和 键 键 | D.产物6的分子中含2个手性碳原子 |
您最近一年使用:0次
3 . 砷化镓是一种高性能半导体材料,被广泛应用于光电子器件等领域。砷化镓立方晶胞(晶胞参数为 )如图1。下列说法正确的是
)如图1。下列说法正确的是
 )如图1。下列说法正确的是
)如图1。下列说法正确的是
A. 的配位数为2 的配位数为2 | B.该晶胞沿z轴方向的平面投影如图2 |
| C.晶体中配位键占共价键总数的25% | D.晶胞中砷原子与镓原子间的最短距离为 |
您最近一年使用:0次
7日内更新
|
556次组卷
|
5卷引用:2024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题
名校
解题方法
4 . 铁及其化合物在生活、生产中有重要应用。回答下列问题:
(1)乳酸亚铁 是一种常用的补铁剂。
是一种常用的补铁剂。
① 的价电子排布图为
的价电子排布图为___________ 。 可用于治疗急性心率衰竭。
可用于治疗急性心率衰竭。
①硝普钠中 的配位数为
的配位数为___________ 。
②硝普钠中不存在的化学键有___________ (填序号)。
a.离子键 b.金属键 c. 配位键 d.极性共价键
(3)咔唑 ( ),)用于制备靶向Fe2+荧光探针,咔唑沸点比
),)用于制备靶向Fe2+荧光探针,咔唑沸点比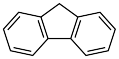 高的主要原因是
高的主要原因是___________ ,咔唑分子中所有原子共平面,咔唑与  都能与
都能与  配位,配位能力: 咔唑
配位,配位能力: 咔唑___________ 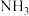 (填"> "、"<"、"=")。
(填"> "、"<"、"=")。
(4)由铁、钾、硒形成的一种超导材料,其晶胞结构和xy平面投影如图所示。___________ 。
②该晶胞参数分别为 a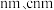 ,该晶体密度
,该晶体密度
___________ 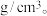 ( 用
( 用  表示阿伏加德罗常数 )
表示阿伏加德罗常数 )
(1)乳酸亚铁
 是一种常用的补铁剂。
是一种常用的补铁剂。①
 的价电子排布图为
的价电子排布图为②乳酸分子( )中
)中  键与
键与  键的数目之比为
键的数目之比为
 可用于治疗急性心率衰竭。
可用于治疗急性心率衰竭。①硝普钠中
 的配位数为
的配位数为②硝普钠中不存在的化学键有
a.离子键 b.金属键 c. 配位键 d.极性共价键
(3)咔唑 (
 ),)用于制备靶向Fe2+荧光探针,咔唑沸点比
),)用于制备靶向Fe2+荧光探针,咔唑沸点比 高的主要原因是
高的主要原因是 都能与
都能与  配位,配位能力: 咔唑
配位,配位能力: 咔唑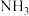 (填"> "、"<"、"=")。
(填"> "、"<"、"=")。(4)由铁、钾、硒形成的一种超导材料,其晶胞结构和xy平面投影如图所示。

②该晶胞参数分别为 a
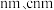 ,该晶体密度
,该晶体密度
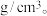 ( 用
( 用  表示阿伏加德罗常数 )
表示阿伏加德罗常数 )
您最近一年使用:0次
5 . 卤族元素单质及其化合物应用广泛。海洋是一个巨大的卤素资源宝库,从海水中能获得NaCl,NaCl的晶胞如下图所示。以NaCl为原料可制得Cl2、HClO、ClO2、 、
、 。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。
。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。
 、
、 。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。
。工业常通过电解NaCl饱和溶液制备Cl2,Cl2氧化卤水中Br-可得到Br2.KClO3酸性溶液中加入H2C2O4可制得黄绿色气体ClO2,该气体常用作自来水消毒剂。F2能与熔融的Na2SO4反应生成硫酰氟(SO2F2)。标况下,氟化氢呈液态。 
| A.HClO呈弱酸性,可用于漂白纸张 |
| B.ClO2具有强氧化性,可用于自来水杀菌消毒 |
C.Cl-有孤电子对,可与 形成 形成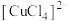 |
| D.HF分子间存在氢键,HF沸点较高 |
您最近一年使用:0次
6 . 下列说法正确的是
A.基态 原子的价电子排布式: 原子的价电子排布式: |
| B.X射线衍射实验中,非晶体会呈现明锐的衍射峰 |
C. 中, 中, 给出孤对电子, 给出孤对电子, 提供空轨道 提供空轨道 |
| D.离子液体是一种常见的等离子体 |
您最近一年使用:0次
名校
7 . 铁合金及其化合物在工业、国防、能源等领域用途广泛。
(1)钛铁合金具有放氢温度低、价格适中等优点,是钛系储氢合金的代表。
①Fe元素在元素周期表中位于第四周期_______ 族,属于_______ 区元素。 )是一种香料的中间体,请画出水杨醛的分子内氢键:
)是一种香料的中间体,请画出水杨醛的分子内氢键:_______ 。
(3)邻二氮菲(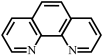 ,平面形分子,简称为phen)能与
,平面形分子,简称为phen)能与 生成稳定的橙色配合物,可测定
生成稳定的橙色配合物,可测定 的浓度,其反应原理如图所示:
的浓度,其反应原理如图所示:__________ 轨道或杂化轨道(只填一种)。
② 中
中 的配位数为
的配位数为_______ 。
③用邻二氮菲测定 的浓度时应控制pH为5~6,请解释原因:
的浓度时应控制pH为5~6,请解释原因:_______ 。
(4)研究发现,用氮化铁作催化材料,对 选择性加氢制烃类具有重要意义。某氮化铁的晶胞结构如图1所示,沿z轴方向的投影如图2所示,A原子的分数坐标为
选择性加氢制烃类具有重要意义。某氮化铁的晶胞结构如图1所示,沿z轴方向的投影如图2所示,A原子的分数坐标为 ,B原子的分数坐标为
,B原子的分数坐标为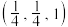 ,则C原子的分数坐标为
,则C原子的分数坐标为_______ (用含b、c的代数式表示);设阿伏加德罗常数的值为 ,该晶体的密度为
,该晶体的密度为_______  (用含a、b、
(用含a、b、 的代数式表示)。
的代数式表示)。
(1)钛铁合金具有放氢温度低、价格适中等优点,是钛系储氢合金的代表。
①Fe元素在元素周期表中位于第四周期
②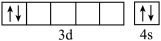 不能正确表示基态钛原子的价电子的电子排布图,因为违背了
不能正确表示基态钛原子的价电子的电子排布图,因为违背了
 )是一种香料的中间体,请画出水杨醛的分子内氢键:
)是一种香料的中间体,请画出水杨醛的分子内氢键:(3)邻二氮菲(
 ,平面形分子,简称为phen)能与
,平面形分子,简称为phen)能与 生成稳定的橙色配合物,可测定
生成稳定的橙色配合物,可测定 的浓度,其反应原理如图所示:
的浓度,其反应原理如图所示: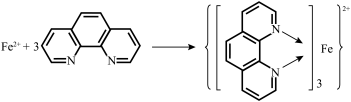
②
 中
中 的配位数为
的配位数为③用邻二氮菲测定
 的浓度时应控制pH为5~6,请解释原因:
的浓度时应控制pH为5~6,请解释原因:(4)研究发现,用氮化铁作催化材料,对
 选择性加氢制烃类具有重要意义。某氮化铁的晶胞结构如图1所示,沿z轴方向的投影如图2所示,A原子的分数坐标为
选择性加氢制烃类具有重要意义。某氮化铁的晶胞结构如图1所示,沿z轴方向的投影如图2所示,A原子的分数坐标为 ,B原子的分数坐标为
,B原子的分数坐标为 ,则C原子的分数坐标为
,则C原子的分数坐标为 ,该晶体的密度为
,该晶体的密度为 (用含a、b、
(用含a、b、 的代数式表示)。
的代数式表示)。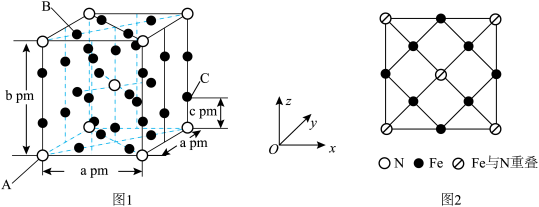
您最近一年使用:0次
名校
解题方法
8 . 以NaOH、 和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下:
和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下: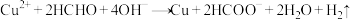
(1)基态Cu原子的价层电子轨道表示式为______
(2)根据反应原理分析
①镀铜反应中,利用了HCHO的______ 性。
②选择HCHO进行化学镀铜的原因之一是它易溶于水。下列分析正确的是______ 。
a.HCHO、 均属于极性分子
均属于极性分子
b.HCHO与 之间能形成氢键
之间能形成氢键
c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的 、HCHO、
、HCHO、 三种微粒,空间结构为平面三角形的是
三种微粒,空间结构为平面三角形的是______ 。
(4)为防止 与
与 形成沉淀,可加入EDTA使
形成沉淀,可加入EDTA使 形成配合物。EDTA能电离出
形成配合物。EDTA能电离出 和
和
 中除部分O外,还能与
中除部分O外,还能与 配位的原子是
配位的原子是______ 。
(5)铜―镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区。Ni位于______ 区。
(6)聚酰亚胺具有高强度、耐紫外线、优良的热氧化稳定性等性质。某聚酰亚胺具有如下结构特征:
①______ 。
②聚酰亚胺在碱性条件下会发生水解。
 和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下:
和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下: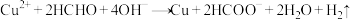
(1)基态Cu原子的价层电子轨道表示式为
(2)根据反应原理分析
①镀铜反应中,利用了HCHO的
②选择HCHO进行化学镀铜的原因之一是它易溶于水。下列分析正确的是
a.HCHO、
 均属于极性分子
均属于极性分子b.HCHO与
 之间能形成氢键
之间能形成氢键c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的
 、HCHO、
、HCHO、 三种微粒,空间结构为平面三角形的是
三种微粒,空间结构为平面三角形的是(4)为防止
 与
与 形成沉淀,可加入EDTA使
形成沉淀,可加入EDTA使 形成配合物。EDTA能电离出
形成配合物。EDTA能电离出 和
和
 (
( )
)
 中除部分O外,还能与
中除部分O外,还能与 配位的原子是
配位的原子是(5)铜―镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区。Ni位于
(6)聚酰亚胺具有高强度、耐紫外线、优良的热氧化稳定性等性质。某聚酰亚胺具有如下结构特征:
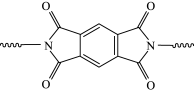
①
②聚酰亚胺在碱性条件下会发生水解。
您最近一年使用:0次
9 . 原子序数依次增大的前四周期元素X、Y、Z、W、T可形成如图所示的化合物。其中仅有Y和Z位于同一周期,且基态Z原子核外有3个未成对电子;W元素形成的单质在常温下为气体;T位于周期表中ds区,其单质在常温下为红色固体。下列说法正确的是

| A.第一电离能:Y>Z>T |
| B.电负性:Z>Y>X |
| C.该化合物中存在配位键,由T提供孤电子对 |
| D.图示结构中的两个六元环和两个五元环均为平面结构 |
您最近一年使用:0次
10 . 乙醇与氢溴酸反应生成一溴乙烷分两步进行:
①乙醇结合氢离子生成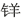 盐中间体:
盐中间体: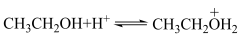
②质子化的羟基以水的形式离去: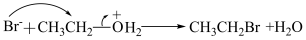
| A.步骤①涉及配位键的形成 |
B.步骤①说明乙醇具有碱性,生成的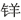 盐具有酸性 盐具有酸性 |
C.一溴乙烷的水解反应中有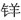 盐中间体生成 盐中间体生成 |
D.碱性强弱顺序: |
您最近一年使用:0次



