名校
1 . 化学是一门以实验为基础的学科,某同学为探究FeCl3溶液的性质进行如下实验,操作如图所示,根据实验现象,下列分析正确的是
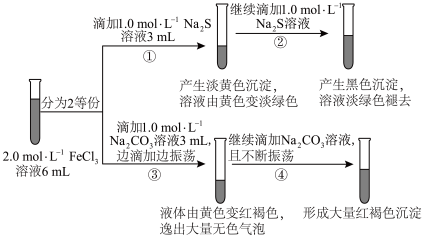

| A.向②后试管加入足量稀盐酸,沉淀全部溶解 |
| B.①~④的变化中,有1处涉及氧化还原反应 |
| C.若将FeCl3溶液滴加到Na2S溶液中,产生的现象与图中①、②现象相同 |
| D.若用Na2SO3代替Na2CO3进行实验,可产生相同现象 |
您最近一年使用:0次
2022-09-15更新
|
835次组卷
|
5卷引用:福建省福清第一中学2023-2024学年高三上学期10月月考化学试题
2 . 某同学用下图所示装置制取氯水并进行相关实验。
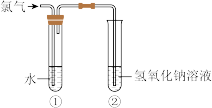
(1)装置②中反应的化学方程式是_______ 。
(2)实验进行一段时间后,装置①中溶液呈黄绿色,说明该溶液中含有的一种物质是(填化学式)_______ 。
(3)下列物质能替代装置②中NaOH溶液的是_______
A.浓硫酸 B.浓FeCl2溶液 C.饱和食盐水
(4)氯水中含有多种成分,因而具有多重性质。将氯水分别加入盛有如图四种物质溶液的试管中,根据发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
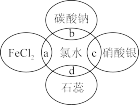
①d过程中溶液先变红后褪色,说明氯水具有的性质是_______ 、_______ 。
②c过程中的现象是_______ 。
③a过程中的化学方程式为_______ 。
④b过程中的离子方程式为_______ 。
(5)欲验证Cl2的氧化性强于I2,取少量氯水加入盛有_______ (填“KI”或“KIO3”)溶液的试管中,用力振荡后加入少量四氯化碳,振荡、静置,观察到的现象是_______ 。

(1)装置②中反应的化学方程式是
(2)实验进行一段时间后,装置①中溶液呈黄绿色,说明该溶液中含有的一种物质是(填化学式)
(3)下列物质能替代装置②中NaOH溶液的是
A.浓硫酸 B.浓FeCl2溶液 C.饱和食盐水
(4)氯水中含有多种成分,因而具有多重性质。将氯水分别加入盛有如图四种物质溶液的试管中,根据发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。

①d过程中溶液先变红后褪色,说明氯水具有的性质是
②c过程中的现象是
③a过程中的化学方程式为
④b过程中的离子方程式为
(5)欲验证Cl2的氧化性强于I2,取少量氯水加入盛有
您最近一年使用:0次
名校
解题方法
3 . 绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。请回答下列问题:
(1)取一定量绿矾配制成 溶液,若绿矾失去部分结晶水,会导致配制的溶液浓度
溶液,若绿矾失去部分结晶水,会导致配制的溶液浓度_______ (填“偏大”“偏小”或“不变”)。
(2)甲组同学取2mL绿矾溶液,加入几滴新制氯水,再加入1滴KSCN溶液,溶液变红,说明 可将
可将 氧化;绿矾溶液与新制氯水反应的离子方程式为
氧化;绿矾溶液与新制氯水反应的离子方程式为_______ 。
(3)乙组同学认为甲组同学的实验不够严谨,该组同学在2mL绿矾溶液中先加入0.5mL煤油,再于液面下依次加入几滴新制氯水和1滴KSCN溶液,溶液变红,煤油的作用是_______ 。
(4)硫酸亚铁加热至高温会分解,生成三种氧化物。为探究硫酸亚铁的分解产物,将无水硫酸亚铁装入反应管A并连接如图所示的装置,打开 和
和 ,缓缓通入
,缓缓通入 ,加热。实验后反应管A中残留的固体为红色粉末
,加热。实验后反应管A中残留的固体为红色粉末
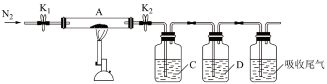
①装置C的溶液为_______ (填标号)。装置D可观察到的实验现象为_______ 。
a.品红 b.NaOH c. d.
d. e.浓硫酸
e.浓硫酸
②写出硫酸亚铁高温分解的化学方程式_______ 。
(1)取一定量绿矾配制成
 溶液,若绿矾失去部分结晶水,会导致配制的溶液浓度
溶液,若绿矾失去部分结晶水,会导致配制的溶液浓度(2)甲组同学取2mL绿矾溶液,加入几滴新制氯水,再加入1滴KSCN溶液,溶液变红,说明
 可将
可将 氧化;绿矾溶液与新制氯水反应的离子方程式为
氧化;绿矾溶液与新制氯水反应的离子方程式为(3)乙组同学认为甲组同学的实验不够严谨,该组同学在2mL绿矾溶液中先加入0.5mL煤油,再于液面下依次加入几滴新制氯水和1滴KSCN溶液,溶液变红,煤油的作用是
(4)硫酸亚铁加热至高温会分解,生成三种氧化物。为探究硫酸亚铁的分解产物,将无水硫酸亚铁装入反应管A并连接如图所示的装置,打开
 和
和 ,缓缓通入
,缓缓通入 ,加热。实验后反应管A中残留的固体为红色粉末
,加热。实验后反应管A中残留的固体为红色粉末
①装置C的溶液为
a.品红 b.NaOH c.
 d.
d. e.浓硫酸
e.浓硫酸②写出硫酸亚铁高温分解的化学方程式
您最近一年使用:0次
2022-08-29更新
|
70次组卷
|
2卷引用:福建省福清虞阳中学2023-2024学年高三上学期第一次综合训练化学试题
4 . 某研究小组设计一种“人体电池”实验装置(如图),进行如下实验。
实验2:两位同学手牵手,一位同学的左手触摸锌片,另一位同学的右手分别触摸铝片、铁片、锡片、铜片。
记录灵敏电流表的读数及指针偏转方向,数据见下表。下列说法正确的是

实验2:两位同学手牵手,一位同学的左手触摸锌片,另一位同学的右手分别触摸铝片、铁片、锡片、铜片。
记录灵敏电流表的读数及指针偏转方向,数据见下表。下列说法正确的是
| 实验时灵敏电流表的读数(微安) | ||||
| 锌-铝 | 锌-铁 | 锌-锡 | 锌-铜 | |
| 实验1 |  | 11 | 17 | a |
| 实验2 |  | 7 | 9 | b |
| A.该人体电池中,锌片作负极,其他金属片均作正极 |
| B.当两手分别触碰锌和铁时,铁片上发生氧化反应 |
| C.实验2的电流均比实验1对应的小,是因为电路中的电阻较大 |
| D.由表格中数据可推测:a<17 |
您最近一年使用:0次
2022-07-06更新
|
355次组卷
|
2卷引用:福建省福州格致中学2022-2023学年高一下学期期末考试化学试题
5 . 某兴趣小组用下图所示实验装置(部分夹持仪器已略去)制取并探究Cl2的性质,装置(I)中发生反应的化学方程式为: 。
。
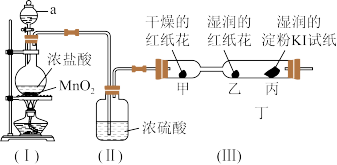
[实验探究]
(1)装置(Ⅰ)中仪器a的名称是_______ 。
(2)装置(Ⅱ)中浓硫酸的作用是_______ 。
(3)实验进行一段时间后,装置(Ⅲ)中的实验现象与分析:
①对甲、乙两处红纸花颜色变化的描述正确的是_______ (填标号)。
A.甲不褪色,乙褪色 B.甲褪色,乙不褪色
②对比甲、乙两处实验现象,可知具有漂白性的物质是_______ (填“Cl2”或“HClO”)。
③丙处淀粉KI试纸变为_______ (填“蓝色”或“红色”),其中Cl2和KI发生反应,补充完整下面的化学方程式: _______。
_______。______
(4)从实验安全和环境保护的角度考虑,该实验存在的一个明显缺陷是_______ 。
(5)用8.7gMnO2固体与足量浓盐酸反应,可生成Cl2气体体积(标准状况下)理论上最多为_______ L。(已知MnO2的摩尔质量为87g/mol)
[知识应用]
Cl2常用于饮用水消毒。Cl2溶于水得到氯水,氯水中HClO的浓度越大杀菌能力越强。
(6)已知25℃时,氯水中Cl2(溶于水的氯气分子)、HClO、 三种微粒所占百分数与pH的关系如图。则用Cl2处理饮用水时,溶液的pH最佳控制范围是
三种微粒所占百分数与pH的关系如图。则用Cl2处理饮用水时,溶液的pH最佳控制范围是_______ (填标号)。

A.3~5.5 B.5.5~7.5
 。
。
[实验探究]
(1)装置(Ⅰ)中仪器a的名称是
(2)装置(Ⅱ)中浓硫酸的作用是
(3)实验进行一段时间后,装置(Ⅲ)中的实验现象与分析:
①对甲、乙两处红纸花颜色变化的描述正确的是
A.甲不褪色,乙褪色 B.甲褪色,乙不褪色
②对比甲、乙两处实验现象,可知具有漂白性的物质是
③丙处淀粉KI试纸变为
 _______。
_______。(4)从实验安全和环境保护的角度考虑,该实验存在的一个明显缺陷是
(5)用8.7gMnO2固体与足量浓盐酸反应,可生成Cl2气体体积(标准状况下)理论上最多为
[知识应用]
Cl2常用于饮用水消毒。Cl2溶于水得到氯水,氯水中HClO的浓度越大杀菌能力越强。
(6)已知25℃时,氯水中Cl2(溶于水的氯气分子)、HClO、
 三种微粒所占百分数与pH的关系如图。则用Cl2处理饮用水时,溶液的pH最佳控制范围是
三种微粒所占百分数与pH的关系如图。则用Cl2处理饮用水时,溶液的pH最佳控制范围是
A.3~5.5 B.5.5~7.5
您最近一年使用:0次
2022-06-11更新
|
211次组卷
|
2卷引用:福建省三明第一中学2022-2023学年高一下学期期中考试化学(学考)试题
6 . 为了探究市售Fe3O4能否与常见的酸(盐酸、稀硫酸)发生反应,实验小组做了以下工作。
Ⅰ.Fe3O4的制备
(1)将可溶性亚铁盐和铁盐按一定配比混合后,加入NaOH溶液,在一定条件下反应可制行Fe3O4,反应的离子方程式为_______ 。
Ⅱ.Fe3O4与酸反应的热力学论证
(2)理论上完全溶解1.16gFe3O4至少需要3 mol/LH2SO4溶液的体积约为_______ mL(保留1位小数)。
(3)查阅文献:吉布斯自由能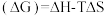 ,在100 kPa下,Fe3O4与酸反应的△G与温度T的关系如图所示。Fe3O4与酸自发反应的温度条件是
,在100 kPa下,Fe3O4与酸反应的△G与温度T的关系如图所示。Fe3O4与酸自发反应的温度条件是_______ 。
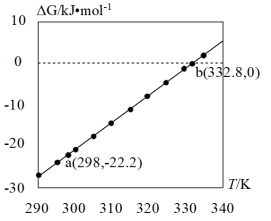
Ⅲ.Fe3O4与酸反应的实验研究
用10 mL3 mol/LH2SO4溶液浸泡1.0 g Fe3O4粉末,5分钟后各取2 mL澄清浸泡液,按编号i进行实验。(所用 、KSCN溶液均为0.1 mol/L,Fe2+遇
、KSCN溶液均为0.1 mol/L,Fe2+遇 溶液生成蓝色沉淀。)
溶液生成蓝色沉淀。)
(4)实验ⅱ的作用是_______ 。
(5)实验ⅰ中滴加K3[Fe(CN)6]溶液无蓝色沉淀生成,其可能原因是Fe2+的浓度太小,为了验证这一推断,可改进的方法是_______ 。
(6)实验ⅲ:用10 mL6 mol/L盐酸代替H2SO4浸泡样品后,重复实验ⅰ,发现试管①有蓝色沉淀,试管②溶液显红色,说明Cl-有利于Fe3O4与H+反应,为了验证这一推测,可在用H2SO4溶液浸泡时加入_______ ,然后重复实验i。
(7)实验ⅳ:用20 mL6 mol/L盐酸浸泡1.0 g天然磁铁矿粉末,20 min后浸泡液几乎无色,重复实验i,发现试管①、②均无明显现象,与实验iii现象不同的可能原因是_______ 。
Ⅰ.Fe3O4的制备
(1)将可溶性亚铁盐和铁盐按一定配比混合后,加入NaOH溶液,在一定条件下反应可制行Fe3O4,反应的离子方程式为
Ⅱ.Fe3O4与酸反应的热力学论证
(2)理论上完全溶解1.16gFe3O4至少需要3 mol/LH2SO4溶液的体积约为
(3)查阅文献:吉布斯自由能
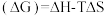 ,在100 kPa下,Fe3O4与酸反应的△G与温度T的关系如图所示。Fe3O4与酸自发反应的温度条件是
,在100 kPa下,Fe3O4与酸反应的△G与温度T的关系如图所示。Fe3O4与酸自发反应的温度条件是
Ⅲ.Fe3O4与酸反应的实验研究
用10 mL3 mol/LH2SO4溶液浸泡1.0 g Fe3O4粉末,5分钟后各取2 mL澄清浸泡液,按编号i进行实验。(所用
 、KSCN溶液均为0.1 mol/L,Fe2+遇
、KSCN溶液均为0.1 mol/L,Fe2+遇 溶液生成蓝色沉淀。)
溶液生成蓝色沉淀。)| 编号 | i | ii |
| 实验操作 | 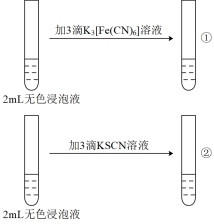 | 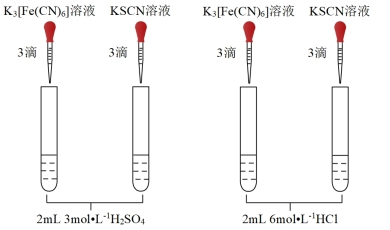 |
| 现象 | ①无蓝色沉淀 ②溶液显红色 | 均无明显现象 |
(5)实验ⅰ中滴加K3[Fe(CN)6]溶液无蓝色沉淀生成,其可能原因是Fe2+的浓度太小,为了验证这一推断,可改进的方法是
(6)实验ⅲ:用10 mL6 mol/L盐酸代替H2SO4浸泡样品后,重复实验ⅰ,发现试管①有蓝色沉淀,试管②溶液显红色,说明Cl-有利于Fe3O4与H+反应,为了验证这一推测,可在用H2SO4溶液浸泡时加入
(7)实验ⅳ:用20 mL6 mol/L盐酸浸泡1.0 g天然磁铁矿粉末,20 min后浸泡液几乎无色,重复实验i,发现试管①、②均无明显现象,与实验iii现象不同的可能原因是
您最近一年使用:0次
2022-05-05更新
|
540次组卷
|
3卷引用:福建省泉州第一中学2023-2024学年高三上学期12月月考化学试题
福建省泉州第一中学2023-2024学年高三上学期12月月考化学试题福建省三明市2022届普通高中毕业班下学期5月质量测试化学试题(已下线)专题17 化学实验综合题-三年(2020-2022)高考真题分项汇编
7 . KMnO4是一种常用的氧化剂。某实验小组利用氯气氧化K2MnO4制备KMnO4并对其性质进行探究。
资料:①锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3 +2H2O=2
+2H2O=2 +MnO2↓+4OH-
+MnO2↓+4OH-
②酸性条件下的氧化性:KMnO4>KIO3>I2
I.KMnO4的制备
(1)从A~D中选择合适的装置制备KMnO4,正确的连接顺序是a→______________ (按气流方向,用小写字母表示);装置A中m的作用是_______ 。

(2)若没有使用装置C,造成的影响是_______ 。
II.KMnO4性质探究
取适量制取的KMnO4溶液稀释至约0.01mol/L(用硫酸酸化至pH=1),取配制好的KMnO4溶液2mL于试管中,逐滴滴加0.1mol/LKI溶液,KMnO4紫色溶液迅速变为棕褐色悬浊液,然后沉淀逐渐消失,最终溶液变为棕黄色。
(3)最终溶液呈现棕黄色推测生成了_______ (写化学式)。
(4)实验小组对初始阶段的产物成分进行探究:

①黑色固体是MnO2,试剂X是_______ (写化学式)。
②在“紫色清液"中存在 ,写出生成
,写出生成 的离子方程式
的离子方程式_______ 。
③下列实验方案中,可用于检验“紫色清液"中是否存在 的是
的是_______ (填序号)。
A.用洁净的玻璃棒随取紫色清液滴在淀粉-KI试纸上,观察试纸是否变蓝色。
B.取少量紫色清液于试管中,向其中加入几滴淀粉溶液,溶液不变蓝,再加入过量NaHSO3溶液,观察溶液是否变色。
C.取少量紫色清液于试管中,向其中加入稀硝酸酸化,再加入几滴硝酸银溶液,观察是否生成黄色沉淀。
(5)探究实验II中棕褐色沉淀消失的原因:

用离子方程式解释步骤③中固体消失的原因_______ 。
(6)由上述实验可知,KMnO4的还原产物与_______ 有关。
资料:①锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3
 +2H2O=2
+2H2O=2 +MnO2↓+4OH-
+MnO2↓+4OH-②酸性条件下的氧化性:KMnO4>KIO3>I2
I.KMnO4的制备
(1)从A~D中选择合适的装置制备KMnO4,正确的连接顺序是a→

(2)若没有使用装置C,造成的影响是
II.KMnO4性质探究
取适量制取的KMnO4溶液稀释至约0.01mol/L(用硫酸酸化至pH=1),取配制好的KMnO4溶液2mL于试管中,逐滴滴加0.1mol/LKI溶液,KMnO4紫色溶液迅速变为棕褐色悬浊液,然后沉淀逐渐消失,最终溶液变为棕黄色。
(3)最终溶液呈现棕黄色推测生成了
(4)实验小组对初始阶段的产物成分进行探究:

①黑色固体是MnO2,试剂X是
②在“紫色清液"中存在
 ,写出生成
,写出生成 的离子方程式
的离子方程式③下列实验方案中,可用于检验“紫色清液"中是否存在
 的是
的是A.用洁净的玻璃棒随取紫色清液滴在淀粉-KI试纸上,观察试纸是否变蓝色。
B.取少量紫色清液于试管中,向其中加入几滴淀粉溶液,溶液不变蓝,再加入过量NaHSO3溶液,观察溶液是否变色。
C.取少量紫色清液于试管中,向其中加入稀硝酸酸化,再加入几滴硝酸银溶液,观察是否生成黄色沉淀。
(5)探究实验II中棕褐色沉淀消失的原因:

用离子方程式解释步骤③中固体消失的原因
(6)由上述实验可知,KMnO4的还原产物与
您最近一年使用:0次
2022-05-03更新
|
932次组卷
|
5卷引用:福建省宁德市五校教学联合体2023届高三一模考试化学试题
福建省宁德市五校教学联合体2023届高三一模考试化学试题(已下线)第3讲 氧化还原反应广东省韶关市2022届高三综合测试(二模)化学试题(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)(已下线)专题17 化学实验综合题-三年(2020-2022)高考真题分项汇编
8 . 某小组设计了如下图所示的实验装置来探究过氧化钠的强氧化性。
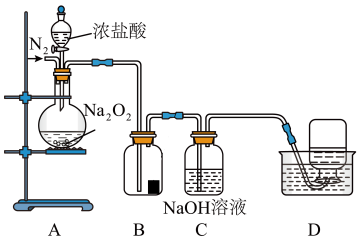
实验步骤及现象如下:
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,停止滴加浓盐酸,再通一段时间N2,直至装置中气体变为无色。
(1)装置D中收集的无色气体X能使带火星的木条复燃,据此推断该气体X是___________ 。
(2)装置B中湿润的淀粉碘化钾试纸变蓝。
甲同学根据A中气体的颜色推测试纸变蓝时发生反应的离子方程式为___________ ;
乙同学认为使试纸变蓝的原因也可能是___________ (填序号)。
a.挥发的HCl气体使试纸变蓝
b.在此实验过程中生成的X气体也能将I-氧化为I2
c.通入的N2使试纸变蓝
(3)C中NaOH溶液的作用是___________ 。
(4)Na2O2与干燥的HCl能发生化学反应生成Cl2、NaCl和H2O,该反应的化学方程式为___________ ,当反应生成标准状况下2.24L Cl2时,转移的电子数为___________ mol。

实验步骤及现象如下:
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,停止滴加浓盐酸,再通一段时间N2,直至装置中气体变为无色。
(1)装置D中收集的无色气体X能使带火星的木条复燃,据此推断该气体X是
(2)装置B中湿润的淀粉碘化钾试纸变蓝。
甲同学根据A中气体的颜色推测试纸变蓝时发生反应的离子方程式为
乙同学认为使试纸变蓝的原因也可能是
a.挥发的HCl气体使试纸变蓝
b.在此实验过程中生成的X气体也能将I-氧化为I2
c.通入的N2使试纸变蓝
(3)C中NaOH溶液的作用是
(4)Na2O2与干燥的HCl能发生化学反应生成Cl2、NaCl和H2O,该反应的化学方程式为
您最近一年使用:0次
2022-01-23更新
|
426次组卷
|
4卷引用:福建师范大学附属中学2022-2023学年高一下学期开学阶段考试化学试题
福建师范大学附属中学2022-2023学年高一下学期开学阶段考试化学试题江苏省无锡市2021-2022学年高一上学期期终教学质量抽测化学试题江苏省盐城市伍佑中学2022-2023学年高一上学期12月月考化学试题(已下线)专题04 氯气及氯的化合物-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)
名校
9 . 取某固体样品,进行如下实验:
①取一定量的样品,加足量水充分溶解,过滤得到白色滤渣和无色溶液
②取白色滤渣,加入稀盐酸,滤渣全部溶解,同时有气体产生
③取①中无色溶液,通入适量 ,产生白色沉淀
,产生白色沉淀
根据上述实验现象,该固体样品的成分可能是
①取一定量的样品,加足量水充分溶解,过滤得到白色滤渣和无色溶液
②取白色滤渣,加入稀盐酸,滤渣全部溶解,同时有气体产生
③取①中无色溶液,通入适量
 ,产生白色沉淀
,产生白色沉淀根据上述实验现象,该固体样品的成分可能是
A. 、 、 、KOH 、KOH | B. 、 、 、NaCl 、NaCl |
C. 、 、 、NaOH 、NaOH | D. 、 、 、NaOH 、NaOH |
您最近一年使用:0次
2022-01-15更新
|
1134次组卷
|
8卷引用:福建省泉州市第九中学 南安市侨光中学2023-2024学年高一上学期12月联考化学试题
解题方法
10 . 某小组同学利用下面的实验装置(气密性已检验)验证稀硝酸的性质。
(1)步骤I中,红棕色气体是 ___________ 。
(2)得出结论:铜与稀硝酸反应生成NO,所依据的实验现象是____________ 。
(3)步骤II中,生成蓝色沉淀的离子方程式是___________ 。
(4)上述实验说明稀硝酸具有的性质是酸性、___________ 。
| 实验装置 | 实验步骤 | 实验现象 |
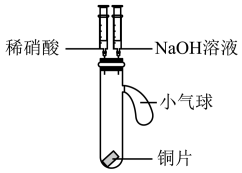 | I.向试管中加入2 mL稀硝酸 | 铜片表面产生无色气泡; 溶液逐渐变为蓝色; 试管上部气体逐渐变为红棕色 |
| II.试管上部气体变为红棕色后, 立即将NaOH溶液加入到试管中 | 溶液中产生蓝色沉淀; 试管上部气体逐渐变为无色 |
(2)得出结论:铜与稀硝酸反应生成NO,所依据的实验现象是
(3)步骤II中,生成蓝色沉淀的离子方程式是
(4)上述实验说明稀硝酸具有的性质是酸性、
您最近一年使用:0次
2021-12-25更新
|
525次组卷
|
2卷引用:福建省福州市福清市虞阳中学2022-2023学年下学期高一年第一次月考化学试卷



