解题方法
1 . I.物质间的转化在生产生活中有着广泛的应用。
A、B、C是中学化学常见的三种物质,它们的相互转化关系如图所示(部分反应条件及产物略去)。
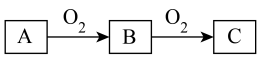
(1)若 是一种活泼金属,
是一种活泼金属, 是淡黄色固体,试用化学方程式表示该物质
是淡黄色固体,试用化学方程式表示该物质 的一个重要应用
的一个重要应用___________ 。将 长期露置于空气中,最后将变成物质
长期露置于空气中,最后将变成物质 的化学式为
的化学式为___________ 。现有 和
和 的固体混合物
的固体混合物 ,加热至质量不再改变,剩余固体质量为
,加热至质量不再改变,剩余固体质量为 的质量分数为
的质量分数为___________ 。
Ⅱ.金属及其化合物在生产生活中有着广泛的应用。
(2)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现___________ 性;___________ (填“能”或“不能”)用氢氧化钠溶液代替。
(3)将 与稀硫酸混合不能反应,但滴入
与稀硫酸混合不能反应,但滴入 后,溶液很快变成蓝色,写出该反应的化学方程式
后,溶液很快变成蓝色,写出该反应的化学方程式___________ 。
(4)利用 溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀掉,从而制作印刷电路板的原理用离子方程式表示为
溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀掉,从而制作印刷电路板的原理用离子方程式表示为___________ 。
A、B、C是中学化学常见的三种物质,它们的相互转化关系如图所示(部分反应条件及产物略去)。

(1)若
 是一种活泼金属,
是一种活泼金属, 是淡黄色固体,试用化学方程式表示该物质
是淡黄色固体,试用化学方程式表示该物质 的一个重要应用
的一个重要应用 长期露置于空气中,最后将变成物质
长期露置于空气中,最后将变成物质 的化学式为
的化学式为 和
和 的固体混合物
的固体混合物 ,加热至质量不再改变,剩余固体质量为
,加热至质量不再改变,剩余固体质量为 的质量分数为
的质量分数为Ⅱ.金属及其化合物在生产生活中有着广泛的应用。
(2)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现
(3)将
 与稀硫酸混合不能反应,但滴入
与稀硫酸混合不能反应,但滴入 后,溶液很快变成蓝色,写出该反应的化学方程式
后,溶液很快变成蓝色,写出该反应的化学方程式(4)利用
 溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀掉,从而制作印刷电路板的原理用离子方程式表示为
溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀掉,从而制作印刷电路板的原理用离子方程式表示为
您最近一年使用:0次
解题方法
2 . 某化学兴趣小组在实验室配制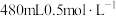 硫酸溶液。回答下列问题:
硫酸溶液。回答下列问题:
(1)在配制溶液时不需要用到的下图仪器是_______ (填字母),配制上述溶液还缺少的玻璃仪器_______ (填仪器名称)。

(2)现用质量分数为98%、密度为 的浓硫酸来配制
的浓硫酸来配制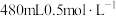 硫酸溶液。所需浓硫酸的体积为
硫酸溶液。所需浓硫酸的体积为_______ mL(保留一位小数)。
(3)配制时,一般可分为以下几个步骤:①量取②计算③稀释④揺匀⑤转移⑥洗涤⑦定容⑧冷却
本实验中正确的操作顺序为_______ →④(填序号,用箭头连接)。
(4)在配制过程中,以下操作会导致所配溶液浓度偏高的是_______(填字母)。
(5)若定容时,加蒸馏水超过刻度线,接下来应采取的措施为_______ 。
(6)用配制好的 的硫酸溶液测定
的硫酸溶液测定 溶液中
溶液中 的物质的量浓度。取
的物质的量浓度。取 该
该 溶液,逐滴滴加
溶液,逐滴滴加 的硫酸溶液,当加入硫酸的体积为
的硫酸溶液,当加入硫酸的体积为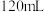 时
时 恰好完全沉淀,则该
恰好完全沉淀,则该 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
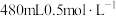 硫酸溶液。回答下列问题:
硫酸溶液。回答下列问题:(1)在配制溶液时不需要用到的下图仪器是

(2)现用质量分数为98%、密度为
 的浓硫酸来配制
的浓硫酸来配制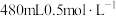 硫酸溶液。所需浓硫酸的体积为
硫酸溶液。所需浓硫酸的体积为(3)配制时,一般可分为以下几个步骤:①量取②计算③稀释④揺匀⑤转移⑥洗涤⑦定容⑧冷却
本实验中正确的操作顺序为
(4)在配制过程中,以下操作会导致所配溶液浓度偏高的是_______(填字母)。
| A.量取浓硫酸时,仰视刻度线 | B.转移前,容量瓶中含有少量蒸馏水 |
| C.转移时,有少量液体溅出 | D.未等溶液恢复至室温就转移到容量瓶中 |
(5)若定容时,加蒸馏水超过刻度线,接下来应采取的措施为
(6)用配制好的
 的硫酸溶液测定
的硫酸溶液测定 溶液中
溶液中 的物质的量浓度。取
的物质的量浓度。取 该
该 溶液,逐滴滴加
溶液,逐滴滴加 的硫酸溶液,当加入硫酸的体积为
的硫酸溶液,当加入硫酸的体积为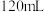 时
时 恰好完全沉淀,则该
恰好完全沉淀,则该 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
解题方法
3 . A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如图所示(部分反应条件及产物略去)。
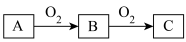
(1)若A是一种黑色单质固体,将一定量C缓慢通入NaOH溶液中,充分反应,测得最后溶液的显碱性,此时溶液的溶质如果是单一成分,可能是___________ 、___________ ;如果是多种成分,可能是___________ 、___________ 。
(2)若A是一种活泼金属,C是淡黄色固体,试用化学方程式表示该物质C的一个重要应用___________ 。将C长期露置于空气中,最后将变成物质D,D的化学式为___________ 。现有D和 的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,D的质量分数为
的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,D的质量分数为___________ 。

(1)若A是一种黑色单质固体,将一定量C缓慢通入NaOH溶液中,充分反应,测得最后溶液的显碱性,此时溶液的溶质如果是单一成分,可能是
(2)若A是一种活泼金属,C是淡黄色固体,试用化学方程式表示该物质C的一个重要应用
 的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,D的质量分数为
的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,D的质量分数为
您最近一年使用:0次
2023-11-30更新
|
107次组卷
|
3卷引用:陕西省西安铁一中滨河高级中学2023-2024学年高一上学期期中考试化学试题
解题方法
4 . 准确称取 铝土矿(含
铝土矿(含 、
、 、
、 )样品,放入盛有
)样品,放入盛有 稀硫酸的烧杯中,充分反应后过滤,向滤液中加入
稀硫酸的烧杯中,充分反应后过滤,向滤液中加入 的
的 溶液,产生沉淀的质量和加入
溶液,产生沉淀的质量和加入 溶液的体积(mL)的关系如图所示
溶液的体积(mL)的关系如图所示
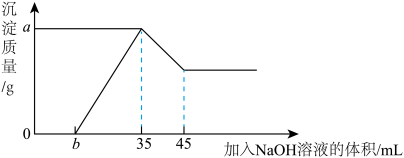
试分析并计算:(写出计算过程)
(1)该铝土矿样品中 的质量分数
的质量分数______
(2)原稀硫酸中 的物质的量浓度
的物质的量浓度______
 铝土矿(含
铝土矿(含 、
、 、
、 )样品,放入盛有
)样品,放入盛有 稀硫酸的烧杯中,充分反应后过滤,向滤液中加入
稀硫酸的烧杯中,充分反应后过滤,向滤液中加入 的
的 溶液,产生沉淀的质量和加入
溶液,产生沉淀的质量和加入 溶液的体积(mL)的关系如图所示
溶液的体积(mL)的关系如图所示
试分析并计算:(写出计算过程)
(1)该铝土矿样品中
 的质量分数
的质量分数(2)原稀硫酸中
 的物质的量浓度
的物质的量浓度
您最近一年使用:0次
名校
解题方法
5 . 小铭所在的化学兴趣小组需要配制1.84 mol·L-1的稀硫酸480 mL,回答下列问题:
(1)需要质量分数为98%,密度为1.84 g·cm-3的浓硫酸_______ mL。
(2)配制时,必须使用的仪器有_______ (填序号),还缺少的仪器是_______ 。
①烧杯②50 mL量筒③100 mL量筒④1 000 mL容量瓶⑤500 mL容量瓶⑥托盘天平(带砝码) ⑦玻璃棒
(3)配制时的操作的顺序是_______ (填字母,下同)。
A.冷却 B.量取 C.洗涤两次 D.定容 E.稀释 F.摇匀 G.转移
(4)下列操作中,容量瓶所不具备的功能有_______。
(5)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”或“不影响”)。
①用量筒量取浓硫酸时,仰视读数:_______ 。
②转移后,没有洗涤烧杯和玻璃棒:_______ 。
③定容时,俯视读数:_______ 。
④定容时,添加蒸馏水超过刻度线后,吸出多余的溶液:_______ 。
(1)需要质量分数为98%,密度为1.84 g·cm-3的浓硫酸
(2)配制时,必须使用的仪器有
①烧杯②50 mL量筒③100 mL量筒④1 000 mL容量瓶⑤500 mL容量瓶⑥托盘天平(带砝码) ⑦玻璃棒
(3)配制时的操作的顺序是
A.冷却 B.量取 C.洗涤两次 D.定容 E.稀释 F.摇匀 G.转移
(4)下列操作中,容量瓶所不具备的功能有_______。
| A.配制一定体积准确浓度的标准溶液 | B.长期贮存溶液 |
| C.用来加热溶解固体溶质 | D.作为反应容器 |
①用量筒量取浓硫酸时,仰视读数:
②转移后,没有洗涤烧杯和玻璃棒:
③定容时,俯视读数:
④定容时,添加蒸馏水超过刻度线后,吸出多余的溶液:
您最近一年使用:0次
2022-12-12更新
|
119次组卷
|
2卷引用:陕西省宝鸡市陈仓区2022-2023学年高一上学期期中检测化学试题
解题方法
6 . 回答下列问题:
(1)从1L 溶液中取出100mL,向其中加入200mL
溶液中取出100mL,向其中加入200mL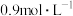 的
的 溶液恰好使
溶液恰好使 完全沉淀,则原溶液中
完全沉淀,则原溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(2)12.4g 含0.4mo
含0.4mo ,则
,则 的摩尔质量为
的摩尔质量为_______ 。
(3)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是_______ 。
(4)由CO2与CO组成的混和气体对H2的相对密度为20,则混和气体中CO2的体积分数为_______ ;CO的质量分数为_______ 。
(1)从1L
 溶液中取出100mL,向其中加入200mL
溶液中取出100mL,向其中加入200mL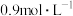 的
的 溶液恰好使
溶液恰好使 完全沉淀,则原溶液中
完全沉淀,则原溶液中 的物质的量浓度为
的物质的量浓度为(2)12.4g
 含0.4mo
含0.4mo ,则
,则 的摩尔质量为
的摩尔质量为(3)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是
(4)由CO2与CO组成的混和气体对H2的相对密度为20,则混和气体中CO2的体积分数为
您最近一年使用:0次
名校
7 . 某种胃药的止酸剂为碳酸钙,测定每片中碳酸钙含量的方法有以下几步操作(设药片中的其它成分不与盐酸反应或氢氧化钠反应):
①配制0.100 稀盐酸和0.100
稀盐酸和0.100 氢氧化钠溶液;
氢氧化钠溶液;
②取一粒药片(0.10g)研碎后加入20.0 蒸馏水;
蒸馏水;
③用0.100 氢氧化钠溶液中和过量的稀盐酸,记录所消耗的体积;
氢氧化钠溶液中和过量的稀盐酸,记录所消耗的体积;
④加入25.0 0.100
0.100 稀盐酸。请回答下列问题:
稀盐酸。请回答下列问题:
(1)测定过程的正确操作顺序为_______________________ (填序号)。
(2)测定过程中发生反应的离子方程式_________________ 、______________________ 。
(3)该测定实验共进行了五次。实验室现有50 、100
、100 、250
、250 、500
、500 4种规格的容量瓶,则配制盐酸应选用的容量瓶的规格为
4种规格的容量瓶,则配制盐酸应选用的容量瓶的规格为_________ ,理由是______________________ 。
(4)某同学4次测定所消耗的 溶液的体积如下:
溶液的体积如下:
请根据这位同学的实验数据,计算药片中碳酸钙的质量分数____________________ 。
①配制0.100
 稀盐酸和0.100
稀盐酸和0.100 氢氧化钠溶液;
氢氧化钠溶液;②取一粒药片(0.10g)研碎后加入20.0
 蒸馏水;
蒸馏水;③用0.100
 氢氧化钠溶液中和过量的稀盐酸,记录所消耗的体积;
氢氧化钠溶液中和过量的稀盐酸,记录所消耗的体积;④加入25.0
 0.100
0.100 稀盐酸。请回答下列问题:
稀盐酸。请回答下列问题:(1)测定过程的正确操作顺序为
(2)测定过程中发生反应的离子方程式
(3)该测定实验共进行了五次。实验室现有50
 、100
、100 、250
、250 、500
、500 4种规格的容量瓶,则配制盐酸应选用的容量瓶的规格为
4种规格的容量瓶,则配制盐酸应选用的容量瓶的规格为(4)某同学4次测定所消耗的
 溶液的体积如下:
溶液的体积如下:测定次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 13.00 | 12.90 | 12.95 | 13.10 | 13.05 |
您最近一年使用:0次
解题方法
8 . 常温下,将20.0 g质量分数为14.0%的KNO3溶液与30.0 g质量分数为24.0%的KNO3溶液混合,得到的密度为1.01 g/cm3的混合溶液。计算:
(1)混合后溶液的质量分数_________ 。
(2)混合后溶液的物质的量浓度_________ 。
(1)混合后溶液的质量分数
(2)混合后溶液的物质的量浓度
您最近一年使用:0次
名校
9 . 实验室里用软锰矿(含MnO2质量分数为60%)与浓盐酸反应来制取适量的氯气,反应方程式如下: (假设HCl全部参加反应,杂质不参与反应)。
(假设HCl全部参加反应,杂质不参与反应)。
(1)用双线桥标出该反应中电子转移的方向和数目_______ 。
(2)若生成5个Cl2分子,计算转移电子总数_______ 。
(3)产生7.1g氯气时,计算所需软锰矿的质量_______ ,被氧化的HCl的质量_______ 。
 (假设HCl全部参加反应,杂质不参与反应)。
(假设HCl全部参加反应,杂质不参与反应)。(1)用双线桥标出该反应中电子转移的方向和数目
(2)若生成5个Cl2分子,计算转移电子总数
(3)产生7.1g氯气时,计算所需软锰矿的质量
您最近一年使用:0次
解题方法
10 . 生活中为了延长鲜花的寿命,通常会在花瓶中加入鲜花保鲜剂。下表是500mL某鲜花保鲜剂中含有的成分及含量:
(1)上述鲜花保鲜剂成分中,属于电解质的是_______ (填序号)。
(2)硫酸钾在水中的电离方程式为_______ 。
(3)“鲜花保鲜剂”中蔗糖的物质的量浓度为_______  。
。
(4)配制该500mL“鲜花保鲜剂”所需的玻璃仪器除了烧杯、玻璃棒、量筒、胶头滴管外,还需要_______ 。
(5)配制溶液过程中,下列操作会使所配结果偏小的是_______(填字母)。
| 成分 | 质量(g) | 摩尔质量(g/mol) |
①蔗糖(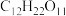 ) ) | 68.4 | 342 |
②硫酸钾( ) ) | 0.5 | 174 |
③高锰酸钾( ) ) | 0.5 | 158 |
④硝酸银( ) ) | 0.04 | 170 |
(2)硫酸钾在水中的电离方程式为
(3)“鲜花保鲜剂”中蔗糖的物质的量浓度为
 。
。(4)配制该500mL“鲜花保鲜剂”所需的玻璃仪器除了烧杯、玻璃棒、量筒、胶头滴管外,还需要
(5)配制溶液过程中,下列操作会使所配结果偏小的是_______(填字母)。
| A.定容时仰视容量瓶刻度线 |
| B.容量瓶在使用前未干燥 |
| C.转移溶液时,溶液不小心从外壁流出 |
| D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理 |
您最近一年使用:0次




