名校
解题方法
1 . 某些化学反应现象能用于制造影视剧中美轮美奂的“仙境”。例如,向置于温热石棉网上的NH4NO3,和Zn粉混合物中滴几滴水后能持续产生白烟,涉及反应:NH4NO3 +Zn ZnO+N2↑+2H2O。下列有关说法中错误的是
ZnO+N2↑+2H2O。下列有关说法中错误的是
 ZnO+N2↑+2H2O。下列有关说法中错误的是
ZnO+N2↑+2H2O。下列有关说法中错误的是| A.ZnO是氧化产物 | B.该反应中NH4NO3只作氧化剂 |
| C.水在反应中可能起催化作用 | D.每生成1 molN2共转移5mol电子 |
您最近一年使用:0次
2023-12-04更新
|
225次组卷
|
5卷引用:湖北省鄂州市部分高中协作体2023-2024学年高一上学期11月期中考试化学试题
名校
解题方法
2 . 请按照要求用对应的化学术语回答下列问题。
(1) 是一种酸式盐,请写出
是一种酸式盐,请写出 在水中的电离方程式
在水中的电离方程式___________ 。
(2)将饱和 溶液滴入到沸水中,继续煮沸至液体变为红褐色,反应的离子方程式为
溶液滴入到沸水中,继续煮沸至液体变为红褐色,反应的离子方程式为___________ 。
(3) 可以作为供氧剂,其与
可以作为供氧剂,其与 反应时若生成标准状况下11.2L
反应时若生成标准状况下11.2L  ,则电子转移数目为
,则电子转移数目为___________ 。
(4) 溶于水可以产生具有漂白性的物质,
溶于水可以产生具有漂白性的物质, 与水反应的离子方程式为:
与水反应的离子方程式为:___________ 。
(5)某温度下将 通入KOH溶液里,反应后得到KCl、KClO、
通入KOH溶液里,反应后得到KCl、KClO、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为11∶1,则
的个数之比为11∶1,则 与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为___________ 。
(6)在标准状况下,将V L氨气溶于0.1L水中,所得溶液的密度为 ,则此氨水的物质的量浓度为
,则此氨水的物质的量浓度为___________  。
。
(1)
 是一种酸式盐,请写出
是一种酸式盐,请写出 在水中的电离方程式
在水中的电离方程式(2)将饱和
 溶液滴入到沸水中,继续煮沸至液体变为红褐色,反应的离子方程式为
溶液滴入到沸水中,继续煮沸至液体变为红褐色,反应的离子方程式为(3)
 可以作为供氧剂,其与
可以作为供氧剂,其与 反应时若生成标准状况下11.2L
反应时若生成标准状况下11.2L  ,则电子转移数目为
,则电子转移数目为(4)
 溶于水可以产生具有漂白性的物质,
溶于水可以产生具有漂白性的物质, 与水反应的离子方程式为:
与水反应的离子方程式为:(5)某温度下将
 通入KOH溶液里,反应后得到KCl、KClO、
通入KOH溶液里,反应后得到KCl、KClO、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为11∶1,则
的个数之比为11∶1,则 与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为(6)在标准状况下,将V L氨气溶于0.1L水中,所得溶液的密度为
 ,则此氨水的物质的量浓度为
,则此氨水的物质的量浓度为 。
。
您最近一年使用:0次
名校
3 .  是新型消毒剂,可以由过硫酸钠(
是新型消毒剂,可以由过硫酸钠( )与
)与 反应制得,下列说法
反应制得,下列说法不正确 的是
 是新型消毒剂,可以由过硫酸钠(
是新型消毒剂,可以由过硫酸钠( )与
)与 反应制得,下列说法
反应制得,下列说法A.该反应的化学方程式为: |
B.每1个 参加反应,得到1个 参加反应,得到1个 |
C. 因具有强氧化性而可以杀菌消毒 因具有强氧化性而可以杀菌消毒 |
D.该实验条件下的氧化性: |
您最近一年使用:0次
2023-10-23更新
|
428次组卷
|
2卷引用:湖北省宜昌市长阳土家族自治县第一高级中学2023-2024学年高一上学期11月期中化学试题
名校
解题方法
4 . 钠及其化合物的叙述错误的是
A. 吸收呼出气体供氧时,每生成1个 吸收呼出气体供氧时,每生成1个 ,转移2个电子 ,转移2个电子 |
| B.碳酸钠水溶液呈碱性,在工业上可用作制作肥皂 |
| C.碳酸钠具有碱性,可用于制胃酸中和剂 |
| D.钠着火需要用干燥的沙土来灭火 |
您最近一年使用:0次
5 . 用尿素水解生成的 催化还原
催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,是柴油机车辆尾气净化的主要方法。反应为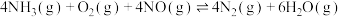 ,下列说法不正确的是
,下列说法不正确的是
 催化还原
催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,是柴油机车辆尾气净化的主要方法。反应为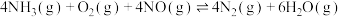 ,下列说法不正确的是
,下列说法不正确的是A.上述反应 |
B.上述反应平衡常数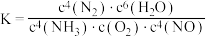 |
C.上述反应中消耗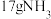 ,转移电子的数目为 ,转移电子的数目为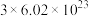 |
| D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气产生的污染越小 |
您最近一年使用:0次
2023-08-08更新
|
311次组卷
|
5卷引用:湖北省重点中学4G+联合体2022-2023学年高二上学期期中考试化学试题
11-12高三上·四川成都·阶段练习
名校
解题方法
6 . 科学研究人员最近发现了一种“水”电池,在海水中电池总反应可表示为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列有关说法正确的是
| A.正极反应式:Ag - e- + Cl- = AgCl |
| B.AgCl是还原产物 |
| C.生成1 mol Na2Mn5O10转移2 mol电子 |
| D.Na+不断向“水”电池的负极移动 |
您最近一年使用:0次
2023-04-26更新
|
134次组卷
|
94卷引用:2016-2017学年湖北省重点高中联考协作体高一下学期期中考试化学试卷
2016-2017学年湖北省重点高中联考协作体高一下学期期中考试化学试卷(已下线)2011-2012学年江西省白鹭洲中学高二上学期期中考试化学(理)试卷(已下线)2011-2012学年浙江省温州中学高二下学期期中考试化学试卷(已下线)2011-2012学年浙江东阳中学、兰溪一中高二下学期期中考试化学卷(已下线)2013-2014湖北省荆州中学高二上学期期末考试化学试卷2014-2015重庆市重庆一中高二上学期期中化学(理)试卷2014-2015江西省白鹭洲中学高一下学期期中考试化学试卷2015-2016学年浙江省绍兴一中高一下期中化学试卷2015-2016学年河北省石家庄市辛集中学高一下期中理科化学试卷2016-2017学年内蒙古鄂尔多斯一中高二上期中化学卷2016-2017学年湖南省娄底市双峰一中等五校高二上期中化学卷湖北省沙市中学、恩施高中、郧阳中学2016-2017学年高一下学期阶段性联考化学试题【全国百强校】北京师范大学附属中学2017-2018学年高一下学期期中考试化学试题福建省莆田市第八中学2018-2019学年高二(理)上学期期中考试化学试题【全国百强校】广西壮族自治区桂林市第十八中学2018-2019学年高一下学期期中段考化学试题【校级联考】浙江省台州市联谊五校2018-2019学年高一下学期期中考试化学试题(已下线)【新东方】高中化学5029浙江省宁波诺丁汉大学附属中学2018-2019学年高一下学期期中考试(实验班)化学试题安徽省淮北市第一中学2019-2020学年高一下学期期中考试化学试题广东省珠海市第二中学2019-2020学年高二上学期期中考试化学试题福建省莆田第十五中学2018-2019学年高二上学期期中考试化学试题福建省莆田第十五中学2019-2020学年高二上学期期中考试化学试题北京市石景山区第九中学2021-2022学年高二上学期期中考试化学试题北京市第一七一中学2021-2022学年高一下学期期中考试化学试题北京市汇文中学2021-2022学年高一下学期期中考试化学试题北京市丰台区2022-2023学年高一下学期期中练习化学试题(已下线)2012届四川省成都外国语学校高三上学期8月月考化学试卷(已下线)2012届山东省枣庄十八中高三10月份质量检测化学试卷(已下线)2011-2012学年福建师大附中高二上学期期末考试化学试卷(已下线)2014高考名师推荐化学原电池的工作原理、电极反应式的书写(已下线)2013-2014云南省玉溪一中高二下学期第二次月考化学试卷2014-2015山东省临沭二中高二1月月考化学试卷2014-2015山西省原平市一中高二上学期期末考试化学试卷2014-2015学年山西省孝义市高一下学期升级考试化学试卷2016届河北省唐山市迁安二中高三上学期期末化学试卷2015-2016学年北大附中河南分校高一下3月月考化学试卷2015-2016学年中国石油天然气管道局中学高一下第二次月考化学试卷2015-2016学年甘肃省天水一中高一下期末理科化学试卷2015-2016学年山东省烟台市招远二中高一下3月月考化学试卷2017届四川省广元市苍溪县高三零诊理综化学试卷2017届四川省双流中学高三12月月考化学卷浙江省名校协作体2016-2017学年高二下学期考试化学试题河北省定州中学2017届高三下学期第二次月考(4月)化学试题2【全国百强校】河北省定州中学2017届高三下学期第二次月考(4月)化学试题天津市南开区2017届高三高考二模化学试卷山西省怀仁县第一中学2016-2017学年高一下学期第三次(5月)月考化学试题江西省南昌市八一中学、洪都中学、麻丘中学等六校2016-2017学年高一5月联考化学试题甘肃省天水市第一中学2016-2017学年高一下学期第二次月考(B卷)化学试题湖南省衡阳市第八中学2016-2017学年高一下学期五科联赛(6月)理综化学试题浙江省金华市东阳中学2016-2017学年高一6月月考化学试题浙江省东阳中学2016-2017学年高一5月月考化学试题浙江省2018版考前特训(2017年10月)学考70快练:原电池河北省鸡泽县第一中学2017-2018学年高二上学期第一次月考化学试题陕西省西安市长安区第一中学2017-2018学年高二上学期第二次月考化学试题福建省晋江市季延中学2018届高三上学期第二阶段检测化学试题北京师范大学附属中学2017-2018学年高二上学期期末考试化学试题【全国校级联考】浙江省宁波市六校2017-2018学年高二下学期期末联考化学试题安徽省宣城市郎溪县郎溪中学2018-2019学年高二上学期返校考化学试题【校级联考】江西省赣州市南康中学、于都中学2018-2019学年高二上学期第三次月考化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二上学期期末考试化学试题(已下线)考点09 原电池原理及其应用——备战2019年浙江新高考化学考点【全国百强校】湖南省衡阳市衡阳县第一中学2018-2019学年高一下学期第一次月考化学试题【全国百强校】江西省新余市第一中学2018-2019学年高一下学期第二次(5月)段考化学试题黑龙江省大庆十中2018-2019学年高一下学期第二次月考化学试题甘肃省玉门一中2018-2019学年高一下学期期末考试化学试题福建省福州市长乐高级中学2020届高三上学期第一次月考化学试题山东省济宁市鱼台县第一中学2020届高三10月月考化学试题湖南省邵东县第一中学、娄底三中2019-2020学年高二上学期第一次月考化学试题湖南省长沙市长沙县第九中学2018-2019学年高二下学期期末考试化学试题云南省武定民族中学2019-2020学年高二上学期期末考试化学试题2020春(新教材)人教化学第二册第6章 化学反应与能量练习课时2 发展中的化学电源——A学习区 夯实基础(人教版必修2)课时3 化学电源——A学习区 夯实基础(鲁科版(2019)第二册)安徽省滁州市明光市明光中学2019-2020高一下学期第二次月考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第四次综合测试化学试题吉林省白城市洮南市第一中学2019-2020学年高一下学期第三次月考化学试题吉林省长春外国语学校2019-2020学年高一下学期期末考试化学(理)试题河南省鹤壁市外国语中学2019-2020学年高一下学期段考化学试题辽宁省六校协作体2020-2021学年高二上学期期初考试化学试题(已下线)第01章 化学反应与能量转化(B卷能力提升篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)山东省滕州市第一中2020-2021学年高二上学期10月月考化学试题鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第2节 化学能转化为电能——电池 课时2 化学电源(已下线)专题讲座(六)新型电源及电极反应式的书写(精练)-2021年高考化学一轮复习讲练测黑龙江宾县第一中学2021届高三上学期第二次月考化学试题山西省运城市临猗县临晋中学2020-2021学年高二上学期12月月考化学试题吉林省前郭尔罗斯蒙古族自治县蒙古族中学2020-2021学年高二上学期期末考试化学试题云南省玉溪市2020-2021学年高一下学期期末教学质量检测化学试题江西省吉安市吉安县第三中学、安福二中2021-2022学年高二入学考试化学试题浙江省磐安县第二中学2019-2020学年高一下学期返校考试化学试题安徽省淮北市第一中学 2021-2022学年高二上学期第一次月考化学试题河北省定州中学2017届高三下学期第二次月考(4月)化学试题1(已下线)第06讲 化学电源-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)山东省实验中学2022-2023学年高二上学期10月月考化学试题山东省威海大光华学校2023-2024学年高二11月月考化学试题
7 . 新冠肺炎期间,化学消毒剂大显身手。高铁酸钾( )是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒。工业制备高铁酸钾的方法主要有湿法和干法两种。实验室模拟湿法制备高铁酸钾的流程如下:
)是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒。工业制备高铁酸钾的方法主要有湿法和干法两种。实验室模拟湿法制备高铁酸钾的流程如下:
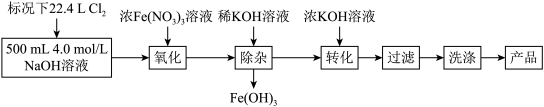
已知:转化过程发生复分解反应。回答下列问题:
(1)NaOH溶液应置于冰水浴中,否则温度升高将发生如下副反应: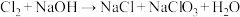 (未配平),请配平该反应
(未配平),请配平该反应_______ 。若有0.15mol 发生该副反应,转移电子的数目为
发生该副反应,转移电子的数目为_______ 。
(2)工业干法制备高铁酸钾的第一步反应为 ,在该反应中还原剂和氧化剂的物质的量之比为
,在该反应中还原剂和氧化剂的物质的量之比为_______ 。
(3)高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂。它能消毒杀菌是因为_______ ,它能净水的原因是_______ 。
(4)由以上信息可知:高铁酸钾的溶解度比高铁酸钠_______ (填“大”或“小”)。
(5)某同学查阅资料得知,最初,人们直接用氯气作漂白剂,但使用起来不方便,效果也不理想。经过多年的实验、改进,才有了今天常用的漂白粉。
①你认为“使用起来不方便,效果也不理想”的原因是_______ 。
②科研人员以氯气、石灰石、水为原料制取漂白粉,有关反应的化学方程式是:_______ 。
 )是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒。工业制备高铁酸钾的方法主要有湿法和干法两种。实验室模拟湿法制备高铁酸钾的流程如下:
)是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒。工业制备高铁酸钾的方法主要有湿法和干法两种。实验室模拟湿法制备高铁酸钾的流程如下:
已知:转化过程发生复分解反应。回答下列问题:
(1)NaOH溶液应置于冰水浴中,否则温度升高将发生如下副反应:
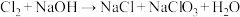 (未配平),请配平该反应
(未配平),请配平该反应 发生该副反应,转移电子的数目为
发生该副反应,转移电子的数目为(2)工业干法制备高铁酸钾的第一步反应为
 ,在该反应中还原剂和氧化剂的物质的量之比为
,在该反应中还原剂和氧化剂的物质的量之比为(3)高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂。它能消毒杀菌是因为
(4)由以上信息可知:高铁酸钾的溶解度比高铁酸钠
(5)某同学查阅资料得知,最初,人们直接用氯气作漂白剂,但使用起来不方便,效果也不理想。经过多年的实验、改进,才有了今天常用的漂白粉。
①你认为“使用起来不方便,效果也不理想”的原因是
②科研人员以氯气、石灰石、水为原料制取漂白粉,有关反应的化学方程式是:
您最近一年使用:0次
8 . 以含硅废石(主要成分为 、含少量
、含少量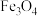 、
、 等杂质)为原料,工业上有以下两种制备高纯硅的工艺。
等杂质)为原料,工业上有以下两种制备高纯硅的工艺。 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃试剂瓶应用橡胶塞的原因是
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃试剂瓶应用橡胶塞的原因是___________ (用离子方程式表示)。
(2)酸浸所得的浸液中含有的金属离子是___________ 。
(3)写出“还原”过程的化学方程式___________ 。当有1 mol C参与反应时,该反应转移的电子数是___________ 。
(4)写出工艺Ⅱ在高温条件下制备纯硅这一步的化学方程式___________ ,工艺Ⅱ与工艺I相比,其优点___________ 。
(5)产品中硅的纯度可以利用Si与NaOH溶液反应产生氢气的体积进行计算,请写出化学方程式___________ 。
 、含少量
、含少量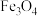 、
、 等杂质)为原料,工业上有以下两种制备高纯硅的工艺。
等杂质)为原料,工业上有以下两种制备高纯硅的工艺。
 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃试剂瓶应用橡胶塞的原因是
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃试剂瓶应用橡胶塞的原因是(2)酸浸所得的浸液中含有的金属离子是
(3)写出“还原”过程的化学方程式
(4)写出工艺Ⅱ在高温条件下制备纯硅这一步的化学方程式
(5)产品中硅的纯度可以利用Si与NaOH溶液反应产生氢气的体积进行计算,请写出化学方程式
您最近一年使用:0次
2023-04-21更新
|
373次组卷
|
2卷引用:湖北省武汉市部分重点中学2022-2023学年高一下学期期中联考化学试题
9 . 自然界的氮循环包括以下过程。下列说法中正确的是


A.氨氧化过程中,亚硝态氮元素与铵态氮元素理论物质的量之比为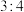 |
| B.硝化过程中,含氮物质均发生还原反应 |
| C.在氨氧化过程中,水体中的氮元素可转移至大气中 |
D. 除去硝态氮生成5.6 L 除去硝态氮生成5.6 L  (标准状况下)时,转移电子数为 (标准状况下)时,转移电子数为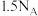 |
您最近一年使用:0次
2023-04-21更新
|
179次组卷
|
2卷引用:湖北省武汉市部分重点中学2022-2023学年高一下学期期中联考化学试题
10 . 每年10月23日上午6:02到晚上6:02被誉为“摩尔日”。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.一定条件下, 与足量的 与足量的 反应,生成 反应,生成 的分子总数为0.5 的分子总数为0.5 |
B.常温常压下,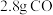 和 和 的混合气体中含有的分子数目为0.1 的混合气体中含有的分子数目为0.1 |
C. 与足量的S反应转移的电子数为0.3 与足量的S反应转移的电子数为0.3 |
D.25℃、 下, 下, 稀有气体混合物中含有的原子总数为 稀有气体混合物中含有的原子总数为 |
您最近一年使用:0次



