1 . 下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素,回答(1)(2)两小问
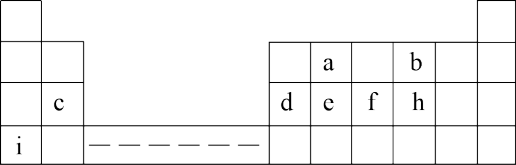
(1)a、b、c三种元素的原子半径由大到小的顺序是___________ (填元素符号);
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是_____ (填水化物的化学式)。
(3)配平下列离子方程式___ __MnO + ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
+ ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
(4)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,写出这一过程的化学方程式:___________ 。

(1)a、b、c三种元素的原子半径由大到小的顺序是
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是
(3)配平下列离子方程式
 + ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
+ ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O(4)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,写出这一过程的化学方程式:
您最近一年使用:0次
2 . 下列物质的性质与用途对应关系正确的是
A. 能与碱反应,可用作食品疏松剂 能与碱反应,可用作食品疏松剂 |
B. 具有还原性,可用于吸收含 具有还原性,可用于吸收含 的尾气 的尾气 |
| C.石墨具有还原性,可用作于电池的正极材料 |
| D.过氧化钠具有强氧化性,可用作漂白剂、消毒剂 |
您最近一年使用:0次
名校
解题方法
3 . 下列物质久置于空气中,均可与空气中某些成分发生化学反应,为确定下列置于空气中的物质是否变质,所选检验试剂(括号内)不能达到目的的是
| A.Na2SO3溶液(BaCl2溶液) | B.KI溶液(淀粉溶液) |
| C.漂白粉(稀盐酸) | D.NaOH溶液[Ba(OH)2 溶液] |
您最近一年使用:0次
名校
4 . 化学还原法是处理含Cr2O 的工业废水常用的方法,主要分为“还原”和“沉淀”两步:
的工业废水常用的方法,主要分为“还原”和“沉淀”两步:
Cr2O
 Cr3+
Cr3+ Cr(OH)3
Cr(OH)3
已知:①Na2S2O5+H2O=2NaHSO3
②“COD”是指化学需氧量,反映了水样中较强还原性物质含量的多少。水中还原性物质越少,则COD越低,表明水质污染程度越小。
(1)取含Cr2O 的工业废水,分别在不同pH条件下,向每个水样中分别加一定量的FeSO4、NaHSO3,搅拌,充分反应,然后滴加Ca(OH)2悬浊液,静置沉淀,测定+6价Cr的去除率,实验结果如图-1所示。
的工业废水,分别在不同pH条件下,向每个水样中分别加一定量的FeSO4、NaHSO3,搅拌,充分反应,然后滴加Ca(OH)2悬浊液,静置沉淀,测定+6价Cr的去除率,实验结果如图-1所示。
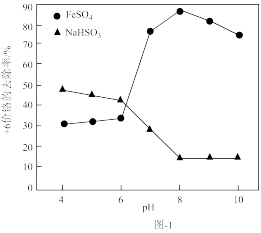
①在酸性条件下,请写出NaHSO3与Cr2O 反应的离子方程式:
反应的离子方程式:___ 。
②分析比较亚铁盐和亚硫酸盐去除+6价Cr的效果。
Ⅰ.亚铁盐在中性和碱性条件下,对+6价Cr的去除效果优于酸性条件下的去除效果,亚硫酸盐则相反;
Ⅱ.___ 。
(2)用焦亚硫酸钠(Na2S2O5)处理废水后,可能会使废水中的COD增大。在焦亚硫酸钠与废水中铬元素不同质量比的情况下,加H2SO4与未加H2SO4处理含铬废水后其COD对比变化如图-2所示。
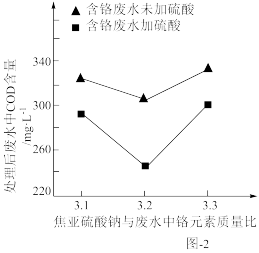
①未加H2SO4时,随着Na2S2O5质量增大,废水COD增大的原因是___ 。
②在焦亚硫酸钠与废水质量比相同的情况下,加H2SO4时,与未加H2SO4相比,废水COD均有所下降,原因可能是___ 。
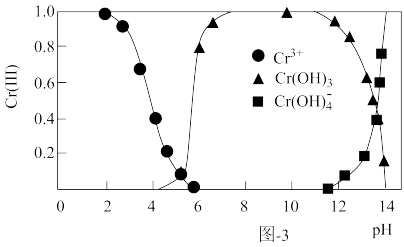
(3)三价铬[Cr(Ⅲ)]在水溶液中的存在形态随pH的变化如图-3所示,为尽可能除去铬元素实现达标排放,沉淀过程中pH要控制在___ ;若pH过高,溶液中残留铬量增大,其原因为___ 。
 的工业废水常用的方法,主要分为“还原”和“沉淀”两步:
的工业废水常用的方法,主要分为“还原”和“沉淀”两步:Cr2O

 Cr3+
Cr3+ Cr(OH)3
Cr(OH)3已知:①Na2S2O5+H2O=2NaHSO3
②“COD”是指化学需氧量,反映了水样中较强还原性物质含量的多少。水中还原性物质越少,则COD越低,表明水质污染程度越小。
(1)取含Cr2O
 的工业废水,分别在不同pH条件下,向每个水样中分别加一定量的FeSO4、NaHSO3,搅拌,充分反应,然后滴加Ca(OH)2悬浊液,静置沉淀,测定+6价Cr的去除率,实验结果如图-1所示。
的工业废水,分别在不同pH条件下,向每个水样中分别加一定量的FeSO4、NaHSO3,搅拌,充分反应,然后滴加Ca(OH)2悬浊液,静置沉淀,测定+6价Cr的去除率,实验结果如图-1所示。
①在酸性条件下,请写出NaHSO3与Cr2O
 反应的离子方程式:
反应的离子方程式:②分析比较亚铁盐和亚硫酸盐去除+6价Cr的效果。
Ⅰ.亚铁盐在中性和碱性条件下,对+6价Cr的去除效果优于酸性条件下的去除效果,亚硫酸盐则相反;
Ⅱ.
(2)用焦亚硫酸钠(Na2S2O5)处理废水后,可能会使废水中的COD增大。在焦亚硫酸钠与废水中铬元素不同质量比的情况下,加H2SO4与未加H2SO4处理含铬废水后其COD对比变化如图-2所示。

①未加H2SO4时,随着Na2S2O5质量增大,废水COD增大的原因是
②在焦亚硫酸钠与废水质量比相同的情况下,加H2SO4时,与未加H2SO4相比,废水COD均有所下降,原因可能是
(3)三价铬[Cr(Ⅲ)]在水溶液中的存在形态随pH的变化如图-3所示,为尽可能除去铬元素实现达标排放,沉淀过程中pH要控制在

您最近一年使用:0次
2020-11-19更新
|
489次组卷
|
5卷引用:江苏省徐州市王杰中学2021届高三12月份阶段性检测化学试题
江苏省徐州市王杰中学2021届高三12月份阶段性检测化学试题江苏省无锡市2021届高三上学期期中考试化学(选修)试题江苏省无锡市2020-2021学年高三上学期期中考试化学试题(已下线)化学-2023年高考押题预测卷01(江苏卷)(含考试版、全解全析、参考答案、答题卡)江苏省前黄高级中学2022-2023学年高三下学期二模适应性考试化学试题



