1 . 下列实验方案不能达到实验目的的是
| A.用过滤法除去NaCl溶液中的泥沙 |
| B.用蒸馏法分离乙酸(沸点118℃)与乙醚(沸点34℃) |
| C.用石灰水鉴别NaHCO3与Na2CO3 |
| D.用盐酸酸化的BaCl2溶液检验Na2SO3是否变质 |
您最近一年使用:0次
名校
解题方法
2 . 填空。
(1)硝酸钙晶体[Ca(NO3)2·4H2O]常用于电子、仪表及冶金工业。一种利用CaO制备Ca(NO3)2·4H2O的流程如下:
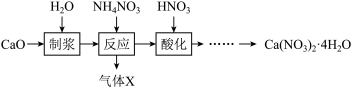
①“制浆”过程中发生反应的化学方程式是___________ 。
②“气体X”的化学式是___________ 。
③Ca(NO3)2·4H2O的溶解度随温度变化的曲线如图所示。
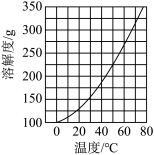
“酸化”后制取Ca(NO3)2·4H2O的操作主要包括加热浓缩、___________ 、过滤、洗涤、干燥。实验室过滤操作必须用到的玻璃仪器有烧杯、玻璃棒和___________ 。
(2)绿矾(FeSO4·7H2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视。
材料一:《唐本草》和《天工开物》等古籍都记载中国很早就能焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色颜料的重要着色剂。
材料二:公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
某研究性学习小组用下图所示试验装置对绿矾的焙烧反应进行探究。
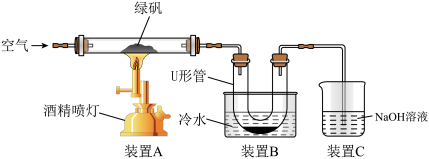
①实验过程中,装置A玻璃管中可观察到的实验现象是___________ 。
②装置C的作用是___________ 。
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入___________ (填试剂名称),溶液呈红色,说明“矾精”中含有H+;检验“矾精”中含有 的方法是
的方法是___________ 。
④某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)160kg,反应原理为:2(FeSO4•7H2O) Fe2O3+SO2+SO3+14H2O,计算理论上所需绿矾的质量,写出计算过程
Fe2O3+SO2+SO3+14H2O,计算理论上所需绿矾的质量,写出计算过程___________ 。
(1)硝酸钙晶体[Ca(NO3)2·4H2O]常用于电子、仪表及冶金工业。一种利用CaO制备Ca(NO3)2·4H2O的流程如下:

①“制浆”过程中发生反应的化学方程式是
②“气体X”的化学式是
③Ca(NO3)2·4H2O的溶解度随温度变化的曲线如图所示。

“酸化”后制取Ca(NO3)2·4H2O的操作主要包括加热浓缩、
(2)绿矾(FeSO4·7H2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视。
材料一:《唐本草》和《天工开物》等古籍都记载中国很早就能焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色颜料的重要着色剂。
材料二:公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
某研究性学习小组用下图所示试验装置对绿矾的焙烧反应进行探究。

①实验过程中,装置A玻璃管中可观察到的实验现象是
②装置C的作用是
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入
 的方法是
的方法是④某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)160kg,反应原理为:2(FeSO4•7H2O)
 Fe2O3+SO2+SO3+14H2O,计算理论上所需绿矾的质量,写出计算过程
Fe2O3+SO2+SO3+14H2O,计算理论上所需绿矾的质量,写出计算过程
您最近一年使用:0次
名校
解题方法
3 . 硫及其化合物有着广泛的作用。硫元素具有多种化合价,在一定条件下能发生相互转化。不同温度下硫单质的状态和分子结构不同,S8环状分子的结构为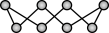 。合理应用和处理含硫的化合物,在生产生活中有重要意义。下列有关硫及其化合物的性质与用途具有对应关系的是
。合理应用和处理含硫的化合物,在生产生活中有重要意义。下列有关硫及其化合物的性质与用途具有对应关系的是
 。合理应用和处理含硫的化合物,在生产生活中有重要意义。下列有关硫及其化合物的性质与用途具有对应关系的是
。合理应用和处理含硫的化合物,在生产生活中有重要意义。下列有关硫及其化合物的性质与用途具有对应关系的是| A.硫单质呈黄色,可用作橡胶硫化剂 |
| B.SO2具有氧化性,可用于漂白草编织物 |
| C.Na2SO3具有还原性,可用于处理自来水中残留的Cl2 |
| D.浓硫酸具有强氧化性,可用作酯化反应的催化剂 |
您最近一年使用:0次
2023-03-23更新
|
696次组卷
|
4卷引用:江苏省连云港高级中学2022-2023学年高二下学期第二次学情检测化学试题
江苏省连云港高级中学2022-2023学年高二下学期第二次学情检测化学试题江苏省苏锡常镇四市2022-2023学年高三下学期教学情况调研(一)(3月)化学试题(已下线)专题05 元素化合物性质(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(选择题6-10)
4 . 含SO2的工业烟气脱硫往往使用较为廉价的碱性物质如生石灰、浓氨水等吸收。近年来一些近海的煤电厂,利用海水的微碱性(8.0≤pH≤8.3)开发海水脱硫新工艺。主要原理是:SO2与海水生成H2SO3,H2SO3电离得到HSO 和SO
和SO 进一步氧化得到SO
进一步氧化得到SO 。脱硫后海水酸性增强,与新鲜海水中的碳酸盐(HCO
。脱硫后海水酸性增强,与新鲜海水中的碳酸盐(HCO 和CO
和CO )发生中和反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。中和反应过程需要鼓入大量空气。下列说法与通入空气作用
)发生中和反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。中和反应过程需要鼓入大量空气。下列说法与通入空气作用无关 的是
 和SO
和SO 进一步氧化得到SO
进一步氧化得到SO 。脱硫后海水酸性增强,与新鲜海水中的碳酸盐(HCO
。脱硫后海水酸性增强,与新鲜海水中的碳酸盐(HCO 和CO
和CO )发生中和反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。中和反应过程需要鼓入大量空气。下列说法与通入空气作用
)发生中和反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。中和反应过程需要鼓入大量空气。下列说法与通入空气作用A.将SO 氧化成为SO 氧化成为SO | B.将产生的CO2赶出水面 |
| C.提高脱硫海水中的含氧量 | D.提高脱硫海水中碳酸盐的浓度 |
您最近一年使用:0次
5 . 含SO2的工业烟气脱硫往往使用较为廉价的碱性物质如生石灰、浓氨水等吸收。近年来一些近海的煤电厂,利用海水的微碱性(8.0≤pH≤8.3)开发海水脱硫新工艺。主要原理是:SO2与海水生成H2SO3,H2SO3电离得到HSO 和SO
和SO 进一步氧化得到SO
进一步氧化得到SO 。脱硫后海水酸性增强,与新鲜海水中的碳酸盐(HCO
。脱硫后海水酸性增强,与新鲜海水中的碳酸盐(HCO 和CO
和CO )发生中和反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。在指定条件下,下列选项所示的物质间转化能实现的是
)发生中和反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。在指定条件下,下列选项所示的物质间转化能实现的是
 和SO
和SO 进一步氧化得到SO
进一步氧化得到SO 。脱硫后海水酸性增强,与新鲜海水中的碳酸盐(HCO
。脱硫后海水酸性增强,与新鲜海水中的碳酸盐(HCO 和CO
和CO )发生中和反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。在指定条件下,下列选项所示的物质间转化能实现的是
)发生中和反应,最终烟气中的SO2大部分以硫酸盐的形式排入大海。在指定条件下,下列选项所示的物质间转化能实现的是A.FeS2(s) 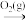 SO3(g) SO3(g) |
B.HSO (aq) (aq) 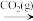 SO2 (g) SO2 (g) |
C.SO2(g)  CaSO3(s) CaSO3(s) |
D.SO2(g)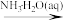 NH4HSO4(aq) NH4HSO4(aq) |
您最近一年使用:0次
解题方法
6 . 认识含硫物质的性质及转化规律,能帮助我们更好地认识自然和保护环境。
(1)酸雨的形成原因。将SO2气体通入蒸馏水中,取出部分溶液并用pH计测定其pH,每隔10min读数一次,所得数据如下:
随着时间的推移,pH逐渐变小的原因是___________ (用化学方程式表示)。
(2)防治SO2对环境的污染。
①从物质分类角度看,SO2属于酸性氧化物。工业上常用熟石灰将SO2转化为亚硫酸盐,写出所得亚硫酸盐的化学式:___________ 。
②从元素价态看,SO2中S元素为+4价,既具有氧化性,又具有还原性。用生物质热解气(主要成分为CO、CH4、H2)可将SO2在高温下还原成单质硫。写出CO还原SO2反应的化学方程式:___________ 。
(3)获取空气质量信息。某化学小组为了测定空气中SO2的体积分数,做了如下实验:取标准状况下的空气20.00L(含N2、O2、CO2、SO2),缓慢通过足量溴水,反应的化学方程式为: 。在所得溶液中加入稍过量的BaCl2溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为4.66g。
。在所得溶液中加入稍过量的BaCl2溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为4.66g。
①检验沉淀是否洗涤干净的方法是___________ 。
②空气样品中SO2的体积分数为___________ 。
(1)酸雨的形成原因。将SO2气体通入蒸馏水中,取出部分溶液并用pH计测定其pH,每隔10min读数一次,所得数据如下:
| 时间(min) | 0 | 10 | 20 | 30 | 40 |
| pH | 4.95 | 4.94 | 4.86 | 4.85 | 4.85 |
随着时间的推移,pH逐渐变小的原因是
(2)防治SO2对环境的污染。
①从物质分类角度看,SO2属于酸性氧化物。工业上常用熟石灰将SO2转化为亚硫酸盐,写出所得亚硫酸盐的化学式:
②从元素价态看,SO2中S元素为+4价,既具有氧化性,又具有还原性。用生物质热解气(主要成分为CO、CH4、H2)可将SO2在高温下还原成单质硫。写出CO还原SO2反应的化学方程式:
(3)获取空气质量信息。某化学小组为了测定空气中SO2的体积分数,做了如下实验:取标准状况下的空气20.00L(含N2、O2、CO2、SO2),缓慢通过足量溴水,反应的化学方程式为:
 。在所得溶液中加入稍过量的BaCl2溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为4.66g。
。在所得溶液中加入稍过量的BaCl2溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为4.66g。①检验沉淀是否洗涤干净的方法是
②空气样品中SO2的体积分数为
您最近一年使用:0次
2021-01-27更新
|
457次组卷
|
3卷引用:江苏省连云港市2020-2021学年高一上学期期末调研考试化学试题
江苏省连云港市2020-2021学年高一上学期期末调研考试化学试题(已下线)专题06 非金属及其化合物-备战2021届高考化学二轮复习题型专练广东省深圳市光明区2022-2023学年高一下学期开学考试化学试题



