名校
1 . 下列物质的转化在给定条件下能实现的是
A.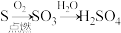 |
B.稀 溶液 溶液 |
C.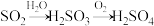 |
D.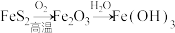 |
您最近一年使用:0次
2 . 下列有关硫及其化合物的性质与用途具有对应关系的是
| A.硫单质呈黄色,可用作橡胶硫化剂 |
B. 具有还原性,可用于漂白草编织物 具有还原性,可用于漂白草编织物 |
C. 具有还原性,可用于处理自来水中残留的 具有还原性,可用于处理自来水中残留的 |
| D.浓硫酸具有强氧化性,可用作酯化反应的催化剂 |
您最近一年使用:0次
名校
解题方法
3 . 工业上制汞的过程是:焙烧辰砂(主要含HgS),发生反应: ,还原出的汞呈气态,冷凝得液态汞。其流程如图,下列说法不正确的是
,还原出的汞呈气态,冷凝得液态汞。其流程如图,下列说法不正确的是
 ,还原出的汞呈气态,冷凝得液态汞。其流程如图,下列说法不正确的是
,还原出的汞呈气态,冷凝得液态汞。其流程如图,下列说法不正确的是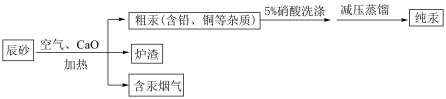
| A.含汞烟气需要经过处理达标后才可以再排放 |
B.在 的反应中,HgS既是还原剂又是氧化剂 的反应中,HgS既是还原剂又是氧化剂 |
| C.洗涤粗汞时不可用5%的硫酸代替5%的硝酸 |
D.流程中加入氧化钙产生的炉渣主要成分是 |
您最近一年使用:0次
名校
解题方法
4 . 某兴趣小组以海藻灰(主要成分是 )为原料进行
)为原料进行 的制备实验。具体步骤如下:将海菜灰浸泡加热过滤后,得到
的制备实验。具体步骤如下:将海菜灰浸泡加热过滤后,得到 溶液,将适量
溶液,将适量 固体溶于
固体溶于 溶液,再将
溶液,再将 饱和溶液滴入上述溶液中,生成白色
饱和溶液滴入上述溶液中,生成白色 ,向白色沉淀中边搅拌边滴入适量浓硝酸得
,向白色沉淀中边搅拌边滴入适量浓硝酸得 。下列有关反应的离子方程式正确的是
。下列有关反应的离子方程式正确的是
 )为原料进行
)为原料进行 的制备实验。具体步骤如下:将海菜灰浸泡加热过滤后,得到
的制备实验。具体步骤如下:将海菜灰浸泡加热过滤后,得到 溶液,将适量
溶液,将适量 固体溶于
固体溶于 溶液,再将
溶液,再将 饱和溶液滴入上述溶液中,生成白色
饱和溶液滴入上述溶液中,生成白色 ,向白色沉淀中边搅拌边滴入适量浓硝酸得
,向白色沉淀中边搅拌边滴入适量浓硝酸得 。下列有关反应的离子方程式正确的是
。下列有关反应的离子方程式正确的是A.生成白色沉淀的反应为: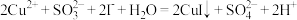 |
B. 固体中加入适量浓硝酸: 固体中加入适量浓硝酸: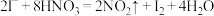 |
C. 中加入过量盐酸: 中加入过量盐酸: |
D. 溶液与氢氧化钡溶液混合: 溶液与氢氧化钡溶液混合: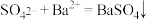 |
您最近一年使用:0次
2024-03-23更新
|
283次组卷
|
3卷引用:江苏省南京市第一中学2023-2024学年高一下学期3月月考化学试题
名校
5 . 利用金属矿渣(含有 、
、 及
及 )制备硫酸亚铁铵[
)制备硫酸亚铁铵[ ]晶体的实验流程如下:
]晶体的实验流程如下: 和
和 转化为
转化为 和CuO。
和CuO。 与
与 反应生成
反应生成 和
和 的化学方程式为
的化学方程式为___________ 。
(2)为提高酸浸过程中铁的浸出率,实验中可采取的措施有___________(填字母)。
(3)由浓硫酸配制250mL“酸浸”所需的1.0 mol/L  溶液,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、
溶液,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、___________ ;检验 是否完全被还原的实验操作是
是否完全被还原的实验操作是___________ 。
(4)煅烧生成的 用石灰乳吸收得到
用石灰乳吸收得到 浆料,以
浆料,以 浆料制备
浆料制备 溶液的实验方案为
溶液的实验方案为___________ 。
已知: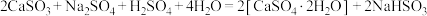 ;
; 难溶于水;pH=4~6溶液中
难溶于水;pH=4~6溶液中 能大量存在。
能大量存在。
实验中可选用的试剂:3mol/L ,3 mol/L
,3 mol/L  ,1 mol/L NaOH。
,1 mol/L NaOH。
 、
、 及
及 )制备硫酸亚铁铵[
)制备硫酸亚铁铵[ ]晶体的实验流程如下:
]晶体的实验流程如下: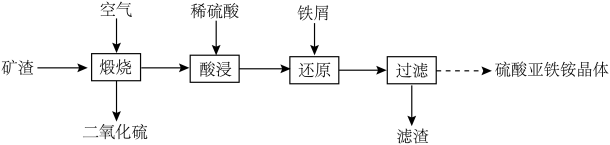
 和
和 转化为
转化为 和CuO。
和CuO。 与
与 反应生成
反应生成 和
和 的化学方程式为
的化学方程式为(2)为提高酸浸过程中铁的浸出率,实验中可采取的措施有___________(填字母)。
| A.增加矿渣投料量 | B.将矿渣粉碎并搅拌 | C.缩短酸浸的时间 | D.适当提高酸浸温度 |
 溶液,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、
溶液,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、 是否完全被还原的实验操作是
是否完全被还原的实验操作是(4)煅烧生成的
 用石灰乳吸收得到
用石灰乳吸收得到 浆料,以
浆料,以 浆料制备
浆料制备 溶液的实验方案为
溶液的实验方案为已知:
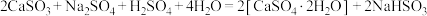 ;
; 难溶于水;pH=4~6溶液中
难溶于水;pH=4~6溶液中 能大量存在。
能大量存在。实验中可选用的试剂:3mol/L
 ,3 mol/L
,3 mol/L  ,1 mol/L NaOH。
,1 mol/L NaOH。
您最近一年使用:0次
2023-09-06更新
|
182次组卷
|
2卷引用:江苏省南京市六校联合体2023-2024学年高三上学期8月调研化学试题
名校
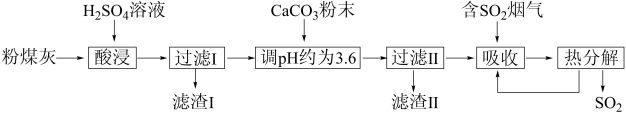
6 . 烟气脱硫能有效减少 的排放。实验室用粉煤灰(主要含
的排放。实验室用粉煤灰(主要含 、
、 等)制备碱式硫酸铝
等)制备碱式硫酸铝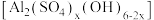 溶液,并用于烟气脱硫。下列说法
溶液,并用于烟气脱硫。下列说法不正确 的是
 的排放。实验室用粉煤灰(主要含
的排放。实验室用粉煤灰(主要含 、
、 等)制备碱式硫酸铝
等)制备碱式硫酸铝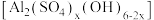 溶液,并用于烟气脱硫。下列说法
溶液,并用于烟气脱硫。下列说法
A.上述过程中,所得滤渣Ⅰ和滤渣II的主要成分分别为 、 、 |
| B.调pH时,若pH偏高,则所得碱式硫酸铝中x将偏小 |
C.碱式硫酸铝溶液吸收 后再热分解放出 后再热分解放出 ,所得溶液中 ,所得溶液中 将减小 将减小 |
D.碱式硫酸铝溶液经多次循环吸收 后,可加入 后,可加入 粉末再生 粉末再生 |
您最近一年使用:0次
2022-06-07更新
|
730次组卷
|
2卷引用:江苏省南京外国语学校、海安中学、金陵中学三校2021-2022学年高三下学期5月联考化学试题
名校
7 . 在澄清溶液中能大量共存的一组离子是
A.Cu2+、SO 、OH-、K+ 、OH-、K+ | B.Fe3+、NO 、Cl-、H+ 、Cl-、H+ |
C.K+、CO 、Cl-、H+ 、Cl-、H+ | D.H+、Na+、ClO-、SO |
您最近一年使用:0次
名校
解题方法
8 . 下列离子方程式表达不正确 的是
A.用氨水吸收废气中的氮氧化物:NO + NO2 + 2OH-=2NO + H2O + H2O |
B.用烧碱溶液除去铝片表面的氧化膜:Al2O3 + 2OH-=2AlO + H2O + H2O |
C.用亚硫酸钠溶液处理纸浆中残氯:SO + 2OH-+ Cl2=2Cl-+ SO + 2OH-+ Cl2=2Cl-+ SO + H2O + H2O |
D.用食醋消除松花蛋中的氨味:CH3COOH + NH3=CH3COO-+ NH |
您最近一年使用:0次
名校
解题方法
9 . Na2S2O3俗称大苏打(海波),是重要的化工原料,无色易溶于水,不溶于乙醇,在中性或碱性环境中稳定,在40~45 ℃熔化,48 ℃分解。实验室用Na2SO3和过量硫粉(不溶于水,可溶于乙醇)在水溶液中加热反应制取Na2S2O3·5H2O晶体【Na2SO3(aq)+S(s)  Na2S2O3(aq)】的步骤如下:
Na2S2O3(aq)】的步骤如下:
① 称取一定量的Na2SO3于烧杯中,溶于水。
② ②另取过量的硫粉,用少许乙醇润湿后,加到上述溶液中。
③ 如图2所示(部分装置略去),水浴加热,微沸,反应后趁热过滤。
④ 滤液在经过相关实验操作后析出Na2S2O3·5H2O晶体。
⑤ 进行减压过滤并低温干燥。
(图1是有关物质的溶解度曲线)
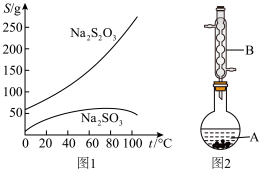
(1) 图2中,仪器B的名称是___________ 。
(2) 实验步骤②中,加入的硫粉用乙醇润湿的目的是___________ 。
(3) 实验步骤③中,趁热过滤的原因是___________ 。
(4) 实验步骤④中,应采取的相关实验操作为___________ 。
(5) 实验步骤⑤中,采用低温干燥的目的是___________ 。
(6) 产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是___________ 。
(7) 准确称取2.00 g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol·L-1碘的标准溶液滴定。反应原理为2S2O +I2=S4O
+I2=S4O +2I-。滴定至终点时,溶液颜色的变化是
+2I-。滴定至终点时,溶液颜色的变化是___________ 。消耗碘的标准溶液体积为36.00 mL,产品的纯度为___________ 。
 Na2S2O3(aq)】的步骤如下:
Na2S2O3(aq)】的步骤如下:① 称取一定量的Na2SO3于烧杯中,溶于水。
② ②另取过量的硫粉,用少许乙醇润湿后,加到上述溶液中。
③ 如图2所示(部分装置略去),水浴加热,微沸,反应后趁热过滤。
④ 滤液在经过相关实验操作后析出Na2S2O3·5H2O晶体。
⑤ 进行减压过滤并低温干燥。
(图1是有关物质的溶解度曲线)

(1) 图2中,仪器B的名称是
(2) 实验步骤②中,加入的硫粉用乙醇润湿的目的是
(3) 实验步骤③中,趁热过滤的原因是
(4) 实验步骤④中,应采取的相关实验操作为
(5) 实验步骤⑤中,采用低温干燥的目的是
(6) 产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是
(7) 准确称取2.00 g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol·L-1碘的标准溶液滴定。反应原理为2S2O
 +I2=S4O
+I2=S4O +2I-。滴定至终点时,溶液颜色的变化是
+2I-。滴定至终点时,溶液颜色的变化是
您最近一年使用:0次
2020-12-28更新
|
301次组卷
|
7卷引用:南京市第二十九中学2021届高三上学期第二次阶段考试化学试题



