名校
解题方法
1 . 在含有大量的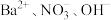 的溶液中,还可能大量共存的离子是
的溶液中,还可能大量共存的离子是
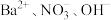 的溶液中,还可能大量共存的离子是
的溶液中,还可能大量共存的离子是A. | B. | C. | D. |
您最近一年使用:0次
2024-01-28更新
|
205次组卷
|
2卷引用:2024年江苏省靖江高级中学学业水平合格性考试化学试题
名校
解题方法
2 . 元素周期表中第ⅥA族元素单质及其化合物有着广泛应用。 、
、 具有杀菌、消毒、漂白等作用。硫磺、黄铁矿(
具有杀菌、消毒、漂白等作用。硫磺、黄铁矿( )可作为工业制硫酸的原料,辉铜矿(
)可作为工业制硫酸的原料,辉铜矿( )煅烧时可发生反应:
)煅烧时可发生反应: 。
。 直接排放会造成环境污染,可将其转化或用石灰乳、
直接排放会造成环境污染,可将其转化或用石灰乳、 等物质进行回收再利用。
等物质进行回收再利用。 与
与 的水溶液反应可制备硒。下列物质性质与应用对应关系正确的是
的水溶液反应可制备硒。下列物质性质与应用对应关系正确的是
 、
、 具有杀菌、消毒、漂白等作用。硫磺、黄铁矿(
具有杀菌、消毒、漂白等作用。硫磺、黄铁矿( )可作为工业制硫酸的原料,辉铜矿(
)可作为工业制硫酸的原料,辉铜矿( )煅烧时可发生反应:
)煅烧时可发生反应: 。
。 直接排放会造成环境污染,可将其转化或用石灰乳、
直接排放会造成环境污染,可将其转化或用石灰乳、 等物质进行回收再利用。
等物质进行回收再利用。 与
与 的水溶液反应可制备硒。下列物质性质与应用对应关系正确的是
的水溶液反应可制备硒。下列物质性质与应用对应关系正确的是A. 有还原性,可用于吸收尾气 有还原性,可用于吸收尾气 | B. 有强氧化性,可用作食品的漂白剂 有强氧化性,可用作食品的漂白剂 |
| C.浓硫酸具有脱水性,可用作酯化反应的催化剂 | D.乙醇是有机溶剂,可用于萃取碘水中的碘单质 |
您最近一年使用:0次
名校
3 . 焦亚硫酸钠 是常用的抗氧化剂,在空气中、受热时均易分解。
是常用的抗氧化剂,在空气中、受热时均易分解。
(1)化学兴趣小组同学利用下图所示装置(部分夹持装置已略去,实验前已除去装置中的空气)制取 并探究
并探究 的性质。
的性质。
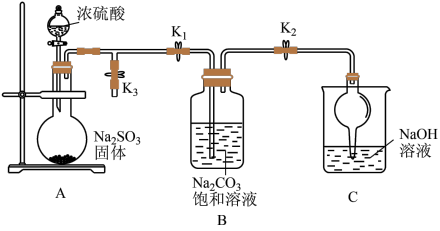
Ⅰ.打开 和
和 ,关闭
,关闭 ,制取
,制取 。
。
① 中O元素化合价为
中O元素化合价为 ,其中S的化合价为
,其中S的化合价为_______ ;装置C中干燥管的作用是_______ 。
②B中通入过量 充分反应后,经冷却结晶时发生反应
充分反应后,经冷却结晶时发生反应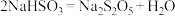 可获得
可获得 晶体。B中生成
晶体。B中生成 的化学方程式为
的化学方程式为_______ 。
③B中所得 晶体常用饱和
晶体常用饱和 水溶液洗涤。用饱和
水溶液洗涤。用饱和 水溶液洗涤的目的除洗去产物表面的杂质离子外还有
水溶液洗涤的目的除洗去产物表面的杂质离子外还有_______ 。
④已知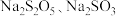 分别与稀硫酸反应得到的产物相同。请设计检验
分别与稀硫酸反应得到的产物相同。请设计检验 样品中是否含
样品中是否含 的实验方案
的实验方案_______ 。
Ⅱ.更换B瓶中的溶液,探究 的性质。
的性质。
⑤将B中溶液更换为品红的乙醇溶液,无明显现象;而将 通入品红的水溶液中,溶液褪色。由此可推知,使品红水溶液褪色的物质可能是
通入品红的水溶液中,溶液褪色。由此可推知,使品红水溶液褪色的物质可能是_______ 。(写化学式)
(2)葡萄酒中常加入 作抗氧化剂。测定某葡萄酒中
作抗氧化剂。测定某葡萄酒中 残留量的实验步骤如下:取
残留量的实验步骤如下:取 葡萄酒样品,用
葡萄酒样品,用 的
的 标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液
标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液 ,已知滴定过程中发生的反应为:
,已知滴定过程中发生的反应为: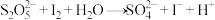 (未配平)。计算该葡萄酒中
(未配平)。计算该葡萄酒中 的残留量
的残留量_______ (以 为单位,写出计算过程)。
为单位,写出计算过程)。
 是常用的抗氧化剂,在空气中、受热时均易分解。
是常用的抗氧化剂,在空气中、受热时均易分解。(1)化学兴趣小组同学利用下图所示装置(部分夹持装置已略去,实验前已除去装置中的空气)制取
 并探究
并探究 的性质。
的性质。
Ⅰ.打开
 和
和 ,关闭
,关闭 ,制取
,制取 。
。①
 中O元素化合价为
中O元素化合价为 ,其中S的化合价为
,其中S的化合价为②B中通入过量
 充分反应后,经冷却结晶时发生反应
充分反应后,经冷却结晶时发生反应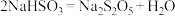 可获得
可获得 晶体。B中生成
晶体。B中生成 的化学方程式为
的化学方程式为③B中所得
 晶体常用饱和
晶体常用饱和 水溶液洗涤。用饱和
水溶液洗涤。用饱和 水溶液洗涤的目的除洗去产物表面的杂质离子外还有
水溶液洗涤的目的除洗去产物表面的杂质离子外还有④已知
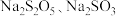 分别与稀硫酸反应得到的产物相同。请设计检验
分别与稀硫酸反应得到的产物相同。请设计检验 样品中是否含
样品中是否含 的实验方案
的实验方案Ⅱ.更换B瓶中的溶液,探究
 的性质。
的性质。⑤将B中溶液更换为品红的乙醇溶液,无明显现象;而将
 通入品红的水溶液中,溶液褪色。由此可推知,使品红水溶液褪色的物质可能是
通入品红的水溶液中,溶液褪色。由此可推知,使品红水溶液褪色的物质可能是(2)葡萄酒中常加入
 作抗氧化剂。测定某葡萄酒中
作抗氧化剂。测定某葡萄酒中 残留量的实验步骤如下:取
残留量的实验步骤如下:取 葡萄酒样品,用
葡萄酒样品,用 的
的 标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液
标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液 ,已知滴定过程中发生的反应为:
,已知滴定过程中发生的反应为: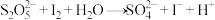 (未配平)。计算该葡萄酒中
(未配平)。计算该葡萄酒中 的残留量
的残留量 为单位,写出计算过程)。
为单位,写出计算过程)。
您最近一年使用:0次
4 . 以卤水(富含I—)为原料用高分子树脂提取碘的工艺流程如图所示,下列说法不正确 的是
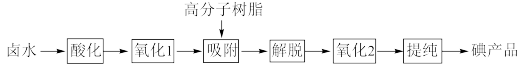
| A.“氧化1”过程既可以用Cl2,也可以用H2O2 |
B.“解脱”用Na2SO3将I2还原为I—,离子方程式为I2+SO +2OH—=2I—+2SO +2OH—=2I—+2SO +H2O +H2O |
| C.用高分子树脂“吸附”,再“解脱”是为了便于分离富集碘元素 |
| D.“提纯”过程先萃取分液、蒸馏得到粗产品,再升华纯化 |
您最近一年使用:0次
5 . SOCl2是一种液态化合物,沸点77℃。向水中滴加8~10滴SOCl2,剧烈反应,液面上有雾形成,并有SO2逸出。待白雾消失后,往溶液中滴加AgNO3溶液,有不溶于HNO3的白色沉淀析出。将SOCl2与AlCl3·6H2O混合加热,可得到无水AlCl3。下列说法错误的是
| A.SOCl2和AlCl3·6H2O的结晶水反应生成HCl抑制AlCl3水解 |
| B.AlCl3的水溶液不导电,不能用于电解制取金属Al |
| C.SO2能使品红溶液褪色,说明SO2具有漂白性 |
| D.SO2的水溶液和氯水放置在空气中一段时间,溶液pH都减小 |
您最近一年使用:0次
6 . 下列物质的性质与用途具有对应关系的是
| A.Al 的金属活泼性强,可用于制作铝金属制品 |
| B.S有氧化性,可用于生产SO2 |
| C.Na2SO3具有还原性,可用于废水脱氯(Cl2) |
| D.NaHCO3受热易分解,可用于制抗酸药物 |
您最近一年使用:0次
2022-01-14更新
|
546次组卷
|
6卷引用:江苏省泰州中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
7 . 已知甲、乙、丙为常见单质,A、B、C、D、E、F、G、H均为常见的化合物;B和乙为淡黄色固体,E的相对式量比D的相对式量大16;F是一种能引起酸雨的气体,有刺激气味;一定条件下,各物质间相互转化关系如图所示(产物中水已忽略)。
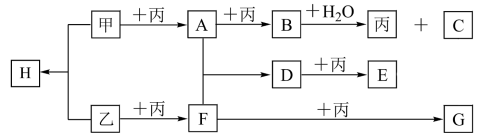
(1)写出下列物质的化学式:丙___ 、B___ 、H___ 。
(2)完成下列转化过程对应的化学方程式:
①B+H2O→丙+C:___ 。
②D+丙→E:___ 。
(3)已知G中含有两种元素且质量比为2∶3,则G的摩尔质量为___ 。

(1)写出下列物质的化学式:丙
(2)完成下列转化过程对应的化学方程式:
①B+H2O→丙+C:
②D+丙→E:
(3)已知G中含有两种元素且质量比为2∶3,则G的摩尔质量为
您最近一年使用:0次
解题方法
8 . 资料显示: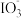 在酸性溶液中能氧化I-,反应为
在酸性溶液中能氧化I-,反应为 +5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。
+5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。
(1)甲同学对这一现象做出如下假设:t秒前生成了I2,但由于存在Na2SO3,I2被消耗,该反应的离子方程式为________ , 的还原性
的还原性________ I-(填“>”“=”或“<”)。
(2)为验证他的猜想,甲同学向反应后的蓝色溶液中加入________ ,蓝色迅速消失,随后再次变蓝。
(3)甲同学设计了如下实验,进一步研究Na2SO3溶液和KIO3溶液反应的过程。
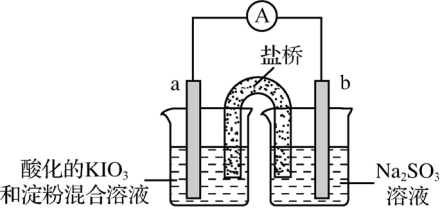
①甲同学在b电极附近的溶液中检测出了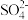
②刚开始放电时,a电极附近溶液未变蓝;取出a电极附近溶液于试管中,溶液变蓝。 在a极放电的产物是
在a极放电的产物是________ 。
③放电一段时间后,a电极附近溶液短暂出现蓝色,随即消失,重复多次后,蓝色不再褪去。电流表显示电路中时而出现电流,时而归零,最终电流消失。电流表短暂归零的原因是________ 。
④下列说法正确的是________ 。
a. a电极附近蓝色不再褪去时, 尚未完全氧化
尚未完全氧化
b. a电极附近短暂出现蓝色,随即消失的原因可能是因为I2被 还原
还原
c. 电流消失后,向b电极附近加入过量Na2SO3溶液,重新产生电流,a电极附近蓝色褪去
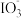 在酸性溶液中能氧化I-,反应为
在酸性溶液中能氧化I-,反应为 +5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。
+5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。(1)甲同学对这一现象做出如下假设:t秒前生成了I2,但由于存在Na2SO3,I2被消耗,该反应的离子方程式为
 的还原性
的还原性(2)为验证他的猜想,甲同学向反应后的蓝色溶液中加入
(3)甲同学设计了如下实验,进一步研究Na2SO3溶液和KIO3溶液反应的过程。

①甲同学在b电极附近的溶液中检测出了
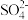
②刚开始放电时,a电极附近溶液未变蓝;取出a电极附近溶液于试管中,溶液变蓝。
 在a极放电的产物是
在a极放电的产物是③放电一段时间后,a电极附近溶液短暂出现蓝色,随即消失,重复多次后,蓝色不再褪去。电流表显示电路中时而出现电流,时而归零,最终电流消失。电流表短暂归零的原因是
④下列说法正确的是
a. a电极附近蓝色不再褪去时,
 尚未完全氧化
尚未完全氧化b. a电极附近短暂出现蓝色,随即消失的原因可能是因为I2被
 还原
还原c. 电流消失后,向b电极附近加入过量Na2SO3溶液,重新产生电流,a电极附近蓝色褪去
您最近一年使用:0次



