名校
解题方法
1 . 硫及其化合物在生产、生活和科学研究中有着广泛的作用。对燃煤烟气脱硫能有效减少对大气的污染并实现资源化利用。方法1用氨水将  先转化为
先转化为 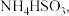 再氧化为
再氧化为 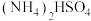 ;方法2用生物质热解气(主要成分为CO、CH4、H2)将
;方法2用生物质热解气(主要成分为CO、CH4、H2)将  在高温下还原为单质硫;方法3用
在高温下还原为单质硫;方法3用  溶液吸收
溶液吸收  生成
生成  ,再加热吸收液,使之重新生成亚硫酸钠;方法4用
,再加热吸收液,使之重新生成亚硫酸钠;方法4用  溶液吸收烟气中
溶液吸收烟气中  ,使用惰性电极电解吸收后的溶液,
,使用惰性电极电解吸收后的溶液, 在阴极被还原为硫单质。可以用
在阴极被还原为硫单质。可以用  溶液除去
溶液除去 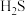 气体,生成黑色
气体,生成黑色  沉淀。下列化学反应表示不正确的是
沉淀。下列化学反应表示不正确的是
 先转化为
先转化为 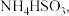 再氧化为
再氧化为 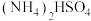 ;方法2用生物质热解气(主要成分为CO、CH4、H2)将
;方法2用生物质热解气(主要成分为CO、CH4、H2)将  在高温下还原为单质硫;方法3用
在高温下还原为单质硫;方法3用  溶液吸收
溶液吸收  生成
生成  ,再加热吸收液,使之重新生成亚硫酸钠;方法4用
,再加热吸收液,使之重新生成亚硫酸钠;方法4用  溶液吸收烟气中
溶液吸收烟气中  ,使用惰性电极电解吸收后的溶液,
,使用惰性电极电解吸收后的溶液, 在阴极被还原为硫单质。可以用
在阴极被还原为硫单质。可以用  溶液除去
溶液除去 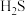 气体,生成黑色
气体,生成黑色  沉淀。下列化学反应表示不正确的是
沉淀。下列化学反应表示不正确的是A.氨水吸收  的反应: 的反应: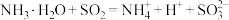 |
B. 还原 还原  的反应:2CO+SO2 的反应:2CO+SO2 S+2CO2 S+2CO2 |
C. 吸收液再生的反应: 吸收液再生的反应: |
D.电解吸收  后的溶液的总反应:3H2SO3 后的溶液的总反应:3H2SO3 S↓+2H2SO4+H2O S↓+2H2SO4+H2O |
您最近一年使用:0次
名校
2 . 室温下,为探究Na2SO3、 NaHSO3 溶液的性质,进行如下实验。
实验 1:测得 0.1mol·L-1NaHSO3 溶液的 pH 约为 5。
实验 2:向 0.1 mol·L -1 Na2SO3 溶液中滴加H2O2,再滴加 BaCl2 溶液,产生白色沉淀。
实验 3:向 0.1 mol·L-1 NaHSO3 中滴加少量 Ba(OH)2 溶液,产生白色沉淀
实验 4:向 0.1mol·L-1Na2SO3溶液中滴加少量酸性KMnO4 溶液,溶液的紫红色褪去。
下列说法正确的是:
实验 1:测得 0.1mol·L-1NaHSO3 溶液的 pH 约为 5。
实验 2:向 0.1 mol·L -1 Na2SO3 溶液中滴加H2O2,再滴加 BaCl2 溶液,产生白色沉淀。
实验 3:向 0.1 mol·L-1 NaHSO3 中滴加少量 Ba(OH)2 溶液,产生白色沉淀
实验 4:向 0.1mol·L-1Na2SO3溶液中滴加少量酸性KMnO4 溶液,溶液的紫红色褪去。
下列说法正确的是:
A.实验 1 中NaHSO3 溶液呈酸性的主要原因是HSO 在水中发生电离,产生了H+ 在水中发生电离,产生了H+ |
B.实验 2 说明SO 被H2O2 氧化生成了SO 被H2O2 氧化生成了SO |
C.实验 3 中发生的离子方程式为:Ba2++SO =BaSO3↓ =BaSO3↓ |
| D.实验 4 说明 Na2SO3溶液具有漂白性 |
您最近一年使用:0次
名校
3 . 下列物质的性质与用途具有对应关系的是
| A.SiO2硬度大,可用于制作光导纤维 |
| B.K2FeO4具有强氧化性,可用于杀菌消毒 |
| C.NaHCO3受热易分解,可用于治疗胃酸 |
| D.Na2SO3溶液呈碱性,可用于污水脱氯(Cl2) |
您最近一年使用:0次
4 . 硫代硫酸钠(Na2S2O3)是常用的分析试剂,也可用作纸浆漂白时的脱氯剂,可由Na2S、Na2SO3为原料制得。实验小组将制取Na2S2O3所用的Na2S进行提纯,然后制取Na2S2O3并对其含量进行了测定。
(1)工业生产Na2S的方法之一是将炭在高温下与Na2SO4反应,所得Na2S固体中含有炭、Na2SO4、Na2SO3、Na2CO3等杂质。实验室所用Na2S可由工业产品净化得到。
①请设计提纯工业Na2S,制取Na2S·9H2O晶体的实验方案:___________ 。(实验中需使用的试剂有BaS溶液,Na2S的溶解度随温度变化曲线、不同温度区间内析出晶体的类型如图1所示)
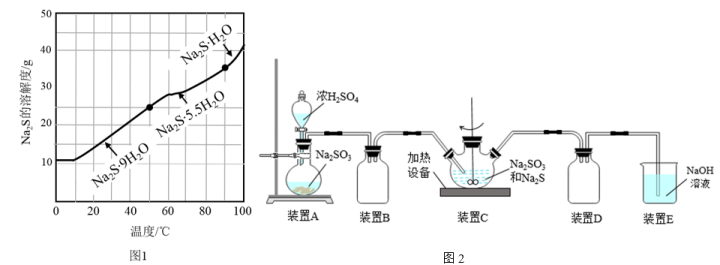
②设计检验工业Na2S产品是否存在Na2SO3的实验方案:___________ 。
(2)实验小组用如图2所示的装置制取Na2S2O3溶液:
①装置C中的反应分为两步,第二步反应为S+Na2SO3=Na2S2O3,则第一反应的化学方程式为___________ 。
②判断装置C中反应已经完全的方法是___________ 。
(3)将装置C反应后的溶液进行结晶,得到Na2S2O3·5H2O晶体样品。用K2Cr2O7标准溶液测定样品的纯度,步骤如下:称取1.5000 g样品,用蒸馏水溶解,配成100 mL溶液。取0.0100 mol·L-1的K2Cr2O7标准溶液20.00 mL,用硫酸酸化后加入过量KI,然后用样品溶液滴定至淡黄绿色,加入淀粉溶液作指示剂,继续滴定,恰好完全反应时消耗样品溶液的体积为20.00 mL。
实验过程中发生的反应为:Cr2O +6I-+14H+=2Cr3++3I2+7H2O I2+2S2O
+6I-+14H+=2Cr3++3I2+7H2O I2+2S2O =S4O
=S4O +2I-
+2I-
①计算样品的纯度。(写出计算过程)___________
②若样品杂质中含有Na2SO3,则所测样品的纯度___________ (填“偏高”、“偏低”或“无影响”)。
(1)工业生产Na2S的方法之一是将炭在高温下与Na2SO4反应,所得Na2S固体中含有炭、Na2SO4、Na2SO3、Na2CO3等杂质。实验室所用Na2S可由工业产品净化得到。
①请设计提纯工业Na2S,制取Na2S·9H2O晶体的实验方案:

②设计检验工业Na2S产品是否存在Na2SO3的实验方案:
(2)实验小组用如图2所示的装置制取Na2S2O3溶液:
①装置C中的反应分为两步,第二步反应为S+Na2SO3=Na2S2O3,则第一反应的化学方程式为
②判断装置C中反应已经完全的方法是
(3)将装置C反应后的溶液进行结晶,得到Na2S2O3·5H2O晶体样品。用K2Cr2O7标准溶液测定样品的纯度,步骤如下:称取1.5000 g样品,用蒸馏水溶解,配成100 mL溶液。取0.0100 mol·L-1的K2Cr2O7标准溶液20.00 mL,用硫酸酸化后加入过量KI,然后用样品溶液滴定至淡黄绿色,加入淀粉溶液作指示剂,继续滴定,恰好完全反应时消耗样品溶液的体积为20.00 mL。
实验过程中发生的反应为:Cr2O
 +6I-+14H+=2Cr3++3I2+7H2O I2+2S2O
+6I-+14H+=2Cr3++3I2+7H2O I2+2S2O =S4O
=S4O +2I-
+2I-①计算样品的纯度。(写出计算过程)
②若样品杂质中含有Na2SO3,则所测样品的纯度
您最近一年使用:0次
名校
5 . 下列物质久置于空气中均会变质,其中发生了氧化还原反应的是
①金属钠 ②过氧化钠 ③硫酸亚铁溶液 ④漂白粉 ⑤亚硫酸钠溶液
①金属钠 ②过氧化钠 ③硫酸亚铁溶液 ④漂白粉 ⑤亚硫酸钠溶液
| A.①②③④⑤ | B.①②③⑤ | C.①③④⑤ | D.①③⑤ |
您最近一年使用:0次
6 . 某固体粉末X中可能含有K2SO4、(NH4)2CO3、K2SO3、NaNO3、Cu2O、FeO、Fe2O3中的若干种。某同学为确定该固体粉末的成分,取X进行如下实验,实验过程及现象如图所示。该同学得出的结论不正确的是( )

已知:Cu2O+2H+=Cu2++Cu+H2O

已知:Cu2O+2H+=Cu2++Cu+H2O
| A.根据现象1无法推出固体粉末中是否含有NaNO3 |
| B.根据现象2可推出白色沉淀是BaSO4 |
| C.根据现象3可推出固体粉末中一定含有K2SO3 |
| D.根据现象4可推出固体粉末中的氧化物只有FeO |
您最近一年使用:0次
2020-07-17更新
|
386次组卷
|
2卷引用:2024届江苏省南通市高三上学期期中考试考前模拟化学试题
名校
解题方法
7 . 氯化亚铜(CuCl) 是一种应用较广的催化剂,有关物质的转化关系如下图所示(除B、E外,均为对应物质的溶液参加反应,部分生成物和反应条件已略去)。其中B 为气体,常用于纸张的漂白; C 为正盐,D 为重要的调味剂,E 为一种红色的金属氧化物,M 溶液常作医用消毒液。
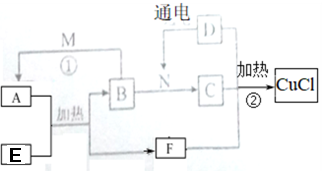
(1)E的化学式______________ ,N的电子式为______________ 。
(2)写出反应①的化学方程式:__________________ 。
(3)写出反应②的离子方程式:_________________ 。

(1)E的化学式
(2)写出反应①的化学方程式:
(3)写出反应②的离子方程式:
您最近一年使用:0次



