名校
解题方法
1 . 实验室由安息香(M=212g/mol)制备二苯乙二酮(M=210g/mol)的反应式如下:
装置示意图如下图所示,实验步骤为:
②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min
③加入50mL水,煮沸后冷却,有黄色固体析出
④过滤,并用冷水洗涤固体3次,得到粗品
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g
回答下列问题:
(1)仪器B的作用是_______ ;冷却水应_______ (填“a”或“b”)口流出。
(2)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是_______ 。
(3)在本实验中,FeCl3为氧化剂且过量,其还原产物为_______ ;某同学尝试改进本实验:
采用催化量的FeCl3并通入空气制备二苯乙二酮,该方法的优点是_______ 。
(4)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是_______ 。
(5)若粗品中混有少量未氧化的安息香,可用少量_______ 洗涤的方法除去(填标号)。
a.冷水 b.热水 c.乙酸 d.乙醇
若要得到更高纯度的产品,可用_______ 的方法进一步提纯。
(6)本实验的产率最接近于_______ (填标号)。
a.85% b.80% c.75% d.70%

| 物质 | 性状 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 安息香 | 白色固体 | 133 | 344 | 难溶于冷水、溶于热水、乙醇、乙酸 |
二苯乙二酮 | 淡黄色固体 | 95 | 347 | 不溶于水、溶于乙醇、苯、乙酸 |
| 冰乙酸 | 无色液体 | 17 | 118 | 与水、乙醇互溶 |

②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min
③加入50mL水,煮沸后冷却,有黄色固体析出
④过滤,并用冷水洗涤固体3次,得到粗品
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g
回答下列问题:
(1)仪器B的作用是
(2)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是
(3)在本实验中,FeCl3为氧化剂且过量,其还原产物为
采用催化量的FeCl3并通入空气制备二苯乙二酮,该方法的优点是
(4)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是
(5)若粗品中混有少量未氧化的安息香,可用少量
a.冷水 b.热水 c.乙酸 d.乙醇
若要得到更高纯度的产品,可用
(6)本实验的产率最接近于
a.85% b.80% c.75% d.70%
您最近一年使用:0次
2 . 定性、定量区分下列有机化合物,用到的化学仪器不正确 的是
| A.质谱仪:2-戊烯和新戊烷 |
| B.红外光谱仪:乙醇和二甲醚 |
| C.核磁共振仪:正丁烷和异丁烷 |
D.现代元素分析仪: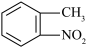 和 和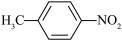 |
您最近一年使用:0次
名校
解题方法
3 . 下列化学用语或图示表达正确的是
A. 的VSEPR模型: 的VSEPR模型: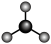 |
B.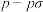 键电子云轮廓图: 键电子云轮廓图: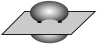 |
C. 的空间结构示意图为 的空间结构示意图为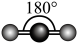 |
D.氨气分子中氮原子的杂化轨道表示式: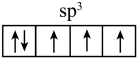 |
您最近一年使用:0次
名校
解题方法
4 . 关于有机物检测,下列说法不正确 的是
| A.1-溴丁烷中的溴元素检验所需的试剂:NaOH溶液、稀硝酸和硝酸银溶液 |
| B.通过核磁共振氢谱检测CH3OCOOCH3,谱图上呈现两组峰 |
| C.用饱和溴水可鉴别1-己烯、2-氯丙烷、丙醛和苯酚溶液 |
| D.用新制氢氧化铜(可加热)可鉴别乙醛、乙醇、苯 |
您最近一年使用:0次
5 . 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂。
(1)写出A、B、D、E的结构简式:A___________ ,B___________ ,D___________ ,F___________ 。
(2)A能发生聚合反应,其产物为E,E的结构简式为___________ 。
(3)写出②反应的化学反应方程式以及反应类型:②___________ ;反应类型___________ 。
(4)D可以在铜或者银的催化下,逐步氧化,请写出D氧化为F的化学反应方程式以及反应类型:D→F___________ ;反应类型___________ 。
(5)写出D和G生成H的化学反应方程式:D+G→H___________ 。
(6)反应②⑤均可制氯乙烷,反应___________ 最好(填反应序号),原因是___________ 。
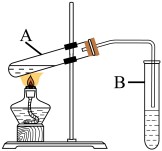
(7)反应D+G→H的实验装置如图所示,试管B中在反应前加入的是___________ 。
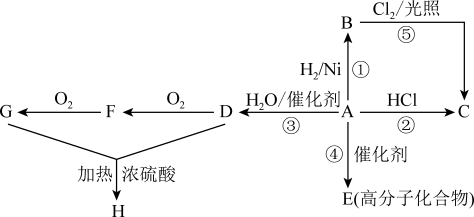
(1)写出A、B、D、E的结构简式:A
(2)A能发生聚合反应,其产物为E,E的结构简式为
(3)写出②反应的化学反应方程式以及反应类型:②
(4)D可以在铜或者银的催化下,逐步氧化,请写出D氧化为F的化学反应方程式以及反应类型:D→F
(5)写出D和G生成H的化学反应方程式:D+G→H
(6)反应②⑤均可制氯乙烷,反应
(7)反应D+G→H的实验装置如图所示,试管B中在反应前加入的是
您最近一年使用:0次
6 . 下列设备工作时,将化学能转化为电能的是
|
|
|
|
| A.硅太阳能电池 | B.锂离子电池 | C.太阳能集热器 | D.燃气灶 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 某有机物的结构简式如图所示,则下列说法中不正确的是
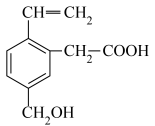
A.该有机物既能与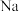 反应,还能与 反应,还能与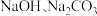 反应 反应 |
| B.该有机物中有3种官能团 |
| C.该有机物在一定条件下能发生加成、加聚、取代、氧化等反应 |
D. 该有机物和足量金属钠反应生成 该有机物和足量金属钠反应生成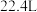 气体 气体 |
您最近一年使用:0次
8 . 下列反应过程中的能量变化情况符合图像的是
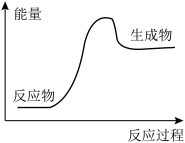
| A.乙醇的燃烧 | B.Ba(OH)2·8H2O与NH4Cl反应 |
| C.镁和盐酸的反应 | D.酸和碱的中和反应 |
您最近一年使用:0次
名校
9 . 化学电源在日常生活和高科技领域中都有广泛应用,下列说法错误的是

A.图I: 向Fe电极方向移动 向Fe电极方向移动 |
| B.图II:锌作负极反应物,发生氧化反应 |
| C.图III:电池放电过程中,负极质量不断减少,正极质量不断增加 |
D.图IV:正极的电极反应式为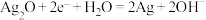 |
您最近一年使用:0次
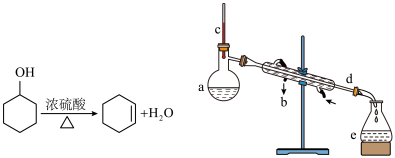
10 . 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置(省略加热和部分夹持装置)如图:
合成反应:在a中加入20g环己醇和少量碎瓷片,在搅动下慢慢加入1mL浓 ;控制馏出物的温度不超过90℃。
;控制馏出物的温度不超过90℃。
分离、提纯:反应得到的粗产物倒入分液漏斗中,分别用少量5%的碳酸钠溶液和蒸馏水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到10g纯净环己烯。
回答下列问题:
(1)装置b的名称是______ 。
(2)加入碎瓷片的作用是______ ,在合成步骤中,应按照______ 的顺序操作(填入序号)
A.先向b中通入冷却水,再开始缓慢加热a B.先开始缓慢加热a,再向b中通入冷却水
(3)分液漏斗在使用前须清洗干净并______ ,在本实验分离过程中,产物应该从分液漏斗的______ (填“上口倒出”或“下口放出”)。
(4)分离、提纯过程中加入无水氯化钙的目的是______ 。
性质物质 | 相对分子质量 | 沸点/℃ | 密度/ | 溶解性 |
环己醇 | 100 | 161 | 0.9618 | 微溶于水 |
环己烯 | 82 | 83 | 0.8102 | 难溶于水 |
 ;控制馏出物的温度不超过90℃。
;控制馏出物的温度不超过90℃。分离、提纯:反应得到的粗产物倒入分液漏斗中,分别用少量5%的碳酸钠溶液和蒸馏水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到10g纯净环己烯。
回答下列问题:
(1)装置b的名称是
(2)加入碎瓷片的作用是
A.先向b中通入冷却水,再开始缓慢加热a B.先开始缓慢加热a,再向b中通入冷却水
(3)分液漏斗在使用前须清洗干净并
(4)分离、提纯过程中加入无水氯化钙的目的是
您最近一年使用:0次








