名校
1 . 下列选项中,所示物质间转化(题中箭头表示一步转化) 不能实现的是
| A.Si→SiO₂→H₂SiO₃ | B.Fe→FeCl₂→Fe(OH)₂ | C.N₂→NO→HNO₃ | D.NaCl→NaHCO₃→Na₂CO₃ |
您最近一年使用:0次
2024-01-31更新
|
247次组卷
|
2卷引用:重点 天津市第五中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
2 . 下列化学用语的表达正确的是
A.HCl分子中 键的形成: 键的形成: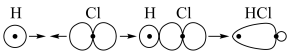 |
B.邻羟基苯甲醛的分子内氢键: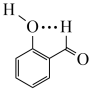 |
C.用电子式表示 的形成: 的形成: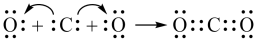 |
D.用轨道表示式表示石墨烯中C原子的杂化: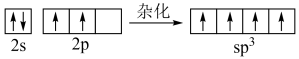 |
您最近一年使用:0次
2024-01-25更新
|
247次组卷
|
2卷引用:天津市静海区第一中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
3 . 某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:

请回答下列问题:
(1)用18.4 mol·L-1的浓硫酸,配制100 mL 1mol·L-1的硫酸溶液,所需浓硫酸的体积为___________ mL(计算结果精确到小数点后一位)。
(2)在下列配制过程示意图中,有错误的是(填写序号)___________ 。
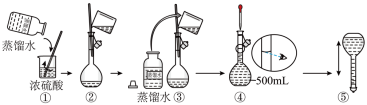
(3)下列说法正确的___________。
(4)验证步骤②反应后的溶液中是否含Fe2+,下列检验试剂选用正确的是___________ 。
A.用氯水、KSCN溶液检验是否有Fe2+
B.用酸性KMnO4溶液检验是否有Fe2+
C.用NaOH溶液检验是否有Fe2+
(5)步骤②加入过量H2O2发生反应的离子方程式为:___________ 。
(6)若称得固体的质量为a g,则每片补血剂中含硫酸亚铁的质量为___________ g。

请回答下列问题:
(1)用18.4 mol·L-1的浓硫酸,配制100 mL 1mol·L-1的硫酸溶液,所需浓硫酸的体积为
(2)在下列配制过程示意图中,有错误的是(填写序号)

(3)下列说法正确的___________。
| A.洗涤烧杯2至3次,并将洗涤液移入容量瓶以减少误差 |
| B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低 |
| C.定容时仰视观察,所配溶液浓度会偏低 |
| D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可 |
A.用氯水、KSCN溶液检验是否有Fe2+
B.用酸性KMnO4溶液检验是否有Fe2+
C.用NaOH溶液检验是否有Fe2+
(5)步骤②加入过量H2O2发生反应的离子方程式为:
(6)若称得固体的质量为a g,则每片补血剂中含硫酸亚铁的质量为
您最近一年使用:0次
解题方法
4 . 请回答下列问题:
Ⅰ.已知: 和HClO的电离平衡常数(25℃)如下:
和HClO的电离平衡常数(25℃)如下:
(1)相同物质的量浓度的 、
、 、NaClO溶液,pH由小到大的顺序是
、NaClO溶液,pH由小到大的顺序是___________ 。
(2)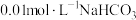 的溶液中
的溶液中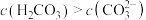 ,结合化学用语解释其原因:
,结合化学用语解释其原因:___________ 。
(3)请写出NaClO溶液中通入少量二氧化碳的离子方程式___________ 。
(4)盐碱地(含有较多的NaCl、 )不利于农作物生长,通过施加适量的石膏可以降低土壤的碱性。试用离子方程式表示盐碱地呈碱性的原因
)不利于农作物生长,通过施加适量的石膏可以降低土壤的碱性。试用离子方程式表示盐碱地呈碱性的原因___________ ,用石膏降低其碱性的反应原理___________ (用离子方程式及必要的文字说明)。
(5)根据酸碱质子理论,给出质子( )的物质是酸,给出质子的能力越强,酸性越强。已知:
)的物质是酸,给出质子的能力越强,酸性越强。已知: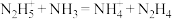 ,
, ,写出上述物质的酸性由强到弱的顺序
,写出上述物质的酸性由强到弱的顺序___________ 。
Ⅱ.在粗制 晶体中常含有杂质
晶体中常含有杂质 。在提纯时,为了除去
。在提纯时,为了除去 ,常加入少量
,常加入少量 ,使
,使 氧化为
氧化为 ,然后调节溶液pH=4,可以达到除去
,然后调节溶液pH=4,可以达到除去 而不损失的目的。
而不损失的目的。
(6)通过计算解释原因___________ (已知:①25℃时 饱和溶液中
饱和溶液中 。②25℃时
。②25℃时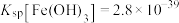 ,
,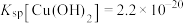 )。
)。
(7)计算过程:___________ 。
Ⅰ.已知:
 和HClO的电离平衡常数(25℃)如下:
和HClO的电离平衡常数(25℃)如下:| 化学式 |  | HClO |
电离平衡常数( ) ) |   |  |
 、
、 、NaClO溶液,pH由小到大的顺序是
、NaClO溶液,pH由小到大的顺序是(2)
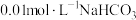 的溶液中
的溶液中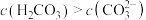 ,结合化学用语解释其原因:
,结合化学用语解释其原因:(3)请写出NaClO溶液中通入少量二氧化碳的离子方程式
(4)盐碱地(含有较多的NaCl、
 )不利于农作物生长,通过施加适量的石膏可以降低土壤的碱性。试用离子方程式表示盐碱地呈碱性的原因
)不利于农作物生长,通过施加适量的石膏可以降低土壤的碱性。试用离子方程式表示盐碱地呈碱性的原因(5)根据酸碱质子理论,给出质子(
 )的物质是酸,给出质子的能力越强,酸性越强。已知:
)的物质是酸,给出质子的能力越强,酸性越强。已知: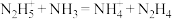 ,
, ,写出上述物质的酸性由强到弱的顺序
,写出上述物质的酸性由强到弱的顺序Ⅱ.在粗制
 晶体中常含有杂质
晶体中常含有杂质 。在提纯时,为了除去
。在提纯时,为了除去 ,常加入少量
,常加入少量 ,使
,使 氧化为
氧化为 ,然后调节溶液pH=4,可以达到除去
,然后调节溶液pH=4,可以达到除去 而不损失的目的。
而不损失的目的。(6)通过计算解释原因
 饱和溶液中
饱和溶液中 。②25℃时
。②25℃时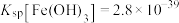 ,
,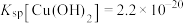 )。
)。(7)计算过程:
您最近一年使用:0次
名校
解题方法
5 . 在 时,对
时,对 浓度均为
浓度均为 盐酸和醋酸的混合溶液进行如下操作。下列说法正确的是
盐酸和醋酸的混合溶液进行如下操作。下列说法正确的是
 时,对
时,对 浓度均为
浓度均为 盐酸和醋酸的混合溶液进行如下操作。下列说法正确的是
盐酸和醋酸的混合溶液进行如下操作。下列说法正确的是A.加入少量 固体,溶液中 固体,溶液中 将减小 将减小 |
B.加入 相同浓度的 相同浓度的 溶液,所得溶液 溶液,所得溶液 |
C.加入 溶液,若所得溶液 溶液,若所得溶液 ,则水电离的 ,则水电离的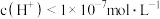 |
D.加入 相同浓度的 相同浓度的 溶液,若忽略混合时的体积变化,此时溶液中: 溶液,若忽略混合时的体积变化,此时溶液中: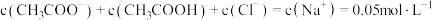 |
您最近一年使用:0次
2024-01-22更新
|
853次组卷
|
6卷引用:天津市河东区2024年高三下学期一模考试化学试题
天津市河东区2024年高三下学期一模考试化学试题2024年1月贵州普通高等学校招生考试适应性测试化学试题(已下线)2024年1月“九省联考”贵州卷真题完全解读与考后提升(已下线)选择题11-14(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)重庆市第八中学2023-2024学年高二下学期第一次月考化学试卷
6 . 下列实验操作、现象和结论均正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 分别向等量乙醇和水中加入绿豆大的钠,钠与水反应更剧烈 | 水分子中的氢原子比乙醇羟基中的氢原子活泼 |
| B | 向某稀溶液中加入NaOH溶液,能产生使湿润的蓝色石蕊试纸变红的气体 | 溶液中含有 |
| C | 向葡萄糖溶液中加入少量NaOH溶液和CuSO4溶液,产生砖红色沉淀 | 新制Cu(OH)2可检验葡萄糖 |
| D | 向少量酸性KMnO4溶液中滴加少量FeCl2溶液,再滴加2滴KSCN溶液,溶液先褪色后变红 | Fe2+具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-22更新
|
993次组卷
|
5卷引用:天津市河东区2024年高三下学期一模考试化学试题
天津市河东区2024年高三下学期一模考试化学试题2024年1月贵州普通高等学校招生考试适应性测试化学试题(已下线)2024年1月“九省联考”贵州卷真题完全解读与考后提升(已下线)选择题6-10(已下线)热点08 表格型实验方案的设计与评价
7 . Ⅰ.次磷酸 具有较强的还原性,可用于制药工业。
具有较强的还原性,可用于制药工业。
(1) 是一元酸,25℃时,
是一元酸,25℃时, 。写出其电离方程式:
。写出其电离方程式:___________ 。
(2)用电渗析法制备 的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
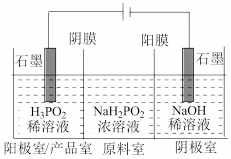
①写出阴极的电极反应:___________ 。
② 的移动方向是:
的移动方向是: 移向
移向___________ (填“阴极室”或“原料室”)。
③阳极室得到 ,
, 的浓度逐渐增大。
的浓度逐渐增大。
a.结合电极反应说明其原因是___________ 。
b.该方法得到的产品 溶液中会混有
溶液中会混有 。产生
。产生 的原因是
的原因是___________ 。
Ⅱ.氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(3)298K时, 燃烧生成
燃烧生成 放热121kJ,
放热121kJ,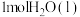 蒸发吸热44kJ,表示
蒸发吸热44kJ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
(4)氢氧燃料电池中氢气在___________ (填“正”或“负”)极发生反应。
(5)在允许 自由迁移的固体电解质燃料电池中,
自由迁移的固体电解质燃料电池中,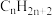 放电的电极反应式为
放电的电极反应式为___________ 。
(6)甲醇燃料电池中,吸附在催化剂表面的甲醇分子逐步脱氢得到CO,四步可能脱氢产物及其相对能量如图,则最可行途径为a→___________ (用b~j等代号表示)。

 具有较强的还原性,可用于制药工业。
具有较强的还原性,可用于制药工业。(1)
 是一元酸,25℃时,
是一元酸,25℃时, 。写出其电离方程式:
。写出其电离方程式:(2)用电渗析法制备
 的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
①写出阴极的电极反应:
②
 的移动方向是:
的移动方向是: 移向
移向③阳极室得到
 ,
, 的浓度逐渐增大。
的浓度逐渐增大。a.结合电极反应说明其原因是
b.该方法得到的产品
 溶液中会混有
溶液中会混有 。产生
。产生 的原因是
的原因是Ⅱ.氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(3)298K时,
 燃烧生成
燃烧生成 放热121kJ,
放热121kJ,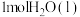 蒸发吸热44kJ,表示
蒸发吸热44kJ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为(4)氢氧燃料电池中氢气在
(5)在允许
 自由迁移的固体电解质燃料电池中,
自由迁移的固体电解质燃料电池中,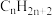 放电的电极反应式为
放电的电极反应式为(6)甲醇燃料电池中,吸附在催化剂表面的甲醇分子逐步脱氢得到CO,四步可能脱氢产物及其相对能量如图,则最可行途径为a→

您最近一年使用:0次
解题方法
8 . 下列有关电极方程式或离子(化学)方程式错误的是
A.电解饱和食盐水的阴极反应: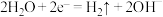 |
B.铅酸蓄电池充电时的阳极反应: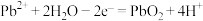 |
C.锅炉除垢过程中将 转化为 转化为 : : |
D. 制备 制备 的反应: 的反应: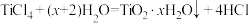 |
您最近一年使用:0次
9 . 向10mL氨水中加入蒸馏水,将其稀释到1L后,下列变化中正确的是
A. 的电离程度减小 的电离程度减小 | B.氨水的 增大 增大 |
C. 的数目增多 的数目增多 | D. 减小 减小 |
您最近一年使用:0次
解题方法
10 . Ⅰ.含硫化合物是实验室和工业上的常用化学品。请回答:
(1)实验室可用铜与浓硫酸反应制备少量 :
: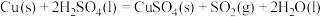
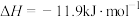 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由___________ 。
(2)已知
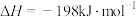 。850K时,在一恒容密闭反应器中充入一定量的
。850K时,在一恒容密闭反应器中充入一定量的 和
和 ,当反应达到平衡后测得
,当反应达到平衡后测得 、
、 和
和 的浓度分别为
的浓度分别为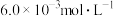 、
、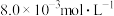 和
和 。
。
①该温度下反应的平衡常数为___________ 。
②平衡时 的转化率为
的转化率为___________ 。
(3)工业上主要采用接触法由含硫矿石制备硫酸。
①下列说法不正确的是___________ 。
A.须采用高温高压的反应条件使 氧化为
氧化为
B.进入接触室之前的气流无需净化处理
C.通入过量的空气可以提高含硫矿石和 的转化率
的转化率
D.在吸收塔中宜采用水或稀硫酸吸收 以提高吸收速率
以提高吸收速率
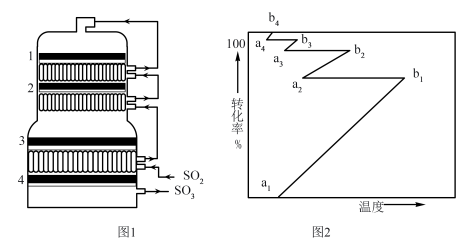
②接触室结构如图1所示,其中1~4表示催化剂层。图2所示进程中表示热交换过程的是___________ 。
A. B.
B. C.
C. D.
D. E.
E. F.
F. G.
G.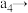
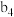
Ⅱ.一定条件下,用 、NiO或
、NiO或 作催化剂对燃煤烟气回收。反应为
作催化剂对燃煤烟气回收。反应为
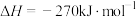 。
。
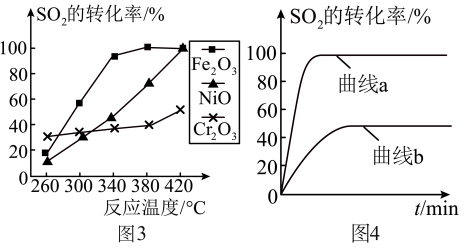
(4)其他条件相同、催化剂不同, 的转化率随反应温度的变化如图3,
的转化率随反应温度的变化如图3, 和NiO作催化剂均能使
和NiO作催化剂均能使 的转化率达到最高,不考虑催化剂价格因素,选择
的转化率达到最高,不考虑催化剂价格因素,选择 的主要优点是:
的主要优点是:___________ 。
(5)某科研小组用 作催化剂。在380℃时,分别研究了
作催化剂。在380℃时,分别研究了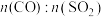 为1:1、3:1时
为1:1、3:1时 转化率的变化情况图4。则图4中表示
转化率的变化情况图4。则图4中表示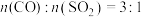 的变化曲线为
的变化曲线为___________ 。
(1)实验室可用铜与浓硫酸反应制备少量
 :
: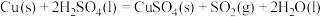
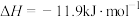 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由(2)已知

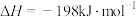 。850K时,在一恒容密闭反应器中充入一定量的
。850K时,在一恒容密闭反应器中充入一定量的 和
和 ,当反应达到平衡后测得
,当反应达到平衡后测得 、
、 和
和 的浓度分别为
的浓度分别为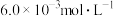 、
、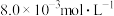 和
和 。
。①该温度下反应的平衡常数为
②平衡时
 的转化率为
的转化率为(3)工业上主要采用接触法由含硫矿石制备硫酸。
①下列说法不正确的是
A.须采用高温高压的反应条件使
 氧化为
氧化为
B.进入接触室之前的气流无需净化处理
C.通入过量的空气可以提高含硫矿石和
 的转化率
的转化率D.在吸收塔中宜采用水或稀硫酸吸收
 以提高吸收速率
以提高吸收速率②接触室结构如图1所示,其中1~4表示催化剂层。图2所示进程中表示热交换过程的是

A.
 B.
B. C.
C. D.
D. E.
E. F.
F. G.
G.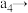
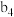
Ⅱ.一定条件下,用
 、NiO或
、NiO或 作催化剂对燃煤烟气回收。反应为
作催化剂对燃煤烟气回收。反应为
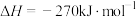 。
。(4)其他条件相同、催化剂不同,
 的转化率随反应温度的变化如图3,
的转化率随反应温度的变化如图3, 和NiO作催化剂均能使
和NiO作催化剂均能使 的转化率达到最高,不考虑催化剂价格因素,选择
的转化率达到最高,不考虑催化剂价格因素,选择 的主要优点是:
的主要优点是:(5)某科研小组用
 作催化剂。在380℃时,分别研究了
作催化剂。在380℃时,分别研究了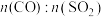 为1:1、3:1时
为1:1、3:1时 转化率的变化情况图4。则图4中表示
转化率的变化情况图4。则图4中表示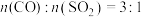 的变化曲线为
的变化曲线为
您最近一年使用:0次



