1 . 下列说法正确的是
A.乙烯的电子式为 |
B.乙烯的球棍模型为 |
| C.乙烯分子是空间平面结构 |
D.乙烯的结构简式为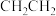 |
您最近一年使用:0次
名校
2 . 硫脲 在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备 ,然后
,然后 再与CaCN2合成
再与CaCN2合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。 易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
回答下列问题:
(1)实验前先检查装置气密性,操作为:①在E中加水至浸没导管末端,……;②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;③一段时间后,E处导管末端形成一段水柱,且高度不变。将操作①补充完整_______ 。
(2)检查气密性后加入药品,装置A中的试剂最佳组合是_______ (填字母),打开K2。
A.FeS固体+浓硫酸 B.FeS固体+稀硝酸 C.FeS固体+稀盐酸
装置B中盛装的试剂为_______ 。待A中反应结束后关闭K2,打开K1通N2一段时间,目的是_______ 。
(3)撤走搅拌器,打开K3,水浴加热D处三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是_______ ,D处合成硫脲的化学方程式为_______ 。
(4)将装置D中液体过滤后,结晶得到粗产品。测定粗产品中硫脲纯度:称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用cmol⋅L-1KMnO4标准溶液滴定,滴定至终点时消耗KMnO4标准溶液VmL。
①硫脲 中硫元素的化合价为
中硫元素的化合价为_______ 价。
②滴定时,硫脲转化为CO2、N2、 的离子方程式为
的离子方程式为_______ 。
③样品中硫脲的质量分数为_______ (用含“m,c、V”的式子表示)。
 在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备 ,然后
,然后 再与CaCN2合成
再与CaCN2合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。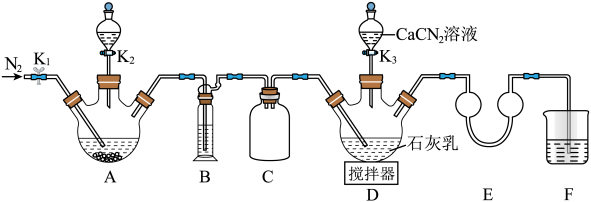
 易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。回答下列问题:
(1)实验前先检查装置气密性,操作为:①在E中加水至浸没导管末端,……;②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;③一段时间后,E处导管末端形成一段水柱,且高度不变。将操作①补充完整
(2)检查气密性后加入药品,装置A中的试剂最佳组合是
A.FeS固体+浓硫酸 B.FeS固体+稀硝酸 C.FeS固体+稀盐酸
装置B中盛装的试剂为
(3)撤走搅拌器,打开K3,水浴加热D处三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是
(4)将装置D中液体过滤后,结晶得到粗产品。测定粗产品中硫脲纯度:称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用cmol⋅L-1KMnO4标准溶液滴定,滴定至终点时消耗KMnO4标准溶液VmL。
①硫脲
 中硫元素的化合价为
中硫元素的化合价为②滴定时,硫脲转化为CO2、N2、
 的离子方程式为
的离子方程式为③样品中硫脲的质量分数为
您最近一年使用:0次
名校
3 . 下列事实不能通过比较氟元素和氯元素的电负性进行解释的是
| A.F-F键的键能小于Cl-Cl键的键能 | B.三氟乙酸的 大于三氯乙酸的 大于三氯乙酸的 |
| C.氟化氢分子的极性强于氯化氢分子的极性 | D.最高价含氧酸的酸性: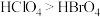 |
您最近一年使用:0次
名校
解题方法
4 . 下列化学用语或图示表达正确的是
| A.丙烯的结构简式为C3H6 |
B.2-甲基-1-丁醇的键线式: |
C.碳化钙中 的电子式: 的电子式: |
D.顺-2-丁烯的球棍模型: |
您最近一年使用:0次
名校
解题方法
5 . 设阿伏加德罗常数的值为NA,下列说法正确的是
| A.标准状况下,11.2L甲醇中含有的分子数为0.5NA |
| B.0.1mol氢氧根(OH-)和羟基(-OH)含有的电子数均为NA |
| C.3.0g甲醛(HCHO)和乙酸的混合物中含有的原子总数为0.4NA |
| D.1mol苯乙烯中含有碳碳双键数为4NA |
您最近一年使用:0次
名校
解题方法
6 . 化学与生产、生活、科技密切相关。下列说法正确的是
| A.我国提出2060年实现碳中和的目标,“碳中和”中的碳是指含碳的有机物 |
| B.T-碳(T-Carbon)是中科院预言的一种三维碳结构晶体,其与C60互为同位素 |
| C.人体细胞和细胞器的双分子膜是由大量两性分子组装而成的 |
| D.制作宇航服常用的材料有聚酯膜、聚四氟乙烯等,聚四氟乙烯的单体属于烯烃 |
您最近一年使用:0次
名校
解题方法
7 . 请回答以下问题:
(1)基态碳原子的价电子排布不能表示为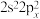 ,原因是违背
,原因是违背_______ 。
(2)下列有关乙烷(C2H6)和乙烯(C2H4)的描述正确的是_______(填字母)。
(3) 分子中Cl-C-Cl的键角
分子中Cl-C-Cl的键角_______ (填“>”、“<”或“=”)甲醛分子中H-C-H的键角。
(4)通常情况下,和乙烯的沸点(-103.7℃)比,氯乙烯(CH2=CHCl)的沸点更高(-13.9℃),其原因是_______ 。
(5)CO2在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于_______ 晶体;该晶体的熔点比SiO2晶体_______ (填“高”或“低”)_______ g/cm3(列出计算式即可)。
(1)基态碳原子的价电子排布不能表示为
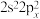 ,原因是违背
,原因是违背(2)下列有关乙烷(C2H6)和乙烯(C2H4)的描述正确的是_______(填字母)。
A.分子中均含有 键和 键和 键 键 | B.分子中的所有原子均处于同一平面上 |
| C.分子中的碳碳键键长:乙烯>乙烷 | D.乙烯中碳原子的杂化轨道类型为sp2 |
(3)
 分子中Cl-C-Cl的键角
分子中Cl-C-Cl的键角(4)通常情况下,和乙烯的沸点(-103.7℃)比,氯乙烯(CH2=CHCl)的沸点更高(-13.9℃),其原因是
(5)CO2在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于


您最近一年使用:0次
8 . 许多过渡金属离子能形成种类繁多的配合物。下列说法正确的是
A.难溶物 却能溶于氨水,是因为 却能溶于氨水,是因为 与 与 的结合能力更强而形成配离子所致 的结合能力更强而形成配离子所致 |
B. 中的 中的 提供接受孤电子对的空轨道,配体是氨分子和氯原子 提供接受孤电子对的空轨道,配体是氨分子和氯原子 |
C. 都是配合物 都是配合物 |
D. 中含 中含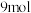 配位键 配位键 |
您最近一年使用:0次
名校
解题方法
9 . 下列化学用语或图示表达正确的是
A. 的VSEPR模型: 的VSEPR模型: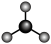 |
B.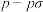 键电子云轮廓图: 键电子云轮廓图: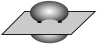 |
C. 的空间结构示意图为 的空间结构示意图为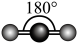 |
D.氨气分子中氮原子的杂化轨道表示式: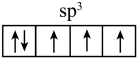 |
您最近一年使用:0次
名校
解题方法
10 . 下列事实不能 用有机物分子内基团间的相互影响解释的是
| A.2-甲基-1-丙醇能发生消去反应,2,2-二甲基-1-丙醇不能发生消去反应 |
| B.苯、甲苯发生硝化反应生成一硝基取代产物时,甲苯的反应温度更低 |
| C.苯不能与溴水发生取代反应,而苯酚能与溴水发生取代反应 |
| D.苯酚中的羟基能与碱反应,甲醇中的羟基不能与碱反应 |
您最近一年使用:0次



