名校
1 . 硫脲 在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备 ,然后
,然后 再与CaCN2合成
再与CaCN2合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。 易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
回答下列问题:
(1)实验前先检查装置气密性,操作为:①在E中加水至浸没导管末端,……;②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;③一段时间后,E处导管末端形成一段水柱,且高度不变。将操作①补充完整_______ 。
(2)检查气密性后加入药品,装置A中的试剂最佳组合是_______ (填字母),打开K2。
A.FeS固体+浓硫酸 B.FeS固体+稀硝酸 C.FeS固体+稀盐酸
装置B中盛装的试剂为_______ 。待A中反应结束后关闭K2,打开K1通N2一段时间,目的是_______ 。
(3)撤走搅拌器,打开K3,水浴加热D处三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是_______ ,D处合成硫脲的化学方程式为_______ 。
(4)将装置D中液体过滤后,结晶得到粗产品。测定粗产品中硫脲纯度:称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用cmol⋅L-1KMnO4标准溶液滴定,滴定至终点时消耗KMnO4标准溶液VmL。
①硫脲 中硫元素的化合价为
中硫元素的化合价为_______ 价。
②滴定时,硫脲转化为CO2、N2、 的离子方程式为
的离子方程式为_______ 。
③样品中硫脲的质量分数为_______ (用含“m,c、V”的式子表示)。
 在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备 ,然后
,然后 再与CaCN2合成
再与CaCN2合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。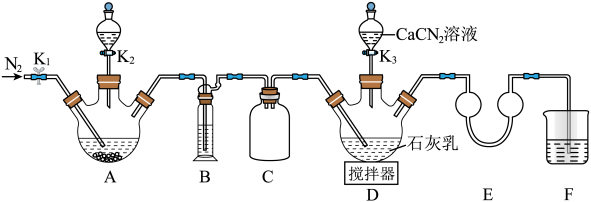
 易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。回答下列问题:
(1)实验前先检查装置气密性,操作为:①在E中加水至浸没导管末端,……;②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;③一段时间后,E处导管末端形成一段水柱,且高度不变。将操作①补充完整
(2)检查气密性后加入药品,装置A中的试剂最佳组合是
A.FeS固体+浓硫酸 B.FeS固体+稀硝酸 C.FeS固体+稀盐酸
装置B中盛装的试剂为
(3)撤走搅拌器,打开K3,水浴加热D处三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是
(4)将装置D中液体过滤后,结晶得到粗产品。测定粗产品中硫脲纯度:称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用cmol⋅L-1KMnO4标准溶液滴定,滴定至终点时消耗KMnO4标准溶液VmL。
①硫脲
 中硫元素的化合价为
中硫元素的化合价为②滴定时,硫脲转化为CO2、N2、
 的离子方程式为
的离子方程式为③样品中硫脲的质量分数为
您最近一年使用:0次
名校
解题方法
2 . 某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
根据表中记录的实验现象,回答下列问题。
(1)实验1、2中Al电极的作用是否相同______ (填“相同”或“不相同”)。
(2)实验3中Al为______ 极,电极反应式为______ ;
石墨为______ 极,电极反应式为______ ;
电池总反应为(离子方程式)______ 。
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
(1)实验1、2中Al电极的作用是否相同
(2)实验3中Al为
石墨为
电池总反应为(离子方程式)
您最近一年使用:0次
名校
解题方法
3 . 某温度下,在2L的恒容密闭容器中充入 与
与 的混合气体发生上述反应:
的混合气体发生上述反应: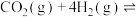
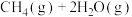 ,
, 与
与 的物质的量随时间的变化如图所示,下列说法正确的是
的物质的量随时间的变化如图所示,下列说法正确的是
 与
与 的混合气体发生上述反应:
的混合气体发生上述反应: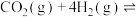
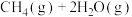 ,
, 与
与 的物质的量随时间的变化如图所示,下列说法正确的是
的物质的量随时间的变化如图所示,下列说法正确的是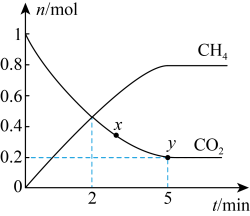
A.0-5min内,用 表示该反应的平均反应速率 表示该反应的平均反应速率 |
| B.2min时,v(正)=v(逆) |
| C.容器中混合气体的平均相对分子质量不再发生改变时,该反应达到平衡 |
D. 的转化率:x点>y点 的转化率:x点>y点 |
您最近一年使用:0次
名校
4 . 紫草是一种常见的中药材,广泛分布于我国的新疆和内蒙古地区,含有较多的活性成分,其中一种活性成分阿卡宁的结构简式如图所示。下列说法不正确的是
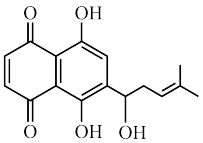
A.阿卡宁的分子式为 |
| B.阿卡宁与足量的氢气发生加成反应后的结构中含有7个手性碳原子 |
| C.阿卡宁可以发生取代、加成、消去、氧化、显色反应 |
| D.阿卡宁中所有的碳原子可能共平面 |
您最近一年使用:0次
2024-06-02更新
|
381次组卷
|
4卷引用:选择题7-12
(已下线)选择题7-12湖南省长沙市一中2024届高三下学期高考适应性演练(三)化学试题湖南省长沙市第一中学2024届高三下学期三模化学试题(已下线)湖南省永州市道县第一中学2023-2024学年高三下学期5月期中考试化学试题
名校
解题方法
5 .  与
与 、
、 均能发生反应,如图为
均能发生反应,如图为 与
与 发生反应生成HF过程中的能量变化示意图、请回答下列问题:
发生反应生成HF过程中的能量变化示意图、请回答下列问题:___________ (填“吸收”或“放出”,下同)能量,完成转化Ⅲ___________ 能量。
(2) 和
和 反应的能量变化图可用
反应的能量变化图可用___________ (填“A”或“B”)表示。 在
在 中燃烧的过程主要是
中燃烧的过程主要是___________ 能转化为___________ 能的过程。
 与
与 、
、 均能发生反应,如图为
均能发生反应,如图为 与
与 发生反应生成HF过程中的能量变化示意图、请回答下列问题:
发生反应生成HF过程中的能量变化示意图、请回答下列问题: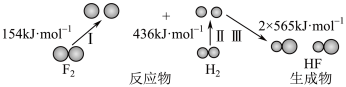
(2)
 和
和 反应的能量变化图可用
反应的能量变化图可用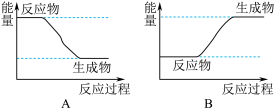
 在
在 中燃烧的过程主要是
中燃烧的过程主要是
您最近一年使用:0次
6 . 某药物中间体M的结构简式如图所示。下列有关该药物中间体的说法正确的是
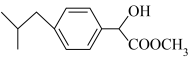
A.分子式为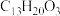 |
| B.最多有9个碳原子共平面 |
| C.苯环上的一氯代物只有2种(不考虑立体异构) |
| D.1mol该物质最多能与2molNaOH反应 |
您最近一年使用:0次
2024-06-01更新
|
175次组卷
|
3卷引用:选择题7-12
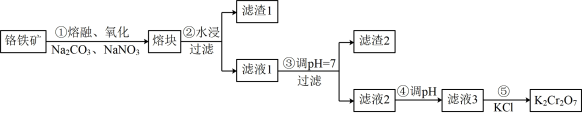
7 . 铬铁矿的主要成分为FeO▪Cr2O3, 制备K2Cr2O7流程如图所示:
(1)基态Cr原子价电子轨道分布图为__________ ,铬位于元素周期表中__________ 区。
(2)配合物[Cr(NH3)4(H2O)2]Cl中提供电子对形成配位键的原子是__________ ,中心离子的配位数为_________ 。
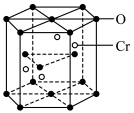
(3)铬的一种氧化物晶胞结构如图所示,若六棱柱的底面边长为lnm,高为hnm,NA代表同伏加德罗常数的值,则该晶体的密度p=__________ g/cm3。 形式存在。则该步主要反应的方程为
形式存在。则该步主要反应的方程为__________ ,该步骤不能使用陶瓷容器,原因是__________ 。
(5)步骤④调滤液2的pH使之变__________ (填“大”或“小”)。原因是__________ (用离子方程式表示)。
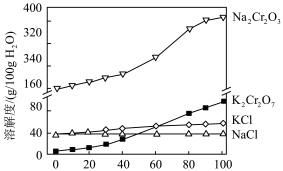
(6)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,分离得到K2Cr2O7固体的方法是__________ ,冷却到__________ (填标号)得到的K2Cr2O7固体产品最多。
(7)已知Ksp(Ag2CrO4 )=1.0×10-12、Ksp(AgCl)=2.0×10-10, 若用10LNaCl溶液溶解0.1mol的Ag2CrO4固体,则NaCl溶液的最初浓度不得低于__________ mol/L。
(1)基态Cr原子价电子轨道分布图为
(2)配合物[Cr(NH3)4(H2O)2]Cl中提供电子对形成配位键的原子是
(3)铬的一种氧化物晶胞结构如图所示,若六棱柱的底面边长为lnm,高为hnm,NA代表同伏加德罗常数的值,则该晶体的密度p=
 形式存在。则该步主要反应的方程为
形式存在。则该步主要反应的方程为(5)步骤④调滤液2的pH使之变
(6)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,分离得到K2Cr2O7固体的方法是
(7)已知Ksp(Ag2CrO4 )=1.0×10-12、Ksp(AgCl)=2.0×10-10, 若用10LNaCl溶液溶解0.1mol的Ag2CrO4固体,则NaCl溶液的最初浓度不得低于
您最近一年使用:0次
8 . 化合物G俗称依普黄酮,是一种抗骨质疏松药物的主要成分。以甲苯为原料合成该化合物的路线如下图所示:___________ 。
(2)H的名称为___________ 。
(3)G中含氧官能团的名称为___________ ,反应B→C的反应类型为___________ 。
(4)F与足量的 完全加成后所生成的化合物中手性碳原子的个数为
完全加成后所生成的化合物中手性碳原子的个数为___________ 。
(5)N的同分异构体中既能发生银镜反应又能发生水解反应的共有___________ 种。请写出其中核磁共振氢谱有五组峰的有机物在加热条件下,和足量的盐酸发生水解反应的化学方程式:___________ 。
(6)根据上述信息,设计以苯酚和为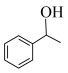 原料,制备
原料,制备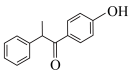 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)___________ 。
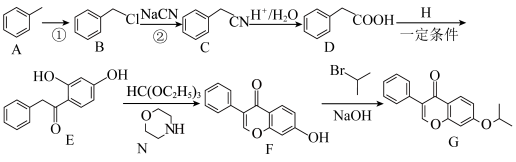
已知: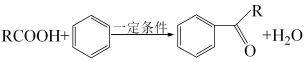
(2)H的名称为
(3)G中含氧官能团的名称为
(4)F与足量的
 完全加成后所生成的化合物中手性碳原子的个数为
完全加成后所生成的化合物中手性碳原子的个数为(5)N的同分异构体中既能发生银镜反应又能发生水解反应的共有
(6)根据上述信息,设计以苯酚和为
 原料,制备
原料,制备 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)
您最近一年使用:0次
解题方法
9 . 下列化学用语或图示表达正确的是
A. 的结构式:Cl﹣S﹣S﹣Cl 的结构式:Cl﹣S﹣S﹣Cl |
B.中子数为18的氯原子: |
C.四氯化碳分子的空间填充模型: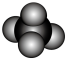 |
D.顺-2-丁烯的结构简式: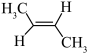 |
您最近一年使用:0次
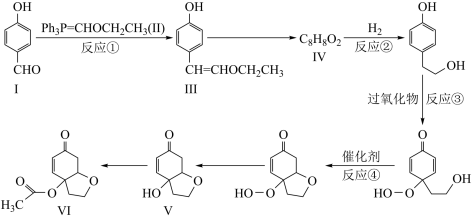
10 . 天然产物V具有抗疟活性,某研究小组以化合物Ⅰ为原料合成Ⅴ及其衍生物Ⅵ的路线如下(部分反应条件省略,Ph表示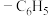 ):
):______ ,化合物Ⅲ中含氧官能团有______ (写名称)。
(2)反应①的方程式可表示为:Ⅰ+Ⅱ=Ⅲ+Z,化合物Z的分子式为______ 。
(3)化合物Ⅳ能发生银镜反应,写出其结构简式______ 。
(4)反应②的反应类型是______ ,反应③的反应类型是______ 。
(5)化合物Ⅵ的芳香族同分异构体中,同时满足如下条件的有______ 种,写出其中任意一种的结构简式______ 。
条件:a.能与NaHCO3反应;b.最多能与2倍物质的量的NaOH反应;c.能与3倍物质的量的Na发生放出H2的反应;d.核磁共振氢谱确定分子中有7个化学环境相同的氢原子;ę.不含手性碳原子(手性碳原子是指连有4个不同的原子或原子团的饱和碳原子)。
(6)已知: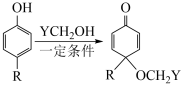 ,根据上述信息,写出以苯酚的一种同系物及
,根据上述信息,写出以苯酚的一种同系物及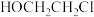 为原料合成
为原料合成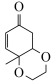 的路线
的路线______ (不需注明反应条件)。
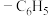 ):
):
(2)反应①的方程式可表示为:Ⅰ+Ⅱ=Ⅲ+Z,化合物Z的分子式为
(3)化合物Ⅳ能发生银镜反应,写出其结构简式
(4)反应②的反应类型是
(5)化合物Ⅵ的芳香族同分异构体中,同时满足如下条件的有
条件:a.能与NaHCO3反应;b.最多能与2倍物质的量的NaOH反应;c.能与3倍物质的量的Na发生放出H2的反应;d.核磁共振氢谱确定分子中有7个化学环境相同的氢原子;ę.不含手性碳原子(手性碳原子是指连有4个不同的原子或原子团的饱和碳原子)。
(6)已知:
 ,根据上述信息,写出以苯酚的一种同系物及
,根据上述信息,写出以苯酚的一种同系物及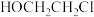 为原料合成
为原料合成 的路线
的路线
您最近一年使用:0次



