1 . 甘氨酸亚铁[(NH2CH2COO)2Fe]是一种补铁强化剂。实验室以FeCO3与甘氨酸(NH2CH2COOH)为原料制备甘氨酸亚铁的装置如图所示(夹持和加热仪器已省略)。
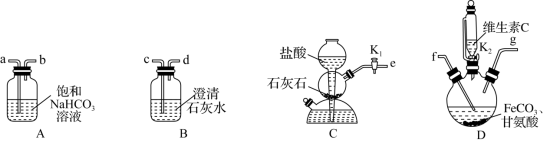
已知:
①甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
②维生素C易溶于水,具有较强的还原性和酸性。
回答下列问题:
(1)装置D中盛放维生素C的仪器名称是_______ ,上述装置依次连接的合理顺序为e→_______ (按气流方向,用小写字母表示)。
(2)实验开始时,先关闭K2,打开K1,当_______ (填实验现象)时,关闭K1,打开K2,进行实验。
(3)为了提高甘氨酸亚铁的产率,需要控制D中溶液的pH不能过高或过低。加入维生素C促进FeCO3溶解并调节溶液pH,维生素C的作用还有_______ 。
(4)写出装置D中生成甘氨酸亚铁的化学方程式:_______ 。
(5)实验结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥,得到甘氨酸亚铁。洗涤所选用的最佳试剂是_______ (填字母)。
a.蒸馏水 b.维生素C c.乙醇
(6)测定产品的含量。实验步骤如下:称量a g产品于锥形瓶中,溶解后进行必要处理,用容量瓶配制成200ml溶液,量取20.00ml,并加入2滴指示剂,用c mol/L Ce(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为b mL。(已知滴定反应为Ce4++Fe2+=Ce3++Fe3+)
①产品中甘氨酸亚铁的质量分数表达式为_______ 。
②若滴定前滴定管内无气泡,滴定结束后有气泡,会使测定结果_______ (填“偏高”、“偏低”或“无影响”)。

已知:
①甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
②维生素C易溶于水,具有较强的还原性和酸性。
回答下列问题:
(1)装置D中盛放维生素C的仪器名称是
(2)实验开始时,先关闭K2,打开K1,当
(3)为了提高甘氨酸亚铁的产率,需要控制D中溶液的pH不能过高或过低。加入维生素C促进FeCO3溶解并调节溶液pH,维生素C的作用还有
(4)写出装置D中生成甘氨酸亚铁的化学方程式:
(5)实验结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥,得到甘氨酸亚铁。洗涤所选用的最佳试剂是
a.蒸馏水 b.维生素C c.乙醇
(6)测定产品的含量。实验步骤如下:称量a g产品于锥形瓶中,溶解后进行必要处理,用容量瓶配制成200ml溶液,量取20.00ml,并加入2滴指示剂,用c mol/L Ce(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为b mL。(已知滴定反应为Ce4++Fe2+=Ce3++Fe3+)
①产品中甘氨酸亚铁的质量分数表达式为
②若滴定前滴定管内无气泡,滴定结束后有气泡,会使测定结果
您最近一年使用:0次
名校
解题方法
2 . 氮化钙有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。某化学兴趣小组设计制备氮化钙并测定其纯度的实验如下:
已知:氮化钙(Ca3N2)是一种棕色粉末,遇水会发生水解,生成氢氧化钙并放出氨。
I.氮化钙的制备(如图):

(1)仪器a的名称是_______ 。
(2)装置A中每生成标准状况下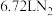 ,转移的电子数为
,转移的电子数为_______ 。
(3)装置C的作用是吸收氧气,则C中发生反应的离子方程式为_______ 。
(4)设计实验证明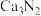 中混有钙单质,写出实验操作及现象:
中混有钙单质,写出实验操作及现象:_______ 。
II.测定氮化钙的纯度:
(5)甲同学称取mg反应后的固体,加入足量的碳酸钠溶液充分反应,过滤、洗涤、干燥得ng沉淀,通过数据m、n即可求得氮化钙的质量分数。
甲同学的方案是否合理?_______ (填“是”或“否”),理由是_______ 。
(6)乙同学的方案如下:
取氮化钙样品24g,按图所示装置进行实验,发现B装置增重5.1g。
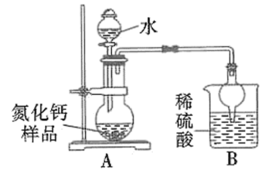
①该样品中氮化钙的质量分数为_______ 。
②导致该样品中氮化钙含量测定结果偏低的可能原因是_______ 。
已知:氮化钙(Ca3N2)是一种棕色粉末,遇水会发生水解,生成氢氧化钙并放出氨。
I.氮化钙的制备(如图):

(1)仪器a的名称是
(2)装置A中每生成标准状况下
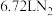 ,转移的电子数为
,转移的电子数为(3)装置C的作用是吸收氧气,则C中发生反应的离子方程式为
(4)设计实验证明
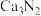 中混有钙单质,写出实验操作及现象:
中混有钙单质,写出实验操作及现象:II.测定氮化钙的纯度:
(5)甲同学称取mg反应后的固体,加入足量的碳酸钠溶液充分反应,过滤、洗涤、干燥得ng沉淀,通过数据m、n即可求得氮化钙的质量分数。
甲同学的方案是否合理?
(6)乙同学的方案如下:
取氮化钙样品24g,按图所示装置进行实验,发现B装置增重5.1g。

①该样品中氮化钙的质量分数为
②导致该样品中氮化钙含量测定结果偏低的可能原因是
您最近一年使用:0次
2021-09-16更新
|
255次组卷
|
3卷引用:内蒙古海拉尔第二中学2021-2022学年高三上学期第一次阶段考化学试题
3 . 七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上有重要的用途。硼镁泥是硼镁矿生产硼砂的废渣,其主要成分是MgCO3,还含有MgO、CaO、Fe2O3、FeO、MnO2、Al2O3、SiO2等杂质,工业上用硼镁泥制取七水硫酸镁的工艺流程如图:
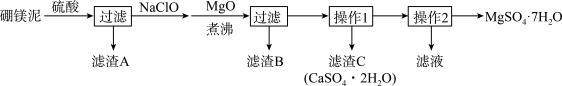
已知:①MnO2不溶于稀硫酸。
②CaSO4和MgSO4·7H2O在不同温度下的溶解度(g)数据如下表所示:
(1)开始用到硫酸的质量分数为70%,密度为1.61g/cm3,则该硫酸溶液的物质的量浓度为___ 。
(2)滤渣A中除含少量CaSO4·2H2O外,还有___ 。
(3)加入MgO后,加热煮沸的目的是___ 。
(4)若滤渣B的主要成分为Al(OH)3和Fe(OH)3。则加入NaClO发生氧化还原反应的离子方程式为___ 。
(5)流程中操作1为蒸发浓缩、趁热过滤,这样即可得到CaSO4·2H2O,又防止___ 。
(6)获取MgSO4·7H2O的操作2为:___ 、___ 、过滤洗涤。
(7)已知开始硼镁泥样品的质量为ag,制取七水硫酸镁的质量为bg,据此能计算出硼镁泥中镁元素的含量吗?若能,请写出表达式;若不能,请说明理由。___ (能或不能),表达式(或理由)为___ 。

已知:①MnO2不溶于稀硫酸。
②CaSO4和MgSO4·7H2O在不同温度下的溶解度(g)数据如下表所示:
| 温度/℃ 物质 | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.21 | 0.19 |
| MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 | —— |
(2)滤渣A中除含少量CaSO4·2H2O外,还有
(3)加入MgO后,加热煮沸的目的是
(4)若滤渣B的主要成分为Al(OH)3和Fe(OH)3。则加入NaClO发生氧化还原反应的离子方程式为
(5)流程中操作1为蒸发浓缩、趁热过滤,这样即可得到CaSO4·2H2O,又防止
(6)获取MgSO4·7H2O的操作2为:
(7)已知开始硼镁泥样品的质量为ag,制取七水硫酸镁的质量为bg,据此能计算出硼镁泥中镁元素的含量吗?若能,请写出表达式;若不能,请说明理由。
您最近一年使用:0次
2020-04-04更新
|
355次组卷
|
3卷引用:内蒙古呼伦贝尔市海拉尔区2020届高三上学期第一次模拟统一考试理科综合化学试题
解题方法
4 . 互为同分异构体的物质不可能
| A.具有相同的相对分子质量 |
| B.具有相同的熔、沸点和密度 |
| C.具有相同的分子式 |
| D.各组成元素的质量分数分别相同 |
您最近一年使用:0次
5 . 实验室需要0.1 mol⋅L NaOH溶液450 mL和0.5 mol⋅L
NaOH溶液450 mL和0.5 mol⋅L 硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:
硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:
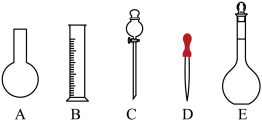
(1)如图所示的仪器中配制溶液肯定不需要的是___________ (填字母)。仪器C的名称是___________ ,本实验所需玻璃仪器E的规格和名称是___________ 。___________ (填“大于”“等于”或“小于”,下同)0.1 mol⋅L 。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度
。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度___________ 0.1 mol⋅L 。
。
(3)根据计算得知,所需质量分数为98%、密度为1.84 g⋅cm 的浓硫酸的体积为
的浓硫酸的体积为___________ mL(计算结果保留一位小数)。如果实验室有10 mL、25 mL、50 mL量筒,应选用___________ mL规格的量筒最好。
(4)如果定容时不小心超过刻度线,应如何操作:___________ 。
 NaOH溶液450 mL和0.5 mol⋅L
NaOH溶液450 mL和0.5 mol⋅L 硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:
硫酸溶液450 mL。根据这两种溶液的配制情况回答下列问题:(1)如图所示的仪器中配制溶液肯定不需要的是
 。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度
。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度 。
。(3)根据计算得知,所需质量分数为98%、密度为1.84 g⋅cm
 的浓硫酸的体积为
的浓硫酸的体积为(4)如果定容时不小心超过刻度线,应如何操作:
您最近一年使用:0次
名校
解题方法
6 . 实验室需要配制 的硫酸溶液500mL。请回答下列问题:
的硫酸溶液500mL。请回答下列问题:
(1)根据计算得,需量取质量分数为98%、密度为 的浓硫酸的体积为
的浓硫酸的体积为_______ mL(保留三位有效数字)。
(2)在如图所示仪器中,配制上述溶液肯定不需要的有_______ (填序号)。

(3)实验操作步骤包括
A.把溶液小心地转移至容量瓶中。
B.量取所需浓硫酸,沿杯壁倒入盛有适量水的烧杯中,同时用玻璃棒搅拌并冷却至室温。
C.继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面与刻度线相切。
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液都小心注入容量瓶,并轻轻振荡。
E.将容量瓶塞塞紧,充分摇匀。
操作步骤的正确顺序为_______ (填序号)。
(4)下列情况中,会使所配溶液浓度偏高的是_______ (填序号)。
A.量取浓硫酸时,某同学仰视液面读数
B.没有进行上述的操作步骤D
C.定容加蒸馏水时,不慎超过了刻度线
D.容量瓶使用前内壁沾有水珠
E.用少量蒸馏水洗涤量取浓硫酸后的量筒,并将洗涤液注入烧杯
 的硫酸溶液500mL。请回答下列问题:
的硫酸溶液500mL。请回答下列问题:(1)根据计算得,需量取质量分数为98%、密度为
 的浓硫酸的体积为
的浓硫酸的体积为(2)在如图所示仪器中,配制上述溶液肯定不需要的有

(3)实验操作步骤包括
A.把溶液小心地转移至容量瓶中。
B.量取所需浓硫酸,沿杯壁倒入盛有适量水的烧杯中,同时用玻璃棒搅拌并冷却至室温。
C.继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面与刻度线相切。
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液都小心注入容量瓶,并轻轻振荡。
E.将容量瓶塞塞紧,充分摇匀。
操作步骤的正确顺序为
(4)下列情况中,会使所配溶液浓度偏高的是
A.量取浓硫酸时,某同学仰视液面读数
B.没有进行上述的操作步骤D
C.定容加蒸馏水时,不慎超过了刻度线
D.容量瓶使用前内壁沾有水珠
E.用少量蒸馏水洗涤量取浓硫酸后的量筒,并将洗涤液注入烧杯
您最近一年使用:0次
2022-08-21更新
|
95次组卷
|
3卷引用:内蒙古海拉尔第一中学2022-2023学年高一上学期期末考试化学试题
名校
7 . 合成氨工业中采用循环操作(如图),主要是为了
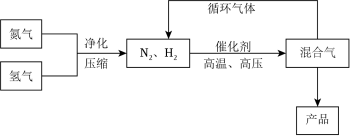
| A.降低氨的沸点 | B.提高氮气和氢气的利用率 |
| C.提高平衡混合物中氨的含量 | D.增大化学反应速率 |
您最近一年使用:0次
2023-05-19更新
|
535次组卷
|
8卷引用:内蒙古呼伦贝尔市满洲里远方中学2023-2024学年高二上学期期末考试化学试题
名校
解题方法
8 . 氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出氮元素的原子结构示意图:_______ 。
(2)通常情况下,氮气性质不活泼,其原因是__________。
(3)N2的电子式:_______ ,将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是_______ 。
A.N2和H2在一定条件下反应生成NH3 B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO D.NH3和HNO3反应生成NH4NO3
(4)氨气的电子式:_______ 。
(5)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。写出此反应的化学方程式_____ 。
(1)写出氮元素的原子结构示意图:
(2)通常情况下,氮气性质不活泼,其原因是__________。
| A.氮分子是双原子分子 | B.氮元素的非金属性很强 |
| C.氮原子的半径较小 | D.破坏氮分子中的化学键很难 |
A.N2和H2在一定条件下反应生成NH3 B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO D.NH3和HNO3反应生成NH4NO3
(4)氨气的电子式:
(5)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。写出此反应的化学方程式
您最近一年使用:0次
2023-03-23更新
|
111次组卷
|
3卷引用:内蒙古呼伦贝尔市满洲里远方中学2023-2024学年高一下学期3月考试化学试题
名校
解题方法
9 . 以铁镍合金(含少量铜)为原料,生产电极材料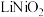 的部分工艺流程如下:
的部分工艺流程如下:
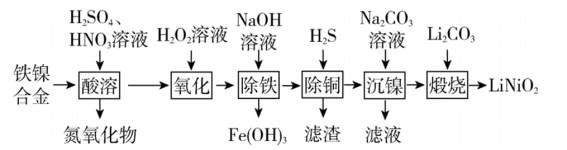
已知:(1)表中列出了几种金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 计算)。
计算)。
(2)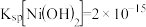 ;
;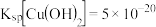 。
。
回答下列问题。
(1)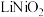 中
中 的化合价为
的化合价为__ 。“酸溶”时 转化为
转化为 ,该过程中温度控制在70~80℃的原因是
,该过程中温度控制在70~80℃的原因是__ 。
(2)“酸溶”时镍生成 ,写出铁镍合金中镍参与反应的离子方程式:
,写出铁镍合金中镍参与反应的离子方程式:____ 。
(3)“除铜”时若选用 ,会导致部分
,会导致部分 也产生沉淀,当溶液中
也产生沉淀,当溶液中 、
、 沉淀同时存在时,溶液中
沉淀同时存在时,溶液中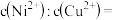
__ 。
(4)“沉镍”时得到碳酸镍( )沉淀。在空气中碳酸镍与碳酸锂共同“煅烧”可制得
)沉淀。在空气中碳酸镍与碳酸锂共同“煅烧”可制得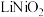 ,该反应的化学方程式为
,该反应的化学方程式为____ 。
(5)“沉镍”后的滤液中主要是 和
和 ,当溶液中二者的物质的量之比为1:1时,溶液中离子浓度由大到小的顺序是
,当溶液中二者的物质的量之比为1:1时,溶液中离子浓度由大到小的顺序是__ 。
(6)已知铁镍合金中镍的质量分数为29.5%,称取10.0g合金,最终制得4.7g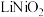 ,则合金中
,则合金中 的利用率为
的利用率为____ (保留两位有效数字)。
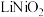 的部分工艺流程如下:
的部分工艺流程如下:
已知:(1)表中列出了几种金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0
 计算)。
计算)。| 开始沉淀的pH | 沉淀完全的pH | |
 | 6.7 | 9.5 |
 | 1.1 | 3.2 |
 | 5.8 | 8.8 |
 | 4.2 | 7.2 |
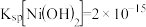 ;
;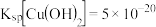 。
。回答下列问题。
(1)
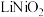 中
中 的化合价为
的化合价为 转化为
转化为 ,该过程中温度控制在70~80℃的原因是
,该过程中温度控制在70~80℃的原因是(2)“酸溶”时镍生成
 ,写出铁镍合金中镍参与反应的离子方程式:
,写出铁镍合金中镍参与反应的离子方程式:(3)“除铜”时若选用
 ,会导致部分
,会导致部分 也产生沉淀,当溶液中
也产生沉淀,当溶液中 、
、 沉淀同时存在时,溶液中
沉淀同时存在时,溶液中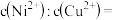
(4)“沉镍”时得到碳酸镍(
 )沉淀。在空气中碳酸镍与碳酸锂共同“煅烧”可制得
)沉淀。在空气中碳酸镍与碳酸锂共同“煅烧”可制得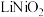 ,该反应的化学方程式为
,该反应的化学方程式为(5)“沉镍”后的滤液中主要是
 和
和 ,当溶液中二者的物质的量之比为1:1时,溶液中离子浓度由大到小的顺序是
,当溶液中二者的物质的量之比为1:1时,溶液中离子浓度由大到小的顺序是(6)已知铁镍合金中镍的质量分数为29.5%,称取10.0g合金,最终制得4.7g
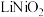 ,则合金中
,则合金中 的利用率为
的利用率为
您最近一年使用:0次
2021-04-19更新
|
278次组卷
|
4卷引用:内蒙古海拉尔第二中学2021-2022学年高三上学期期末考试理科综合化学试题
内蒙古海拉尔第二中学2021-2022学年高三上学期期末考试理科综合化学试题辽宁省“决胜新高考·名校交流“2021届高三3月联考化学试题(已下线)微专题18 金属及其化合物制备流程(Ni)-备战2022年高考化学考点微专题湖南省株洲市南方中学2021-2022学年高三下学期4月月考化学试题
解题方法
10 . 氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示:
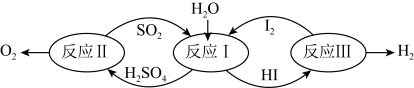
(1)反应Ⅰ的化学方程式是___ 。
(2)已知反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)△H=+550kJ·mol-1
它由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g)△H=+177kJ·mol-1;ii.SO3(g)分解。
则SO3(g)分解的热化学方程式为___ 。
(3)L(L1、L2)、X可分别代表压强或温度其中之一。如图表示L一定时,ii中SO3(g)的质量分数随X的变化关系。
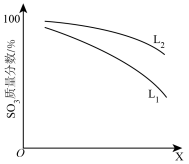
①X代表的物理量是___ 。
②判断L1、L2的大小关系:L1___ L2(填“>”“<”或“=”)。

(1)反应Ⅰ的化学方程式是
(2)已知反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)△H=+550kJ·mol-1
它由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g)△H=+177kJ·mol-1;ii.SO3(g)分解。
则SO3(g)分解的热化学方程式为
(3)L(L1、L2)、X可分别代表压强或温度其中之一。如图表示L一定时,ii中SO3(g)的质量分数随X的变化关系。

①X代表的物理量是
②判断L1、L2的大小关系:L1
您最近一年使用:0次
2020-11-18更新
|
57次组卷
|
2卷引用:内蒙古阿荣旗第一中学2020-2021学年高二上学期期中考试化学试题



