1 . 卤素化合物在生产生活中应用广泛,回答下列问题
(1)研究表明 气体中存在单体和环状六聚体的平衡:
气体中存在单体和环状六聚体的平衡: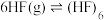 ,HF形成环状六聚体的作用力是
,HF形成环状六聚体的作用力是____________ ;在测定 相对分子质量的实验中,
相对分子质量的实验中,____________ (填“低压”或“高压”)有利于测定的准确性.
(2) 气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸
气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸 和氯酸钾
和氯酸钾 在酸性条件下制备
在酸性条件下制备 ,离子方程式为
,离子方程式为__________ ;产物中的另一种气体可以起到的作用是________________ .
(3) 与
与 以共价键形成
以共价键形成 ,其中
,其中________ 显负电性, 与水反应的方程式是
与水反应的方程式是____________ .
(4)利用 和浓磷酸制备
和浓磷酸制备 的原理是:
的原理是: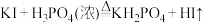 ,该反应中利用了浓磷酸的什么性质:
,该反应中利用了浓磷酸的什么性质:________ (“强酸性”“强氧化性”“高沸点”).
(1)研究表明
 气体中存在单体和环状六聚体的平衡:
气体中存在单体和环状六聚体的平衡: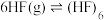 ,HF形成环状六聚体的作用力是
,HF形成环状六聚体的作用力是 相对分子质量的实验中,
相对分子质量的实验中,(2)
 气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸
气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸 和氯酸钾
和氯酸钾 在酸性条件下制备
在酸性条件下制备 ,离子方程式为
,离子方程式为(3)
 与
与 以共价键形成
以共价键形成 ,其中
,其中 与水反应的方程式是
与水反应的方程式是(4)利用
 和浓磷酸制备
和浓磷酸制备 的原理是:
的原理是: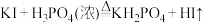 ,该反应中利用了浓磷酸的什么性质:
,该反应中利用了浓磷酸的什么性质:
您最近一年使用:0次
解题方法
2 . 某溶液可能含有等浓度的下列某些离子: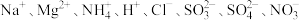 ,取溶液分别进行如下实验:
,取溶液分别进行如下实验:
①加入 酸化的
酸化的 溶液产生白色沉淀;
溶液产生白色沉淀;
②加入淀粉 溶液,呈蓝色;
溶液,呈蓝色;
③加入 溶液产生白色沉淀,加热后产生有刺激性气味的气体。
溶液产生白色沉淀,加热后产生有刺激性气味的气体。
下列说法错误的是
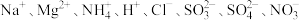 ,取溶液分别进行如下实验:
,取溶液分别进行如下实验:①加入
 酸化的
酸化的 溶液产生白色沉淀;
溶液产生白色沉淀;②加入淀粉
 溶液,呈蓝色;
溶液,呈蓝色;③加入
 溶液产生白色沉淀,加热后产生有刺激性气味的气体。
溶液产生白色沉淀,加热后产生有刺激性气味的气体。下列说法错误的是
A.由①②可知一定有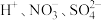 |
B.若将①中的试剂换成盐酸酸化的 溶液,不影响成分的判断 溶液,不影响成分的判断 |
C.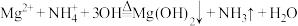 |
D.不能确定有无 |
您最近一年使用:0次
3 . 实验室中用如图装置,以氨气和钠为原料加热至 制备氨基钠
制备氨基钠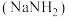 ,并检验气体产物.已知:
,并检验气体产物.已知: 极易水解.下列说法正确的是
极易水解.下列说法正确的是
 制备氨基钠
制备氨基钠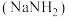 ,并检验气体产物.已知:
,并检验气体产物.已知: 极易水解.下列说法正确的是
极易水解.下列说法正确的是
| A.装置A中的药品是氯化铵固体 | B.装置B和装置D均只起到干燥作用 |
| C.实验时先点燃C处酒精灯,再点燃A处酒精灯 | D.装置E中黑色粉末变成红色,证明有氢气生成 |
您最近一年使用:0次
2024-03-26更新
|
322次组卷
|
2卷引用:安徽省淮北市2024届高三第一次质量检测(一模)化学试题
名校
解题方法
4 . 某小组为探究 (三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。
(三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。

(1)在实验进行的过程中,应该持续通入氮气的目的是___________ 。
(2)若实验中观察装置F中澄清石灰水变浑浊,装置E中固体变为红色,则说明 的热分解产物中一定含有
的热分解产物中一定含有___________ 。
(3)该样品完全热分解后,欲检测固体生成物中的组成,某同学待装置冷却后取少量固体加入稀硫酸溶解,再加入 溶液变红,说明
溶液变红,说明___________ 。
(4)已知: 是一种光敏化合物,见光分解。该实验小组在探究
是一种光敏化合物,见光分解。该实验小组在探究 热分解后,用该装置再次探究它光解的产物,现取
热分解后,用该装置再次探究它光解的产物,现取 固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。
固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。
完成下列小题:
①若反应后 元素的化合价降为
元素的化合价降为 价,K元素的化合价未改变,且两者仍为草酸
价,K元素的化合价未改变,且两者仍为草酸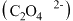 盐,写出三草酸合铁酸钾完全光解的化学方程式
盐,写出三草酸合铁酸钾完全光解的化学方程式___________ 。
②据此计算出该 固体的纯度为
固体的纯度为___________ (保留一位有效数字) 。
③样品完全分解后,实验小组停止通氮气,一段时间后,某同学取少许装置A中的残留物于试管中,加入稀硫酸溶解,滴入1~2滴 溶液,发现溶液变红,这与上述
溶液,发现溶液变红,这与上述 分解产物为
分解产物为 价
价 的结论不符可能的原因是
的结论不符可能的原因是___________ 。
 (三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。
(三草酸合铁酸钾晶体)的热分解产物,按如图所示装置进行实验(部分夹持装置省略)。
(1)在实验进行的过程中,应该持续通入氮气的目的是
(2)若实验中观察装置F中澄清石灰水变浑浊,装置E中固体变为红色,则说明
 的热分解产物中一定含有
的热分解产物中一定含有(3)该样品完全热分解后,欲检测固体生成物中的组成,某同学待装置冷却后取少量固体加入稀硫酸溶解,再加入
 溶液变红,说明
溶液变红,说明(4)已知:
 是一种光敏化合物,见光分解。该实验小组在探究
是一种光敏化合物,见光分解。该实验小组在探究 热分解后,用该装置再次探究它光解的产物,现取
热分解后,用该装置再次探究它光解的产物,现取 固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。
固体20.00g,使充分反应后,称得B、C装置共增重1.76g,D装置增重2.16g,E、F装置均无明显现象。完成下列小题:
①若反应后
 元素的化合价降为
元素的化合价降为 价,K元素的化合价未改变,且两者仍为草酸
价,K元素的化合价未改变,且两者仍为草酸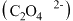 盐,写出三草酸合铁酸钾完全光解的化学方程式
盐,写出三草酸合铁酸钾完全光解的化学方程式②据此计算出该
 固体的纯度为
固体的纯度为③样品完全分解后,实验小组停止通氮气,一段时间后,某同学取少许装置A中的残留物于试管中,加入稀硫酸溶解,滴入1~2滴
 溶液,发现溶液变红,这与上述
溶液,发现溶液变红,这与上述 分解产物为
分解产物为 价
价 的结论不符可能的原因是
的结论不符可能的原因是
您最近一年使用:0次
名校
解题方法
5 . 如表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
针对元素①~⑩回答下列问题。
(1)元素①和②的单质化合形成的化合物 中,H元素的化合价为
中,H元素的化合价为___________ , 能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为
能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为___________ 。
(2)由元素①和⑥形成的一种物质是天然气的主要成分,其化学式为___________ ;元素⑥还可以和⑧形成一种三原子直线形分子,其结构式为___________ ;元素②的单质在元素⑦的单质中点燃生成淡黄色固体,将该固体投入硫酸亚铁溶液中,预测主要的反应现象是___________ 。
(3)元素③、⑧、⑨的简单离子中半径最大的是___________ ;(填离子符号),元素②和⑤的最高价氧化物对应的水化物之间可以发生反应,其反应的离子方程式为___________ 。
| 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ⑤ | ⑧ | ⑨ | ||||
| 4 | ③ | ④ | ⑩ | |||||
(1)元素①和②的单质化合形成的化合物
 中,H元素的化合价为
中,H元素的化合价为 能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为
能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为(2)由元素①和⑥形成的一种物质是天然气的主要成分,其化学式为
(3)元素③、⑧、⑨的简单离子中半径最大的是
您最近一年使用:0次
名校
解题方法
6 . 金属铋在工业上常用于制造低熔点合金,用于消防装置、自动喷水器、锅炉等的安全塞,一旦发生火灾,·些水管的活塞会“自动”熔化,喷出水来。由一种铋矿[主要成分为 (不溶于水),含强氧化性杂质
(不溶于水),含强氧化性杂质 等]制备金属铋的简单工艺如图:
等]制备金属铋的简单工艺如图:
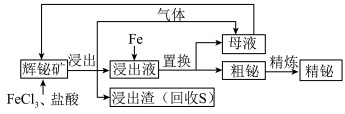
已知:酸性条件下的氧化性: 。
。
(1)“浸出”过程中,溶液中放出的气体是_________ ;放出该气体的离子方程式是________ 。
(2)加入 溶液的目的是
溶液的目的是___________ ,该反应的离子方程式是___________ 。
(3)检验母液中所含有的主要金属阳离子的方法是___________ 。
(4)铋的+5价盐类( 盐)具有强氧化性。欲探究
盐)具有强氧化性。欲探究 盐类的氧化性强弱,某实验小组进行了以下实验,取一定量的
盐类的氧化性强弱,某实验小组进行了以下实验,取一定量的 溶液,向其中依次加入下列试剂,对应的现象如下表所示:
溶液,向其中依次加入下列试剂,对应的现象如下表所示:
据图回答下面的问题:
①上述试剂的氧化性强弱顺序为:___________ 。
②写出 和
和 反应的离子方程式,并用双线桥法标注电子转移方向
反应的离子方程式,并用双线桥法标注电子转移方向_________ ,已知 不溶于水。)
不溶于水。)
 (不溶于水),含强氧化性杂质
(不溶于水),含强氧化性杂质 等]制备金属铋的简单工艺如图:
等]制备金属铋的简单工艺如图:
已知:酸性条件下的氧化性:
 。
。(1)“浸出”过程中,溶液中放出的气体是
(2)加入
 溶液的目的是
溶液的目的是(3)检验母液中所含有的主要金属阳离子的方法是
(4)铋的+5价盐类(
 盐)具有强氧化性。欲探究
盐)具有强氧化性。欲探究 盐类的氧化性强弱,某实验小组进行了以下实验,取一定量的
盐类的氧化性强弱,某实验小组进行了以下实验,取一定量的 溶液,向其中依次加入下列试剂,对应的现象如下表所示:
溶液,向其中依次加入下列试剂,对应的现象如下表所示:| 加入溶液 | ①适量铋酸钠固体 | ②过量的双氧水 | ③加入淀粉 溶液 溶液 |
| 实验现象 | 溶液呈现紫红色 | 紫红色消失,产生气泡 | 溶液变为蓝色 |
①上述试剂的氧化性强弱顺序为:
②写出
 和
和 反应的离子方程式,并用双线桥法标注电子转移方向
反应的离子方程式,并用双线桥法标注电子转移方向 不溶于水。)
不溶于水。)
您最近一年使用:0次
名校
解题方法
7 . 硫酸有着广泛的用途。硫酸工业在国民经济中占有重要地位。
(1)实验室可用铜与浓硫酸反应制备少量 :
: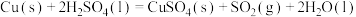
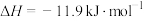 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由___________ 。
(2)我国古籍记载了硫酸的制备方法—“炼石胆( )取精华法”。
)取精华法”。
①借助现代仪器分析,该制备过程中 分解的TG曲线(热重曲线,即受热分解过程中固体质量变化曲线)及DSC曲线(反映体系热量变化情况,数值已省略)如图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有
分解的TG曲线(热重曲线,即受热分解过程中固体质量变化曲线)及DSC曲线(反映体系热量变化情况,数值已省略)如图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有___________ 、___________ (填化学式)和 。
。
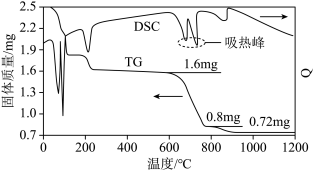
②已知下列热化学方程式:
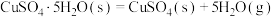



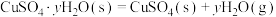

则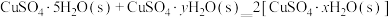 的△H=
的△H=__________  。
。
(3)接触法制硫酸的关键反应为 的催化氧化:
的催化氧化: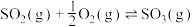
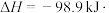

①为寻求固定投料比下不同反应阶段的最佳生产温度,绘制不同转化率( )下反应速率(数值已略去)与温度的关系如图,下列说法正确的是
)下反应速率(数值已略去)与温度的关系如图,下列说法正确的是__________ 。
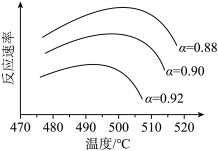
A.温度越高,反应速率越大 B.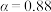 的曲线代表平衡转化率
的曲线代表平衡转化率
C. 越大,反应速率最大值对应温度越低 D.可根据不同
越大,反应速率最大值对应温度越低 D.可根据不同 下的最大速率,选择最佳生产温度
下的最大速率,选择最佳生产温度
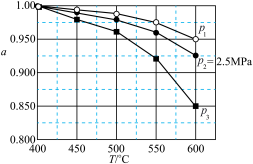
②固定投料比,在压强分别为0.5MPa、2.5MPa和5.0MPa下,得到 的平衡转化率随温度的变化如图所示。则在5.0MPa、550℃时,该反应的平衡转化率=
的平衡转化率随温度的变化如图所示。则在5.0MPa、550℃时,该反应的平衡转化率=__________ 。
③对于气体参与的反应,可用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B)来表示平衡常数 。设
。设 的平衡分压为p,
的平衡分压为p, 的平衡转化率为
的平衡转化率为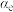 ,则上述催化氧化反应
,则上述催化氧化反应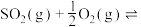
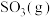 的
的
_____________ (用含p和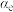 的代数式表示)。
的代数式表示)。
(1)实验室可用铜与浓硫酸反应制备少量
 :
: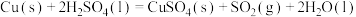
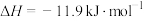 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由(2)我国古籍记载了硫酸的制备方法—“炼石胆(
 )取精华法”。
)取精华法”。①借助现代仪器分析,该制备过程中
 分解的TG曲线(热重曲线,即受热分解过程中固体质量变化曲线)及DSC曲线(反映体系热量变化情况,数值已省略)如图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有
分解的TG曲线(热重曲线,即受热分解过程中固体质量变化曲线)及DSC曲线(反映体系热量变化情况,数值已省略)如图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有 。
。
②已知下列热化学方程式:
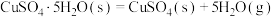



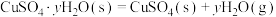

则
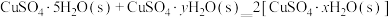 的△H=
的△H= 。
。(3)接触法制硫酸的关键反应为
 的催化氧化:
的催化氧化: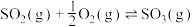
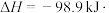

①为寻求固定投料比下不同反应阶段的最佳生产温度,绘制不同转化率(
 )下反应速率(数值已略去)与温度的关系如图,下列说法正确的是
)下反应速率(数值已略去)与温度的关系如图,下列说法正确的是
A.温度越高,反应速率越大 B.
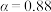 的曲线代表平衡转化率
的曲线代表平衡转化率C.
 越大,反应速率最大值对应温度越低 D.可根据不同
越大,反应速率最大值对应温度越低 D.可根据不同 下的最大速率,选择最佳生产温度
下的最大速率,选择最佳生产温度②固定投料比,在压强分别为0.5MPa、2.5MPa和5.0MPa下,得到
 的平衡转化率随温度的变化如图所示。则在5.0MPa、550℃时,该反应的平衡转化率=
的平衡转化率随温度的变化如图所示。则在5.0MPa、550℃时,该反应的平衡转化率=
③对于气体参与的反应,可用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B)来表示平衡常数
 。设
。设 的平衡分压为p,
的平衡分压为p, 的平衡转化率为
的平衡转化率为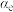 ,则上述催化氧化反应
,则上述催化氧化反应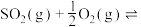
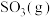 的
的
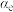 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
8 . T℃时,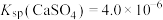 、
、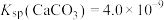 、
、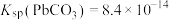 ,三种盐的沉淀溶解平衡曲线如图所示,pM=-lgc(阴离子)、pN=-lgc(阳离子)。下列说法错误的是
,三种盐的沉淀溶解平衡曲线如图所示,pM=-lgc(阴离子)、pN=-lgc(阳离子)。下列说法错误的是

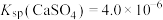 、
、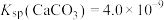 、
、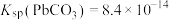 ,三种盐的沉淀溶解平衡曲线如图所示,pM=-lgc(阴离子)、pN=-lgc(阳离子)。下列说法错误的是
,三种盐的沉淀溶解平衡曲线如图所示,pM=-lgc(阴离子)、pN=-lgc(阳离子)。下列说法错误的是
A.c线是 沉淀溶解平衡曲线 沉淀溶解平衡曲线 |
B.T℃时,向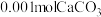 沉淀中加入 沉淀中加入 溶液(反应后溶液为1L),使 溶液(反应后溶液为1L),使 沉淀会转化为 沉淀会转化为 沉淀,所需 沉淀,所需 的物质的量至少为1.001mol 的物质的量至少为1.001mol |
C.T℃时,向10mL水中加入 和 和 至二者均饱和,溶液中 至二者均饱和,溶液中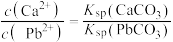 |
D.若d点表示 的饱和溶液加入 的饱和溶液加入 饱和溶液等体积混合则: 饱和溶液等体积混合则: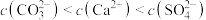 |
您最近一年使用:0次
2023-12-02更新
|
452次组卷
|
3卷引用:安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题
安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题浙江省台州市山海协作体2023-2024学年高二上学期期中联考化学试题(已下线)寒假作业07 沉淀溶解平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
名校
解题方法
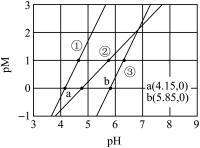
9 . 常温下,向含有CH3COOH、CuSO4、FeSO4的工业废水中逐滴加入NaOH溶液,pM随pH变化关系如图所示[pM表示 或
或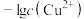 或
或 ],曲线①③斜率相同。已知:
],曲线①③斜率相同。已知: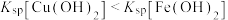 ;当离子浓度
;当离子浓度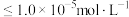 时,可认为该离子沉淀完全。下列说法不正确的是
时,可认为该离子沉淀完全。下列说法不正确的是
 或
或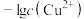 或
或 ],曲线①③斜率相同。已知:
],曲线①③斜率相同。已知: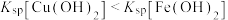 ;当离子浓度
;当离子浓度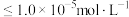 时,可认为该离子沉淀完全。下列说法不正确的是
时,可认为该离子沉淀完全。下列说法不正确的是
A.曲线①表示 与pH的关系 与pH的关系 |
B.pH=6时,溶液中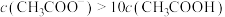 |
C.pH=7时,可认为 沉淀完全 沉淀完全 |
D.pH=8时 |
您最近一年使用:0次
2023-12-01更新
|
423次组卷
|
5卷引用:安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题
安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题河北省沧州市部分高中2023-2024学年高三上学期11月期中考试化学试题(已下线)寒假作业07 沉淀溶解平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)(已下线)选择题11-15江西省宜春市丰城市第九中学2023-2024学年高二下学期4月月考化学试题
10 . 阿斯巴甜(G)是一种广泛应用于食品工业的添加剂,一种合成阿斯巴甜(G)的路线如下:
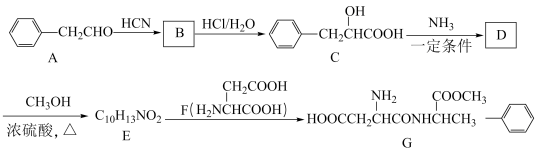
已知如下信息:
①


②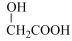


回答下列问题:
(1)A中官能团的名称是_______ 。
(2)A生成B反应的化学方程式为_______ 。
(3)D的结构简式为_______ ,D生成E的反应中浓硫酸的作用是_______ 。
(4)E生成G的反应类型为_______ 。
(5)写出能同时满足下列条件的C的同分异构体的结构简式_______ 。
①分子中含有苯环,且苯环上有两个取代基
②能与FeCl3溶液发生显色反应
③能在氢氧化钠溶液中发生水解反应,且含有苯环的水解产物的核磁共振氢谱只有一组峰
(6)参照上述合成路线,设计以乙醛为起始原料制备聚丙氨酸的合成路线_______ (无机试剂任选)。

已知如下信息:
①



②
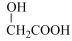


回答下列问题:
(1)A中官能团的名称是
(2)A生成B反应的化学方程式为
(3)D的结构简式为
(4)E生成G的反应类型为
(5)写出能同时满足下列条件的C的同分异构体的结构简式
①分子中含有苯环,且苯环上有两个取代基
②能与FeCl3溶液发生显色反应
③能在氢氧化钠溶液中发生水解反应,且含有苯环的水解产物的核磁共振氢谱只有一组峰
(6)参照上述合成路线,设计以乙醛为起始原料制备聚丙氨酸的合成路线
您最近一年使用:0次
2023-06-30更新
|
192次组卷
|
2卷引用:安徽省淮北市2023-2024学年高三上学期1月调研化学试题



