名校
解题方法
1 . 第十四届全国冬季运动会主火炬使用天然气燃料,第19届杭州亚运会主火炬首次采用零排放的甲醇燃料。下列叙述正确的是
A. 和 和 均为正四面体形分子 均为正四面体形分子 |
| B.等物质的量的甲烷和甲醇完全燃烧,甲烷消耗的氧气更多 |
C.甲烷和甲醇中只有碳原子采用 杂化 杂化 |
D. 和 和 的红外光谱信号相同 的红外光谱信号相同 |
您最近一年使用:0次
名校
2 . 钠、镁、铝、硅、磷、硫、氯的元素对应的某“物理量”递变规律符合图像的是

| A.原子半径 | B.单质的熔点 | C.第一电离能 | D.电负性 |
您最近一年使用:0次
名校
解题方法
3 . 氢气是非常重要的化学能源,利用氢气可以实现化学能向热能、电能的直接转化。
(1)已知断开 、
、 、
、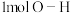 需要的能量依次是
需要的能量依次是 、
、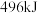 、.
、. .,则
.,则 是
是___________ (填“吸热”或“放热”)反应,能正确表示反应 中能量变化的是图
中能量变化的是图___________ (填“甲”或“乙”)。 和
和 组合形成的质子交换膜燃料电池的结构如下图:
组合形成的质子交换膜燃料电池的结构如下图:___________ (填“正极”或“负极”),电极c的电极反应式为___________ 。
②若电路中转移 电子,则该燃料电池理论上消耗的
电子,则该燃料电池理论上消耗的 在标况下的体积为
在标况下的体积为___________ L。
(3)将纯锌片和纯铜片按图中方式插入100mL浓度为2mol/L的稀硫酸中一段时间,回答下列问题:___________ 。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②当图中构成原电池的电路中转移0.1mol的电子时,负极的质量___________ (填“增加”或“减少”)___________ g。
③请写出图中构成原电池的负极电极反应式:___________ 。
(1)已知断开
 、
、 、
、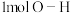 需要的能量依次是
需要的能量依次是 、
、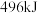 、.
、. .,则
.,则 是
是 中能量变化的是图
中能量变化的是图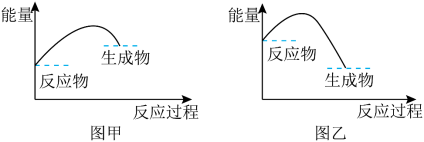
 和
和 组合形成的质子交换膜燃料电池的结构如下图:
组合形成的质子交换膜燃料电池的结构如下图: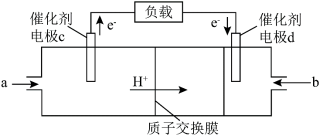
②若电路中转移
 电子,则该燃料电池理论上消耗的
电子,则该燃料电池理论上消耗的 在标况下的体积为
在标况下的体积为(3)将纯锌片和纯铜片按图中方式插入100mL浓度为2mol/L的稀硫酸中一段时间,回答下列问题:

A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②当图中构成原电池的电路中转移0.1mol的电子时,负极的质量
③请写出图中构成原电池的负极电极反应式:
您最近一年使用:0次
名校
解题方法
4 . 某实验小组同学用铜与浓硫酸反应制取SO2,验证SO2性质并制备NaHSO3,设计如图所示实验装置。
(1)装浓硫酸的仪器名称是___________ 。
(2)C中的实验现象是___________ ,若把C试管中紫色石蕊溶液换为品红溶液,C中的现象为___________ ;F的作用是___________ 。
(3)A中发生反应的化学方程式是___________ ,该反应体现了浓硫酸具有___________ 性。
(4)试管D中酸性高锰酸钾溶液褪色,表明SO2具有___________ 性。
(5)装置E中设计多孔球泡的目的是___________ 。
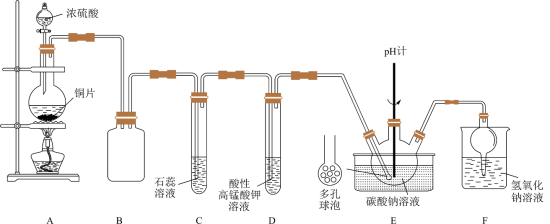
(1)装浓硫酸的仪器名称是
(2)C中的实验现象是
(3)A中发生反应的化学方程式是
(4)试管D中酸性高锰酸钾溶液褪色,表明SO2具有
(5)装置E中设计多孔球泡的目的是
您最近一年使用:0次
名校
解题方法
5 . 某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示,由图中数据分析:___________ 。
(2)反应开始至2min,用X表示的平均反应速率为___________ ;平衡时,Y的转化率为___________ ,平衡时,Z的浓度为___________ mol·L-1。
(3)下列叙述能说明上述反应达到平衡状态的是___________。
(4)若改变下列一个条件,该反应的速率变化是(填“增大”、“减小”或“不变”)。
①降低温度,化学反应速率___________ 。
②恒容下充入1molNe,化学反应速率___________ 。
③恒容下充入1molX,化学反应速率___________ 。
④将容器的体积变为3L,化学反应速率___________ 。
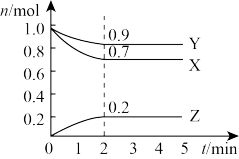
(2)反应开始至2min,用X表示的平均反应速率为
(3)下列叙述能说明上述反应达到平衡状态的是___________。
| A.正、逆反应速率相等且不为零 |
| B.X、Y、Z的物质的量之比为3:1:2 |
| C.单位时间内每消耗3molX,同时消耗2molZ |
| D.混合气体的密度不随时间的变化而变化 |
①降低温度,化学反应速率
②恒容下充入1molNe,化学反应速率
③恒容下充入1molX,化学反应速率
④将容器的体积变为3L,化学反应速率
您最近一年使用:0次
名校
解题方法
6 . 元素周期表的一部分如图,表中每一序号分别代表一种元素。回答下列问题。
(1)⑧元素的简单离子的结构示意图为___________ ,⑨元素在周期表中的位置为___________ 。
(2)④元素和⑤元素形成的某种化合物A可以做供氧剂,A与②元素的最高价氧化物反应的化学方程式为___________ 。
(3)⑤元素的焰色为___________ 色,⑤元素最高价氧化物对应的水化物溶液与⑥元素形成的单质反应的离子方程式为___________ 。
(4)③元素、⑧元素的最简单气态氢化物接触时会有白烟产生,该白烟为___________ (填化学式);②元素、③元素、④元素的最简单氢化物稳定性由强到弱的顺序为___________ 。
(5)⑦元素和⑧元素中的最高价氧化物对应水化物的酸性更强的为___________ (填化学式)。
| ① | ||||||||||
| ② | ③ | ④ | ||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | |||||||
| ⑨ | …… | |||||||||
(2)④元素和⑤元素形成的某种化合物A可以做供氧剂,A与②元素的最高价氧化物反应的化学方程式为
(3)⑤元素的焰色为
(4)③元素、⑧元素的最简单气态氢化物接触时会有白烟产生,该白烟为
(5)⑦元素和⑧元素中的最高价氧化物对应水化物的酸性更强的为
您最近一年使用:0次
名校
解题方法
7 . 某同学设计如下方案从粗食盐水中除去 等离子,以制得精盐水。并进行电解饱和食盐水的实验:
等离子,以制得精盐水。并进行电解饱和食盐水的实验:
 等离子,以制得精盐水。并进行电解饱和食盐水的实验:
等离子,以制得精盐水。并进行电解饱和食盐水的实验: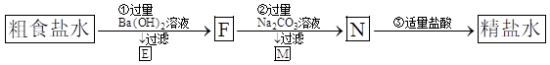
A.②中加入过量 溶液的主要目的是为了除去 溶液的主要目的是为了除去 |
B.E中主要有 和 和 ,也可能有一些 ,也可能有一些 |
| C.N溶液呈碱性 |
D.③目的是除去 和 和 |
您最近一年使用:0次
名校
8 . 设NA为阿伏加德罗常数的值。下列有关叙述正确的是
| A.N2与H2反应生成1molNH3转移的电子数目为3NA |
| B.18gD2O中含有的质子数为10NA |
C.标准状况下,11.2L 分子数为0.5 分子数为0.5 |
D.0.5mol/L 溶液中,含有 溶液中,含有 的数目为 的数目为 |
您最近一年使用:0次
名校
解题方法
9 . 化学与生产、生活密切相关。下列说法不正确的是
| A.在燃煤中加入石灰石,有利于防治酸雨 |
| B.84消毒液应避光密封保存 |
| C.补铁剂搭配维生素C服用有助于铁的吸收 |
| D.食品包装袋中的生石灰有防氧化作用 |
您最近一年使用:0次
名校
解题方法
10 . 某化学兴趣小组用甲、乙两套装置(如图所示)进行丙烯酸( )与乙醇(
)与乙醇( )酯化反应的实验。已知:乙醇的沸点为78.5℃,丙烯酸的沸点为141℃,丙烯酸乙酯的沸点为99.8℃、回答下列问题:
)酯化反应的实验。已知:乙醇的沸点为78.5℃,丙烯酸的沸点为141℃,丙烯酸乙酯的沸点为99.8℃、回答下列问题:_______ ,仪器A、B中的溶液均为_______ 。
(2)甲、乙两套装置中效果比较好的装置是_______ ,原因是_______ 。
(3)乙装置中冷凝水应该从_______ (填“a”或“b”)口进入。
(4)按甲图安装好仪器后,在反应管中加入配制的体积比为3∶2的乙醇和丙烯酸,加热至沸腾,很久也没有果香味液体生成,原因是_______ 。
(5)乙醇需要过量一些的原因是_______ 。
(6)某同学选用了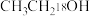 、
、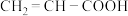 两个反应物,对酯化反应的原理进行探究。请写出该反应的化学方程式:
两个反应物,对酯化反应的原理进行探究。请写出该反应的化学方程式:_______ 。
(7)下列有关有机知识表述正确的是_______ (填字母)。
A.乙烯可以通过加成反应制得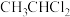
B.等物质的量的甲烷和乙酸完全燃烧时所需 的质量相同
的质量相同
C.乙酸乙酯中含有乙酸杂质,可加入一定量的乙醇和浓硫酸通过酯化反应除去
 )与乙醇(
)与乙醇( )酯化反应的实验。已知:乙醇的沸点为78.5℃,丙烯酸的沸点为141℃,丙烯酸乙酯的沸点为99.8℃、回答下列问题:
)酯化反应的实验。已知:乙醇的沸点为78.5℃,丙烯酸的沸点为141℃,丙烯酸乙酯的沸点为99.8℃、回答下列问题:
(2)甲、乙两套装置中效果比较好的装置是
(3)乙装置中冷凝水应该从
(4)按甲图安装好仪器后,在反应管中加入配制的体积比为3∶2的乙醇和丙烯酸,加热至沸腾,很久也没有果香味液体生成,原因是
(5)乙醇需要过量一些的原因是
(6)某同学选用了
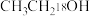 、
、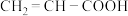 两个反应物,对酯化反应的原理进行探究。请写出该反应的化学方程式:
两个反应物,对酯化反应的原理进行探究。请写出该反应的化学方程式:(7)下列有关有机知识表述正确的是
A.乙烯可以通过加成反应制得
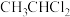
B.等物质的量的甲烷和乙酸完全燃烧时所需
 的质量相同
的质量相同C.乙酸乙酯中含有乙酸杂质,可加入一定量的乙醇和浓硫酸通过酯化反应除去
您最近一年使用:0次



