解题方法
1 .  加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。
加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。
(1)由 加氢生成
加氢生成 的反应为
的反应为
①若 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热
___________ 
②若在一定温度下的容积固定的密闭容器中进行该反应,则可以提高 平衡转化率的措施有
平衡转化率的措施有___________ (写出两种)。
③下列说法可以证明该反应已达到平衡状态的是___________ (填字母)。
a.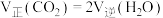 b.
b. 的物质的量分数不再改变
的物质的量分数不再改变
c.容器内气体密度不再改变 d. 和
和 的浓度之比为1:2
的浓度之比为1:2
e.混合气的平均摩尔质量不再变化 f.单位时间内生成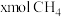 的同时又消耗
的同时又消耗
④ 催化加氢合成
催化加氢合成 过程中,
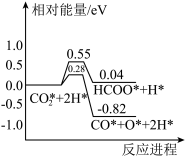
过程中, 活化的可能途径如有图所示,CO是
活化的可能途径如有图所示,CO是 活化的优势中间体,原因是
活化的优势中间体,原因是___________ 。
(2)一定条件下 与
与 也可以生成
也可以生成 ,某温度下在容积为2L的恒容密闭容器中充入
,某温度下在容积为2L的恒容密闭容器中充入 和一定量
和一定量 发生反应:
发生反应: 。
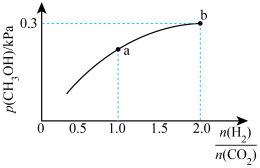
。 的平衡分压与起始投料比
的平衡分压与起始投料比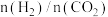 的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
___________ 。b点时,再充入 和
和 ,使两者分压均增大0.2kPa,则此时平衡
,使两者分压均增大0.2kPa,则此时平衡___________ (填“正向”、“逆向”或“不”)移动。
(3)一定条件下 与
与 还可以生成甲酸,方程式为
还可以生成甲酸,方程式为
 。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体,
。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体, 除了能分解成
除了能分解成 和
和 ,还能分解为CO和
,还能分解为CO和 ,反应为:
,反应为:
 ,则此平衡体系中CO或
,则此平衡体系中CO或 的选择性和HCOOH的转化率随温度变化曲线如图所示。
的选择性和HCOOH的转化率随温度变化曲线如图所示。

提示:CO(或氢气)的选择性
图中随着温度升高,HCOOH的转化率增大,请解释CO的选择性下降可能的原因:___________ ;400°C时 的体积分数为
的体积分数为___________ 。
 加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。
加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。(1)由
 加氢生成
加氢生成 的反应为
的反应为
①若
 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热

| 物质 |  |  |  |  |
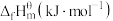 |  | 0 | 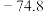 | 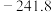 |
 平衡转化率的措施有
平衡转化率的措施有③下列说法可以证明该反应已达到平衡状态的是
a.
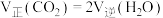 b.
b. 的物质的量分数不再改变
的物质的量分数不再改变c.容器内气体密度不再改变 d.
 和
和 的浓度之比为1:2
的浓度之比为1:2e.混合气的平均摩尔质量不再变化 f.单位时间内生成
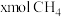 的同时又消耗
的同时又消耗
④
 催化加氢合成
催化加氢合成 过程中,
过程中, 活化的可能途径如有图所示,CO是
活化的可能途径如有图所示,CO是 活化的优势中间体,原因是
活化的优势中间体,原因是
(2)一定条件下
 与
与 也可以生成
也可以生成 ,某温度下在容积为2L的恒容密闭容器中充入
,某温度下在容积为2L的恒容密闭容器中充入 和一定量
和一定量 发生反应:
发生反应: 。
。 的平衡分压与起始投料比
的平衡分压与起始投料比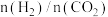 的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
 和
和 ,使两者分压均增大0.2kPa,则此时平衡
,使两者分压均增大0.2kPa,则此时平衡
(3)一定条件下
 与
与 还可以生成甲酸,方程式为
还可以生成甲酸,方程式为
 。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体,
。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体, 除了能分解成
除了能分解成 和
和 ,还能分解为CO和
,还能分解为CO和 ,反应为:
,反应为:
 ,则此平衡体系中CO或
,则此平衡体系中CO或 的选择性和HCOOH的转化率随温度变化曲线如图所示。
的选择性和HCOOH的转化率随温度变化曲线如图所示。
提示:CO(或氢气)的选择性

图中随着温度升高,HCOOH的转化率增大,请解释CO的选择性下降可能的原因:
 的体积分数为
的体积分数为
您最近一年使用:0次
2 . 下列关于各图的说法错误的是
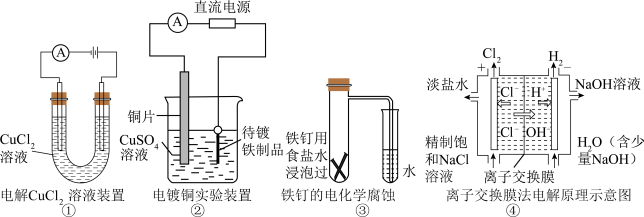

| A.①中阳极处能产生使湿润的淀粉-KI试纸变蓝的气体 |
| B.②中待镀铁制品应与电源负极相连而形成铜镀层 |
| C.③中可证明铁发生了析氢腐蚀 |
D.④中的离子交换膜可以避免生成的 与NaOH溶液反应 与NaOH溶液反应 |
您最近一年使用:0次
2023-10-22更新
|
753次组卷
|
6卷引用:江西省萍乡中学、新余市第一中学2023-2024学年高二上学期10月创新班联考化学试题
名校
解题方法
3 . 研究小组探究高铜酸钠(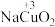 )的制备和性质。
)的制备和性质。
资料:高铜酸钠为棕黑色固体,难溶于水。
实验I.向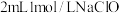 溶液中滴加
溶液中滴加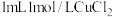 溶液,迅速产生蓝绿色沉淀,振荡后得到棕黑色的浊液a,将其等分成2份。
溶液,迅速产生蓝绿色沉淀,振荡后得到棕黑色的浊液a,将其等分成2份。
(1)蓝绿色沉淀中含有 ,用离子方程式表示
,用离子方程式表示 溶液显碱性的原因:
溶液显碱性的原因:_________ 。
(2)探究棕黑色沉淀的组成。
实验II.将一份浊液a过滤、洗涤、干燥,得到固体b;取少量固体b,滴加稀 ,沉淀溶解,有气泡产生,得到蓝色溶液。
,沉淀溶解,有气泡产生,得到蓝色溶液。
①另取少量固体b进行实验,证实了 中钠元素的存在,实验操作的名称是
中钠元素的存在,实验操作的名称是_________ 。
②进一步检验,棕黑色固体是 ,
, 与稀
与稀 反应的离子方程式是
反应的离子方程式是_________ 。
(3)探究实验条件对 制备的影响。
制备的影响。
实验III.向另一份浊液a中继续滴加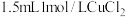 溶液,沉淀由棕黑色变为蓝绿色,溶液的
溶液,沉淀由棕黑色变为蓝绿色,溶液的 约为5,有
约为5,有 产生。
产生。
①对 的来源,甲同学认为是
的来源,甲同学认为是 和
和 反应生成了
反应生成了 ,乙同学认为该说法不严谨,提出了生成
,乙同学认为该说法不严谨,提出了生成 的其他原因:
的其他原因:_________ 。
②探究“继续滴加 溶液,
溶液, 能氧化
能氧化 的原因。
的原因。
ⅰ.提出假设1: 增大,
增大, 的还原性增强,实验证明假设成立,操作和现象是:取少量
的还原性增强,实验证明假设成立,操作和现象是:取少量 固体于试管中,
固体于试管中,_________ 。
ⅱ.提出假设2:_________ ,经证实该假设也成立。
(4)改进实验方案,进行实验。
实验IV,向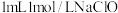 溶液中滴加
溶液中滴加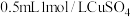 溶液,迅速生成蓝色沉淀,振荡后得到棕黑色浊液。浊液放置过程中,沉淀表面缓慢产生气泡并出现蓝色固体,该气体不能使湿润的淀粉
溶液,迅速生成蓝色沉淀,振荡后得到棕黑色浊液。浊液放置过程中,沉淀表面缓慢产生气泡并出现蓝色固体,该气体不能使湿润的淀粉 试纸变蓝。
试纸变蓝。
 放置过程中产生气体的化学方程式是
放置过程中产生气体的化学方程式是_________ 。
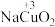 )的制备和性质。
)的制备和性质。资料:高铜酸钠为棕黑色固体,难溶于水。
实验I.向
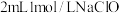 溶液中滴加
溶液中滴加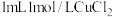 溶液,迅速产生蓝绿色沉淀,振荡后得到棕黑色的浊液a,将其等分成2份。
溶液,迅速产生蓝绿色沉淀,振荡后得到棕黑色的浊液a,将其等分成2份。(1)蓝绿色沉淀中含有
 ,用离子方程式表示
,用离子方程式表示 溶液显碱性的原因:
溶液显碱性的原因:(2)探究棕黑色沉淀的组成。
实验II.将一份浊液a过滤、洗涤、干燥,得到固体b;取少量固体b,滴加稀
 ,沉淀溶解,有气泡产生,得到蓝色溶液。
,沉淀溶解,有气泡产生,得到蓝色溶液。①另取少量固体b进行实验,证实了
 中钠元素的存在,实验操作的名称是
中钠元素的存在,实验操作的名称是②进一步检验,棕黑色固体是
 ,
, 与稀
与稀 反应的离子方程式是
反应的离子方程式是(3)探究实验条件对
 制备的影响。
制备的影响。实验III.向另一份浊液a中继续滴加
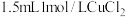 溶液,沉淀由棕黑色变为蓝绿色,溶液的
溶液,沉淀由棕黑色变为蓝绿色,溶液的 约为5,有
约为5,有 产生。
产生。①对
 的来源,甲同学认为是
的来源,甲同学认为是 和
和 反应生成了
反应生成了 ,乙同学认为该说法不严谨,提出了生成
,乙同学认为该说法不严谨,提出了生成 的其他原因:
的其他原因:②探究“继续滴加
 溶液,
溶液, 能氧化
能氧化 的原因。
的原因。ⅰ.提出假设1:
 增大,
增大, 的还原性增强,实验证明假设成立,操作和现象是:取少量
的还原性增强,实验证明假设成立,操作和现象是:取少量 固体于试管中,
固体于试管中,ⅱ.提出假设2:
(4)改进实验方案,进行实验。
实验IV,向
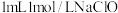 溶液中滴加
溶液中滴加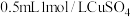 溶液,迅速生成蓝色沉淀,振荡后得到棕黑色浊液。浊液放置过程中,沉淀表面缓慢产生气泡并出现蓝色固体,该气体不能使湿润的淀粉
溶液,迅速生成蓝色沉淀,振荡后得到棕黑色浊液。浊液放置过程中,沉淀表面缓慢产生气泡并出现蓝色固体,该气体不能使湿润的淀粉 试纸变蓝。
试纸变蓝。 放置过程中产生气体的化学方程式是
放置过程中产生气体的化学方程式是
您最近一年使用:0次
名校
解题方法
4 . 甲烷是重要的资源,通过一系列过程可实现由甲烷到氢气的转化。
Ⅰ.500℃时,CH4与H2O重整主要发生下列反应:
反应1:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.1kJ/mol
CO(g)+3H2(g) ΔH=+206.1kJ/mol
反应2:CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
(1)恒温恒容下,不能证明反应体系已达平衡的是_________
(2)已知:CaO(s)+CO2(g)=CaCO3(s) ΔH=-178.8kJ/mol,向重整反应体系中加入适量多孔CaO,其优点是___________ 。
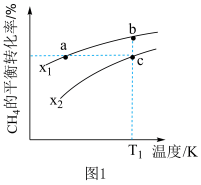
(3)向一恒容密闭容器中加入1molCH4和一定量的H2O,若只发生反应1,CH4的平衡转化率按不同投料x(x=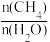 )随温度的变化曲线如图1所示。下列说法不正确的是
)随温度的变化曲线如图1所示。下列说法不正确的是
Ⅱ.CH4与CO2重整的主要反应的热化学方程式为
反应a:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+246.5kJ/mol K1
反应b:H2(g)+CO2(g)=CO(g)+H2O(g) ΔH=+41.2kJ/mol K2
反应c:2CO(g)=CO2(g)+C(s) ΔH=-172.5kJ/mol K3
(4)在CH4与CO2重整体系中通入适量H2O(g),可减少C(s)的生成,反应3CH4(g)+CO2(g)+2H2O(g)=4CO(g)+8H2(g)的ΔH=___________ ,K=___________ (用K1、K2或K3表示)
(5)将1molCH4与1molCO2在2L密闭容器中反应制取CO和H2时,若只发生反应a和反应b,CH4和CO2的平衡转化率随温度变化关系如图2所示。
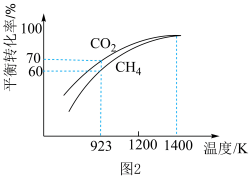
①请列出923K时反应a的化学平衡常数K的计算式(不用计算结果):K=___________ 。
②CH4还原能力R可衡量CO2转化效率,(R=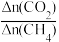 ),同一时段内CO2与CH4的物质的量变化量之比),从平衡移动的角度分析,随着温度升高,R值逐渐减小直至近似等于1的原因是
),同一时段内CO2与CH4的物质的量变化量之比),从平衡移动的角度分析,随着温度升高,R值逐渐减小直至近似等于1的原因是___________ 。
Ⅰ.500℃时,CH4与H2O重整主要发生下列反应:
反应1:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH=+206.1kJ/mol
CO(g)+3H2(g) ΔH=+206.1kJ/mol反应2:CO(g)+H2O(g)
 H2(g)+CO2(g)
H2(g)+CO2(g)(1)恒温恒容下,不能证明反应体系已达平衡的是_________
| A.体系的气体平均相对分子质量不变 |
| B.1molH2O消耗的同时有3molH2消耗 |
| C.体系的压强不再变化 |
| D.CO与H2的物质的量之比不再改变 |
(2)已知:CaO(s)+CO2(g)=CaCO3(s) ΔH=-178.8kJ/mol,向重整反应体系中加入适量多孔CaO,其优点是
(3)向一恒容密闭容器中加入1molCH4和一定量的H2O,若只发生反应1,CH4的平衡转化率按不同投料x(x=
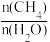 )随温度的变化曲线如图1所示。下列说法不正确的是
)随温度的变化曲线如图1所示。下列说法不正确的是
| A.x1>x2 |
| B.点a、b、c对应的平衡常数:Ka<Kb=Kc |
| C.反应速率:vb正<vc正 |
| D.反应温度为T1,当容器内压强不变时,反应达到平衡状态 |
Ⅱ.CH4与CO2重整的主要反应的热化学方程式为
反应a:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+246.5kJ/mol K1
反应b:H2(g)+CO2(g)=CO(g)+H2O(g) ΔH=+41.2kJ/mol K2
反应c:2CO(g)=CO2(g)+C(s) ΔH=-172.5kJ/mol K3
(4)在CH4与CO2重整体系中通入适量H2O(g),可减少C(s)的生成,反应3CH4(g)+CO2(g)+2H2O(g)=4CO(g)+8H2(g)的ΔH=
(5)将1molCH4与1molCO2在2L密闭容器中反应制取CO和H2时,若只发生反应a和反应b,CH4和CO2的平衡转化率随温度变化关系如图2所示。

①请列出923K时反应a的化学平衡常数K的计算式(不用计算结果):K=
②CH4还原能力R可衡量CO2转化效率,(R=
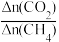 ),同一时段内CO2与CH4的物质的量变化量之比),从平衡移动的角度分析,随着温度升高,R值逐渐减小直至近似等于1的原因是
),同一时段内CO2与CH4的物质的量变化量之比),从平衡移动的角度分析,随着温度升高,R值逐渐减小直至近似等于1的原因是
您最近一年使用:0次
名校
5 . 小组同学探究盐溶液对反应 (血红色)的影响。将
(血红色)的影响。将
 的
的 溶液与
溶液与 的
的 溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
ii. (黄色)
(黄色)
iii.已知 对实验无影响
对实验无影响
下列说法不正确的是
 (血红色)的影响。将
(血红色)的影响。将
 的
的 溶液与
溶液与 的
的 溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。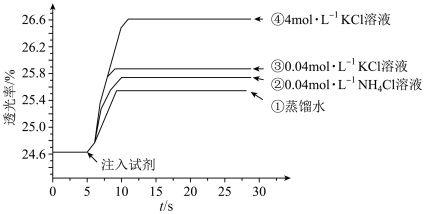
ii.
 (黄色)
(黄色)iii.已知
 对实验无影响
对实验无影响下列说法不正确的是
A.注入试剂①后溶液透光率增大,证明 逆向移动 逆向移动 |
B.透光率③比②高,可能是阳离子种类或溶液 不同导致的 不同导致的 |
C.透光率④比③高,可能发生了反应 |
D.若要证明试剂③中 对平衡体系有影响,还应使用 对平衡体系有影响,还应使用 的 的 溶液进行对照实验 溶液进行对照实验 |
您最近一年使用:0次
2023-11-21更新
|
366次组卷
|
7卷引用:北京市对外经济贸易大学附属中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
6 . 盐碱地是土壤表层集聚过多盐碱成分,对农作物有害的土地。回答下列问题:
(1)盐碱地(含较多 、NaCl)不利于植物生长,盐碱地呈碱性的原因为
、NaCl)不利于植物生长,盐碱地呈碱性的原因为______ (用离子方程式说明);已知25℃时, 的
的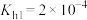 ,则当
,则当 溶液中
溶液中 时,溶液的
时,溶液的
______ 。
(2)已知:常温下,碳酸的电离平衡常数 ,
, 。常温下,向100 mL 0.1 mol⋅L
。常温下,向100 mL 0.1 mol⋅L
 溶液中缓慢滴加100 mL 0.2 mol⋅L
溶液中缓慢滴加100 mL 0.2 mol⋅L 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
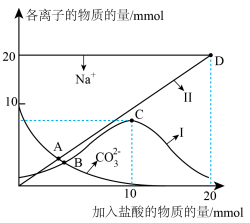
①曲线Ⅰ代表的离子是______ 。
②A、B两点水的电离程度大小为A______ B(填“<”“>”或“=”)。
③根据上图,下列有关说法不正确的是______ 。
a.滴加至B点时,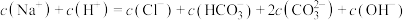
b.滴加至C点时,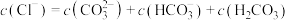
c.滴加至D点时,溶液
④下列事实中,能证明HCN是弱电解质的是______ 。
a.室温下NaCN溶液的
b.HCN溶液导电能力比盐酸弱
c.10 mL 0.1 mol/L的HCN溶液恰好与10 mL 0.1 mol/L的NaOH溶液完全反应
d.取 的HCN溶液,稀释10倍,稀释后
的HCN溶液,稀释10倍,稀释后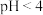
⑤已知HCN电离平衡常数约为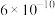 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱______ 。
(1)盐碱地(含较多
 、NaCl)不利于植物生长,盐碱地呈碱性的原因为
、NaCl)不利于植物生长,盐碱地呈碱性的原因为 的
的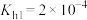 ,则当
,则当 溶液中
溶液中 时,溶液的
时,溶液的
(2)已知:常温下,碳酸的电离平衡常数
 ,
, 。常温下,向100 mL 0.1 mol⋅L
。常温下,向100 mL 0.1 mol⋅L
 溶液中缓慢滴加100 mL 0.2 mol⋅L
溶液中缓慢滴加100 mL 0.2 mol⋅L 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
①曲线Ⅰ代表的离子是
②A、B两点水的电离程度大小为A
③根据上图,下列有关说法不正确的是
a.滴加至B点时,
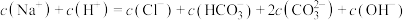
b.滴加至C点时,
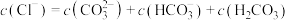
c.滴加至D点时,溶液

④下列事实中,能证明HCN是弱电解质的是
a.室温下NaCN溶液的

b.HCN溶液导电能力比盐酸弱
c.10 mL 0.1 mol/L的HCN溶液恰好与10 mL 0.1 mol/L的NaOH溶液完全反应
d.取
 的HCN溶液,稀释10倍,稀释后
的HCN溶液,稀释10倍,稀释后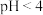
⑤已知HCN电离平衡常数约为
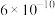 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱
您最近一年使用:0次
名校
解题方法
7 . 某实验小组用如下实验测定海带预处理后所得溶液的碘含量,实验步骤及现象如下:
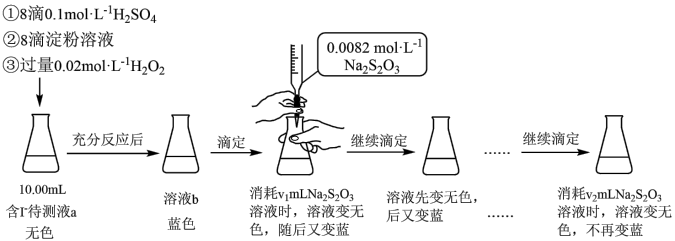
已知:I2+2Na2S2O3=2NaI+Na2S4O6,下列说法不正确 的是:

已知:I2+2Na2S2O3=2NaI+Na2S4O6,下列说法
| A.溶液b为蓝色是因为发生了反应:H2O2+2I-+2H+=I2+2H2O |
| B.该实验可证明蓝色恢复与空气无关 |
| C.溶液反复由无色变蓝的原因可能是H2O2氧化I-的反应速率比Na2S2O3还原I2的反应速率快 |
| D.上述实验不能准确测定待测液中的碘含量,应补充实验步骤:滴定前向溶液b中加少量MnO2,反应至不再产生气泡,过滤,对滤液进行滴定 |
您最近一年使用:0次
2023-11-06更新
|
1274次组卷
|
10卷引用:内蒙古赤峰二中2023-2024学年高二上学期第二次月考化学试题
内蒙古赤峰二中2023-2024学年高二上学期第二次月考化学试题湖南省长沙市长郡中学2023-2024学年高二上学期12月阶段性检测化学试题河北省保定市唐县第一中学2023-2024学年高二上学期1月期末化学试题河南省信阳高级中学2023-2024学年高二上学期元旦测试化学试题北京市丰台区2023-2024学年高三上学期期中练习化学试题(已下线)选择题21-23(已下线)选择题11-14湖北省武昌实验中学2023-2024学年高三上学期12月月考化学试题黑龙江省大庆实验中学实验三部2023-2024学年高三上学期阶段考试(二)化学试题北京实验学校2023-2024学年高三上学期12月化学学科竞赛试题
名校
解题方法
8 . 以 为代表的温室气体大量排放易导致极端天气的出现,减少碳排放,推进碳中和,提升
为代表的温室气体大量排放易导致极端天气的出现,减少碳排放,推进碳中和,提升 的综合利用技术,降低空气中
的综合利用技术,降低空气中 的含量显得刻不容缓。目前
的含量显得刻不容缓。目前 的综合利用技术常用的有如下三种:
的综合利用技术常用的有如下三种:
一、光催化技术
(1)中国广州分析测试中心研究团队在温和条件下用 合成
合成 ,方程式为:
,方程式为: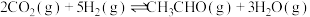
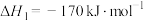
已知生成乙醛的净反应速率为 (
( 、
、 分别表示正、逆反应速率常数)。若在某一温度下
分别表示正、逆反应速率常数)。若在某一温度下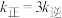 ,则此温度下,上述反应的平衡常数
,则此温度下,上述反应的平衡常数
__________ 。
二、电化学技术
(2)研究证明 也可在熔融碳酸钠中通过电解生成
也可在熔融碳酸钠中通过电解生成 ,收集
,收集 可进行其他有机类合成,化废为宝。则生成
可进行其他有机类合成,化废为宝。则生成 的电极反应式是
的电极反应式是____________________ 。
三、化学催化技术
恒温、体积不变的密闭容器中,加入一定量的 和
和 ,在催化剂下同时发生反应Ⅰ、Ⅱ。
,在催化剂下同时发生反应Ⅰ、Ⅱ。
反应Ⅰ
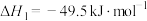
反应Ⅱ
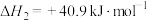
回答下列问题:
(3)下列说法不正确 的是__________。
(4)其他条件相同,仅改变容器体积,实验测得 的平衡产率随着压强的增加而减少,可能原因是
的平衡产率随着压强的增加而减少,可能原因是________________ 。
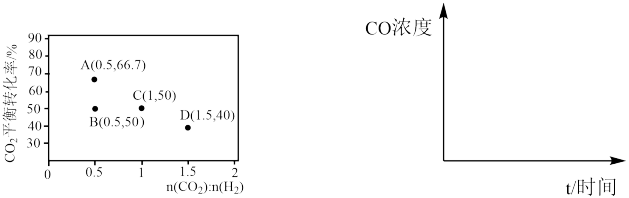
(5)在一定条件下,选择合适的催化剂只进行反应Ⅱ,调整 和
和 初始投料比,测得在一定投料比和一定温度下,
初始投料比,测得在一定投料比和一定温度下, 的平衡转化率如图所示(各点对应的反应温度可能相同,也可能不同)。
的平衡转化率如图所示(各点对应的反应温度可能相同,也可能不同)。
①C、D二点对应的反应温度 、
、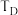 的关系是
的关系是__________ 。
②A、B两点的起始浓度相同,请分别在如图定性画出CO浓度随时间的变化关系,请在曲线上标明 和
和
_______ 。
 为代表的温室气体大量排放易导致极端天气的出现,减少碳排放,推进碳中和,提升
为代表的温室气体大量排放易导致极端天气的出现,减少碳排放,推进碳中和,提升 的综合利用技术,降低空气中
的综合利用技术,降低空气中 的含量显得刻不容缓。目前
的含量显得刻不容缓。目前 的综合利用技术常用的有如下三种:
的综合利用技术常用的有如下三种:一、光催化技术
(1)中国广州分析测试中心研究团队在温和条件下用
 合成
合成 ,方程式为:
,方程式为: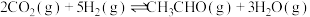
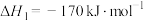
已知生成乙醛的净反应速率为
 (
( 、
、 分别表示正、逆反应速率常数)。若在某一温度下
分别表示正、逆反应速率常数)。若在某一温度下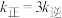 ,则此温度下,上述反应的平衡常数
,则此温度下,上述反应的平衡常数
二、电化学技术
(2)研究证明
 也可在熔融碳酸钠中通过电解生成
也可在熔融碳酸钠中通过电解生成 ,收集
,收集 可进行其他有机类合成,化废为宝。则生成
可进行其他有机类合成,化废为宝。则生成 的电极反应式是
的电极反应式是三、化学催化技术
恒温、体积不变的密闭容器中,加入一定量的
 和
和 ,在催化剂下同时发生反应Ⅰ、Ⅱ。
,在催化剂下同时发生反应Ⅰ、Ⅱ。反应Ⅰ

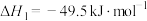
反应Ⅱ

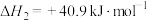
回答下列问题:
(3)下列说法
A.反应Ⅰ的活化能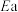 大于反应Ⅱ 大于反应Ⅱ | B.容器内压强不变时可以判断反应达到平衡 |
C.该温度下,反应Ⅱ的 大于零 大于零 | D.使用性能更佳的催化剂可以提高 平衡转化率 平衡转化率 |
 的平衡产率随着压强的增加而减少,可能原因是
的平衡产率随着压强的增加而减少,可能原因是(5)在一定条件下,选择合适的催化剂只进行反应Ⅱ,调整
 和
和 初始投料比,测得在一定投料比和一定温度下,
初始投料比,测得在一定投料比和一定温度下, 的平衡转化率如图所示(各点对应的反应温度可能相同,也可能不同)。
的平衡转化率如图所示(各点对应的反应温度可能相同,也可能不同)。①C、D二点对应的反应温度
 、
、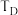 的关系是
的关系是②A、B两点的起始浓度相同,请分别在如图定性画出CO浓度随时间的变化关系,请在曲线上标明
 和
和

您最近一年使用:0次
9 . 某小组同学探究溶液中的 能否被金属钠还原,进行实验:
能否被金属钠还原,进行实验:
①在干燥试管中加入绿豆大小的金属钠,逐滴滴加 溶液,产生无色气体,溶液由紫红色变为浅绿色
溶液,产生无色气体,溶液由紫红色变为浅绿色 。
。
②向 溶液中持续通入
溶液中持续通入 ,水浴加热,溶液颜色无明显变化。
,水浴加热,溶液颜色无明显变化。
③向 溶液中加入
溶液中加入 固体,溶液由紫红色变为浅绿色。
固体,溶液由紫红色变为浅绿色。
下列说法不正确 的是
 能否被金属钠还原,进行实验:
能否被金属钠还原,进行实验:①在干燥试管中加入绿豆大小的金属钠,逐滴滴加
 溶液,产生无色气体,溶液由紫红色变为浅绿色
溶液,产生无色气体,溶液由紫红色变为浅绿色 。
。②向
 溶液中持续通入
溶液中持续通入 ,水浴加热,溶液颜色无明显变化。
,水浴加热,溶液颜色无明显变化。③向
 溶液中加入
溶液中加入 固体,溶液由紫红色变为浅绿色。
固体,溶液由紫红色变为浅绿色。下列说法
| A.实验①中还可能观察到钠块浮在溶液表面,剧烈燃烧,发出黄色火焰 |
| B.实验②中的现象说明实验①中溶液变色的原因与产生的气体无关 |
C.实验③中的现象说明实验①中可能发生的反应: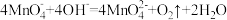 |
D.上述实验能证明溶液中的 可以被金属钠还原 可以被金属钠还原 |
您最近一年使用:0次
2023-05-07更新
|
1689次组卷
|
7卷引用:湖南省邵阳市第二中学2023-2024学年高二上学期基础知识竞赛化学试题
湖南省邵阳市第二中学2023-2024学年高二上学期基础知识竞赛化学试题北京市海淀区2022-2023学年高三第二次模拟(下学期期末)考试化学试题(已下线)T12-化学反应及限度(已下线)第4讲 钠及其重要化合物北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题(已下线)选择题11-14(已下线)选择题6-10
10 . 化学小组研究 的性质,完成如下实验:
的性质,完成如下实验: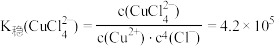 ;
;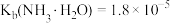 ;
;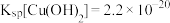
下列说法不正确 的是
 的性质,完成如下实验:
的性质,完成如下实验: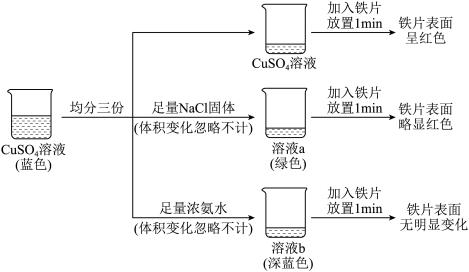
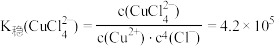 ;
;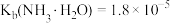 ;
;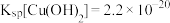
下列说法
A. 溶液中加入NaCl固体: 溶液中加入NaCl固体: |
B.溶液a中加入浓氨水时不可能出现 蓝色沉淀 蓝色沉淀 |
C.溶液a、b中铁片的颜色不同证明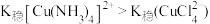 |
D.溶液b中加入足量乙醇时可以析出深蓝色晶体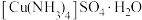 |
您最近一年使用:0次
2023-07-12更新
|
335次组卷
|
5卷引用:北京朝阳区2022-2023学年高二下学期期末考试化学试题
北京朝阳区2022-2023学年高二下学期期末考试化学试题辽宁省实验中学2023-2024学年高二下学期第一次月考化学试题(已下线)题型突破01 有机实验(选择题)-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(北京专用)北京市第三十五中学2023-2024学年高二下学期期中考试化学试题北京师范大学良乡附中2023-2024学年高三上学期10月月考化学试题



