1 . 磷酸是重要的化学试剂和工业原料。回答下列问题:
(1)已知:25℃时,磷酸和氢氟酸的电离常数如下表所示。
向NaF溶液中滴加少量 溶液,反应的离子方程式为
溶液,反应的离子方程式为___________ 。
(2)已知:
Ⅰ. CaO(s)+H2SO4(l) CaSO4(s)+H2O(l)
CaSO4(s)+H2O(l) 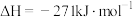
Ⅱ.

①工业上用 和硫酸反应制备磷酸的热化学方程式为
和硫酸反应制备磷酸的热化学方程式为___________ 。
②一定条件下,在密闭容器中只发生反应Ⅱ,达到平衡后缩小容器容积,HF的平衡转化率___________ (填“增大”“减小”“不变”,下同);HF的平衡浓度___________ 。
(3)工业上用磷尾矿制备 时生成的副产物CO可用于制备
时生成的副产物CO可用于制备 ,原理为
,原理为

①一定温度下,向10L密闭容器中充入0.5molCO和 ,2min达到平衡时,测得0~2min内用
,2min达到平衡时,测得0~2min内用 表示的反应速率
表示的反应速率 ,则CO的平衡转化率
,则CO的平衡转化率
___________ ,该反应的平衡常数K=___________ 。
②在压强不变的密闭容器中发生上述反应,设起始的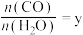 ,CO的平衡体积分数
,CO的平衡体积分数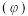 与温度(T)的关系如图所示。
与温度(T)的关系如图所示。

则:该反应的
___________ 0(填“>”“<”或“=”,下同),a___________ 1。
(1)已知:25℃时,磷酸和氢氟酸的电离常数如下表所示。
| 物质 |  |  |
| 电离常数 |  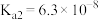 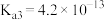 |  |
 溶液,反应的离子方程式为
溶液,反应的离子方程式为(2)已知:
Ⅰ. CaO(s)+H2SO4(l)
 CaSO4(s)+H2O(l)
CaSO4(s)+H2O(l) 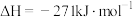
Ⅱ.


①工业上用
 和硫酸反应制备磷酸的热化学方程式为
和硫酸反应制备磷酸的热化学方程式为②一定条件下,在密闭容器中只发生反应Ⅱ,达到平衡后缩小容器容积,HF的平衡转化率
(3)工业上用磷尾矿制备
 时生成的副产物CO可用于制备
时生成的副产物CO可用于制备 ,原理为
,原理为

①一定温度下,向10L密闭容器中充入0.5molCO和
 ,2min达到平衡时,测得0~2min内用
,2min达到平衡时,测得0~2min内用 表示的反应速率
表示的反应速率 ,则CO的平衡转化率
,则CO的平衡转化率
②在压强不变的密闭容器中发生上述反应,设起始的
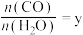 ,CO的平衡体积分数
,CO的平衡体积分数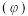 与温度(T)的关系如图所示。
与温度(T)的关系如图所示。
则:该反应的

您最近一年使用:0次
名校
2 .  排放到空气中会引起酸雨等环境问题,严重危害人类健康,
排放到空气中会引起酸雨等环境问题,严重危害人类健康, 水溶液中存在下列平衡:
水溶液中存在下列平衡:
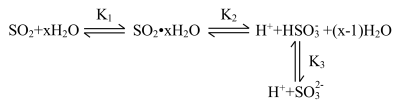
已知: ,
, ,
, 为各步反应的平衡常数,且
为各步反应的平衡常数,且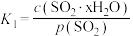 [
[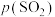 表示
表示 的平衡压强]。下列说法正确的是
的平衡压强]。下列说法正确的是
 排放到空气中会引起酸雨等环境问题,严重危害人类健康,
排放到空气中会引起酸雨等环境问题,严重危害人类健康, 水溶液中存在下列平衡:
水溶液中存在下列平衡: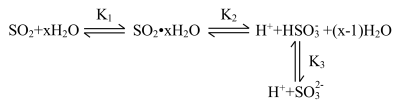
已知:
 ,
, ,
, 为各步反应的平衡常数,且
为各步反应的平衡常数,且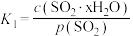 [
[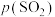 表示
表示 的平衡压强]。下列说法正确的是
的平衡压强]。下列说法正确的是A.由上图平衡可知 溶液和 溶液和 溶液都可以水解,溶液一定呈碱性 溶液都可以水解,溶液一定呈碱性 |
B.氨水也可吸收 ,防止大气污染,同时通入 ,防止大气污染,同时通入 能进一步提高 能进一步提高 去除率 去除率 |
C.当 的平衡压强为p时,测得 的平衡压强为p时,测得 ,则溶液 ,则溶液 |
D.用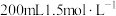 的氢氧化钠溶液吸收0.2mol的 的氢氧化钠溶液吸收0.2mol的 ,则溶液中存在关系式: ,则溶液中存在关系式: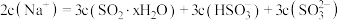 |
您最近一年使用:0次
名校
3 . 温度为 时,在三个容积均为1L的恒容密闭容器中均发生反应:
时,在三个容积均为1L的恒容密闭容器中均发生反应: (正反应吸热)。实验测得:
(正反应吸热)。实验测得: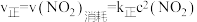 ,
,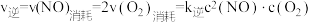 ,
, 、
、 为速率常数,受温度影响。
为速率常数,受温度影响。
下列说法正确的是
 时,在三个容积均为1L的恒容密闭容器中均发生反应:
时,在三个容积均为1L的恒容密闭容器中均发生反应: (正反应吸热)。实验测得:
(正反应吸热)。实验测得: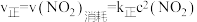 ,
,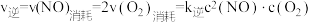 ,
, 、
、 为速率常数,受温度影响。
为速率常数,受温度影响。| 容器编号 | 物质的起始浓度( ) ) | 物质的平衡浓度( ) ) | ||
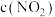 | 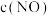 | 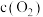 |
| |
| Ⅰ | 0.6 | 0 | 0 | 0.2 |
| Ⅱ | 0.3 | 0.5 | 0.2 | |
| Ⅲ | 0 | 0.5 | 0.35 | |
A.容器Ⅱ达到平衡前 |
B.达到平衡时,容器Ⅲ中 的体积分数大于50% 的体积分数大于50% |
C.设K为该反应的化学平衡常数,则有 |
D.当温度改变为 时,若 时,若 ,则 ,则 |
您最近一年使用:0次
2023-07-16更新
|
595次组卷
|
4卷引用:福建省宁德市第一中学2021-2022学年高二上学期10月月考化学试题
4 . 双酚A是重要的有机化工原料,工业上可以用苯酚和丙酮合成双酚A:
2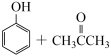
 H2O+
H2O+
(1)丙酮含氧官能团名称为______ ;双酚A的分子式为______ 。
(2)双酚A分子中共平面的碳原子最多可以有______ 个。
(3)在盐酸或氨水催化下,苯酚和甲醛混合共热可得到酚醛树脂:
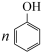 +nHCHO
+nHCHO (n-1)H2O+
(n-1)H2O+
关于该反应及相关物质的判断正确的是_____ (填字母)。
A.甲醛可溶于水
B.该反应属于缩聚反应
C.甲醛防腐可用于保存海鲜
D.酚醛树脂常用于制造电器材料
E.苯酚的酸性介于醋酸和盐酸之间
(4)苯酚可用于合成酚酞:

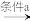 A
A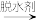 B
B
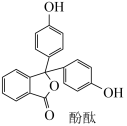
已知:2HCOOH H2O+
H2O+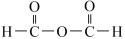
①邻二甲苯核磁共振氢谱有______ 组峰。
②条件a是______ 。
③A→B反应的化学方程式为______ 。
2
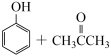
 H2O+
H2O+
(1)丙酮含氧官能团名称为
(2)双酚A分子中共平面的碳原子最多可以有
(3)在盐酸或氨水催化下,苯酚和甲醛混合共热可得到酚醛树脂:
 +nHCHO
+nHCHO (n-1)H2O+
(n-1)H2O+
关于该反应及相关物质的判断正确的是
A.甲醛可溶于水
B.该反应属于缩聚反应
C.甲醛防腐可用于保存海鲜
D.酚醛树脂常用于制造电器材料
E.苯酚的酸性介于醋酸和盐酸之间
(4)苯酚可用于合成酚酞:

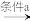 A
A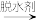 B
B

已知:2HCOOH
 H2O+
H2O+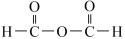
①邻二甲苯核磁共振氢谱有
②条件a是
③A→B反应的化学方程式为
您最近一年使用:0次
2023-02-14更新
|
436次组卷
|
5卷引用:福建省福州市2021届高中毕业班4月质量检测化学试题
福建省福州市2021届高中毕业班4月质量检测化学试题(已下线)第35讲 生命中的基础有机化学物质 合成有机高分子(精练)-2022年高考化学一轮复习讲练测河北省迁安市第三中学2020-2021学年高二下学期期中考试化学试题(已下线)第九章 有机化学基础 第61练 生命中的基础有机化学物质 合成有机高分子(已下线)第5讲 生物大分子 合成高分子
名校
5 . 常温下, 的溶液A中含有
的溶液A中含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的四种,且溶液中各离子的浓度均为0.1
中的四种,且溶液中各离子的浓度均为0.1 。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确的是
。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确的是
 的溶液A中含有
的溶液A中含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的四种,且溶液中各离子的浓度均为0.1
中的四种,且溶液中各离子的浓度均为0.1 。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确的是
。现取该溶液进行有关实验,实验结果如图所示。下列有关说法正确的是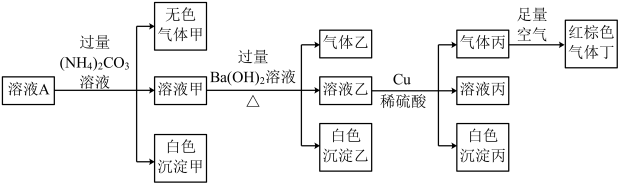
A.溶液A中一定含有 、 、 、 、 、 、 |
B.若实验消耗 14.4g,则生成气体丁的体积为3.36L 14.4g,则生成气体丁的体积为3.36L |
C.沉淀乙中一定有 ,可能有 ,可能有 |
D.溶液A中一定没有 ,但是无法确定是否含有 ,但是无法确定是否含有 |
您最近一年使用:0次
2023-02-08更新
|
242次组卷
|
17卷引用:福建省龙岩第一中学2021-2022学年高三上学期第三次月考化学试题
福建省龙岩第一中学2021-2022学年高三上学期第三次月考化学试题湖南省新高考联盟2021届高三下学期3月提升检测化学(A)试题安徽省名校2020-2021学年高二下学期5月第二次联考化学试题陕西省西安中学2021-2022学年高三上学期期中考试化学试题河南省豫南豫北名校2018届高三精英联赛化学试题1江西省莲塘一中、临川二中2018届高三上学期第一次联考化学试题(已下线)黄金30题系列 高三化学 小题易丢分陕西省陕师大附中2018届高三第五次月考化学试题河南省南阳市第一中学校2018届高三第七次考试理综化学试题河北省定州中学2018届高三(承智班)下学期开学考试化学试题河南省豫南豫北名校2018届高三精英联赛化学试题2西藏自治区拉萨中学2018届高三第六次月考理综化学试题(已下线)三轮冲刺卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)湖南省常德市第一中学 2023届高三7月摸底考试化学试题(已下线)易错点03 离子反应-备战2023年高考化学考试易错题(已下线)学科特色6 离子推断湖南省永州市祁阳县第四中学2023-2024学年高三上学期第三次段考化学试题
名校
解题方法
6 . 某兴趣小组对84消毒液的组成、性质与使用进行探究。所用试剂:84 消毒液(NaClO 浓度为 )、医用酒精(乙醇体积分数为
)、医用酒精(乙醇体积分数为 )
)
Ⅰ:探究84 消毒液的成分
(1)实测该84消毒液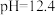 ,能使pH试纸
,能使pH试纸_______ ,因此其成分中,除了NaCl、NaC1O,还含有少量_______ (填化学式)。
(2)84消毒液露置于空气中,消毒效果先增强后降低。消毒效果增强的原因是_______ 。
Ⅱ:探究 84 消毒液的性质与使用
(3)84消毒液具有氧化性,预测的依据是________ 。巴西奥运会期间,由于工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长该反应的离子方程式为_______ 。
Ⅲ:84消毒液能否与医用酒精混用实验装置如图所示
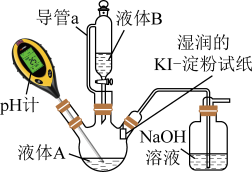
(4)导管 a 的作用是_______ 。
(5)实验ⅰ的目的是_______ 。
(6)判断实验ⅱ中生成了 的依据是
的依据是_______ 。
(7)实验过程,混合溶液的pH逐渐增大至13.1,预测酒精与NaClO反应还可能生成NaOH ,
但需补充以下实验ⅲ,才能说明反应中是有NaOH生成。填写表中空白完成实验设计。
结论:医用酒精可与84消毒液发生反应,二者不可混用。
 )、医用酒精(乙醇体积分数为
)、医用酒精(乙醇体积分数为 )
)Ⅰ:探究84 消毒液的成分
(1)实测该84消毒液
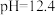 ,能使pH试纸
,能使pH试纸(2)84消毒液露置于空气中,消毒效果先增强后降低。消毒效果增强的原因是
Ⅱ:探究 84 消毒液的性质与使用
(3)84消毒液具有氧化性,预测的依据是
Ⅲ:84消毒液能否与医用酒精混用实验装置如图所示

| 序号 | 液体A | 液体B | 现象 |
| ⅰ |  ( (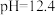 )的84消毒液 )的84消毒液 |  蒸馏水 蒸馏水 | 溶液中无明显现象;溶液 变为12.0; 变为12.0;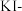 淀粉试纸在 淀粉试纸在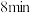 时变蓝, 时变蓝, 时蓝色完全褪去 时蓝色完全褪去 |
| ⅱ |  ( (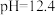 )的84消毒液 )的84消毒液 |  医用酒精 医用酒精 | 产生气泡,颜色无明显变化;溶液 升高到13.1, 升高到13.1,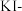 淀粉试纸在 淀粉试纸在 时变蓝, 时变蓝, 时蓝色完全褪去 时蓝色完全褪去 |
(5)实验ⅰ的目的是
(6)判断实验ⅱ中生成了
 的依据是
的依据是(7)实验过程,混合溶液的pH逐渐增大至13.1,预测酒精与NaClO反应还可能生成NaOH ,
但需补充以下实验ⅲ,才能说明反应中是有NaOH生成。填写表中空白完成实验设计。
| 序号 | 液体A | 液体B | 现象 |
| ⅲ |  医用酒精 医用酒精 | 溶液 升高到12.6 升高到12.6 |
您最近一年使用:0次
2022-12-24更新
|
194次组卷
|
2卷引用:福建省宁德第一中学2021-2022学年高一上学期12月月考化学试题
7 . 回答下列问题:
(1)氨水中存在:NH3·H2O
 +OH-,在5份0.01 mol∙L−1的氨水中分别加入下列物质:A.浓氨水,B.纯水,C.少量NaOH固体, D.NH4Cl固体。按照要求填空(答案选填物质对应的字母):
+OH-,在5份0.01 mol∙L−1的氨水中分别加入下列物质:A.浓氨水,B.纯水,C.少量NaOH固体, D.NH4Cl固体。按照要求填空(答案选填物质对应的字母):
①电离平衡会向正向移动是_______ 。
②c( )、c(OH-)都增大的是
)、c(OH-)都增大的是_______ 。
③c( )增大,c(OH-)减小的是
)增大,c(OH-)减小的是_______ 。
④c( )减小,c(OH-)增大的是
)减小,c(OH-)增大的是_______ 。
(2)将6 g CH3COOH溶于水制成1 L溶液,此溶液的物质的量浓度为_______ ,若此温度下醋酸的电离常数K=1×10−5,c(H+)为_______ ,若升高温度, K将_______ (填“变大”、“变小”或“不变”)。
(3)现有浓度均为0.1 mol∙L−1的盐酸、硫酸、醋酸三种溶液,回答下列问题:
①若三种溶液中c(H+)分别为a mol∙L−1、b mol∙L−1、c mol∙L−1,则它们的大小关系为_______ 。
②等体积的以上三种酸分别与过量的NaOH溶液反应,若生成的盐的物质的量依次为A mol、B mol、C mol,则它们的大小关系为_______ 。
(4)现有c(H+)= 1×10−3 mol∙L−1的盐酸、硫酸、醋酸三种溶液,回答下列问题:
①分别用以上三种酸中和一定量的NaOH溶液生成正盐,若需要酸的体积分别为V1、V2、V3,其大小关系为_______ 。
②分别与Zn反应,开始时生成H2的速率为v1、v2、v3,其大小关系为_______ 。
(1)氨水中存在:NH3·H2O

 +OH-,在5份0.01 mol∙L−1的氨水中分别加入下列物质:A.浓氨水,B.纯水,C.少量NaOH固体, D.NH4Cl固体。按照要求填空(答案选填物质对应的字母):
+OH-,在5份0.01 mol∙L−1的氨水中分别加入下列物质:A.浓氨水,B.纯水,C.少量NaOH固体, D.NH4Cl固体。按照要求填空(答案选填物质对应的字母):①电离平衡会向正向移动是
②c(
 )、c(OH-)都增大的是
)、c(OH-)都增大的是③c(
 )增大,c(OH-)减小的是
)增大,c(OH-)减小的是④c(
 )减小,c(OH-)增大的是
)减小,c(OH-)增大的是(2)将6 g CH3COOH溶于水制成1 L溶液,此溶液的物质的量浓度为
(3)现有浓度均为0.1 mol∙L−1的盐酸、硫酸、醋酸三种溶液,回答下列问题:
①若三种溶液中c(H+)分别为a mol∙L−1、b mol∙L−1、c mol∙L−1,则它们的大小关系为
②等体积的以上三种酸分别与过量的NaOH溶液反应,若生成的盐的物质的量依次为A mol、B mol、C mol,则它们的大小关系为
(4)现有c(H+)= 1×10−3 mol∙L−1的盐酸、硫酸、醋酸三种溶液,回答下列问题:
①分别用以上三种酸中和一定量的NaOH溶液生成正盐,若需要酸的体积分别为V1、V2、V3,其大小关系为
②分别与Zn反应,开始时生成H2的速率为v1、v2、v3,其大小关系为
您最近一年使用:0次
8 . 以软锰矿粉(主要含MnO2,还含有少量的Fe2O3、Al2O3等杂质)为原料制取高纯MnO2的流程如下:

(1)酸浸时MnO2参与反应的离子方程式为_______ 。
(2)酸浸时加入一定体积的硫酸,硫酸浓度不能过小或过大。当硫酸浓度偏小时,酸浸时会有红褐色渣出现,原因是_______ 。硫酸浓度不能过大的原因是_______ 。
(3)过滤II所得滤渣为MnCO3,滤液中溶质的主要成分是_______ 。
(4)焙烧MnCO3的装置如下图所示:

①焙烧时所发生反应的化学方程式为_______ 。
②焙烧一定时间后需转动石英管,目的是_______ 。
(5)工业上采用间接氧化还原滴定法测定MnO2纯度,其操作过程如下:准确称量0.9200g该样品,与足量酸性KI溶液充分反应后,配制成100mL溶液。取其中20.00mL,恰好与25.00mL0.0800mol•L-1Na2S2O3溶液反应(I2+2 =2I-+
=2I-+ )。计算可得该样品纯度为
)。计算可得该样品纯度为_______ 。

(1)酸浸时MnO2参与反应的离子方程式为
(2)酸浸时加入一定体积的硫酸,硫酸浓度不能过小或过大。当硫酸浓度偏小时,酸浸时会有红褐色渣出现,原因是
(3)过滤II所得滤渣为MnCO3,滤液中溶质的主要成分是
(4)焙烧MnCO3的装置如下图所示:

①焙烧时所发生反应的化学方程式为
②焙烧一定时间后需转动石英管,目的是
(5)工业上采用间接氧化还原滴定法测定MnO2纯度,其操作过程如下:准确称量0.9200g该样品,与足量酸性KI溶液充分反应后,配制成100mL溶液。取其中20.00mL,恰好与25.00mL0.0800mol•L-1Na2S2O3溶液反应(I2+2
 =2I-+
=2I-+ )。计算可得该样品纯度为
)。计算可得该样品纯度为
您最近一年使用:0次
解题方法
9 . 磷化硼是一种典型的超硬无机材料,常以BCl3,PH3为原料制备。
回答下列问题:
(1)基态P原子与B原子中未成对电子数之比为______ 。P在周期表中的位置___________________
(2)PH3分子的立体结构为________ ;PH3沸点______ (填"高于"或“低于")NH3,理由是__________________ 。
(3)BCl3、PCl3和PF3三种分子中键角由大到小的顺序为_________________ 。
(4)BCl3可转化为硼酸,硼酸为一元弱酸的原因是__________________________________ 。(用电离方程式表示)。
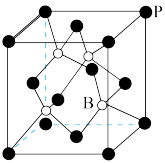
(5)磷化硼晶胞如图所示,其中黑球表示P原子,白球表示B原子,晶胞中磷原子空间堆积方式为______________ 。已知磷化硼晶体的密度为ρg·cm-3,设阿伏加德罗常数的值为NA,则晶胞中B与P间最短距离为_______________ pm。
回答下列问题:
(1)基态P原子与B原子中未成对电子数之比为
(2)PH3分子的立体结构为
(3)BCl3、PCl3和PF3三种分子中键角由大到小的顺序为
(4)BCl3可转化为硼酸,硼酸为一元弱酸的原因是
(5)磷化硼晶胞如图所示,其中黑球表示P原子,白球表示B原子,晶胞中磷原子空间堆积方式为

您最近一年使用:0次
解题方法
10 . 电解原理在化学工业中有广泛应用。
(1)利用图装置电解制备NaOH,两电极区电解液分别为NaOH和NaCl溶液。
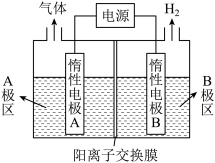
①B极区电解液为__________ 溶液(填化学式),A极要连接电源的________ (填“正”或“负”)极。
②阳极电极反应式为____________________________ ,电解过程中Na+向___________ 电极迁移(填“A”或“B”)。
③电解总反应的离子方程式 是_________________________ 。
(2)利用图装置,可以模拟铁的电化学防护。
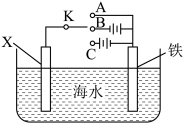
①若X为碳电极,为减缓铁的腐蚀,开关K应置于______ 处。(填“A”、“B”或“C”)
②若X为锌电极,开关K置于A处,该电化学防护法称为_____________ 。
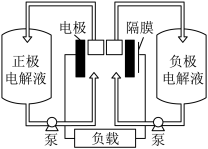
(3)全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟。如图是钒电池示意图。钒电池是以溶解于一定浓度硫酸溶液中的不同价态的钒离子为正极电极反应的活性物质(VO2+、VO )和负极电极反应的活性物质(V2+、V3+),电池总反应为:V2++VO
)和负极电极反应的活性物质(V2+、V3+),电池总反应为:V2++VO +2H+
+2H+ VO2++V3++H2O。放电时的正极反应式为
VO2++V3++H2O。放电时的正极反应式为__________________________________ 。能够通过钒电池基本工作原理示意图中“隔膜”的离子是___________ 。
(1)利用图装置电解制备NaOH,两电极区电解液分别为NaOH和NaCl溶液。

①B极区电解液为
②阳极电极反应式为
③电解总反应的
(2)利用图装置,可以模拟铁的电化学防护。

①若X为碳电极,为减缓铁的腐蚀,开关K应置于
②若X为锌电极,开关K置于A处,该电化学防护法称为
(3)全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟。如图是钒电池示意图。钒电池是以溶解于一定浓度硫酸溶液中的不同价态的钒离子为正极电极反应的活性物质(VO2+、VO
 )和负极电极反应的活性物质(V2+、V3+),电池总反应为:V2++VO
)和负极电极反应的活性物质(V2+、V3+),电池总反应为:V2++VO +2H+
+2H+ VO2++V3++H2O。放电时的正极反应式为
VO2++V3++H2O。放电时的正极反应式为
您最近一年使用:0次



