1 . 常温下0.2mol•L-1NaHCO3溶液与0.1mol•L-1Na2CO3溶液等体积混合后,下列关于说法不正确 的是
A.NaHCO3=Na++ | B.c(Na+)>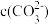 > > >c(OH-) >c(OH-) |
C.c(H+)+c(Na+)=c(OH-)+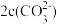 + + | D.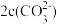 + + + +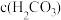 <c(Na+) <c(Na+) |
您最近一年使用:0次
名校
2 . 氨的催化氧化反应是硝酸工业中的重要反应,某条件下 与
与 作用时可发生如下3个反应:
作用时可发生如下3个反应:
Ⅰ.
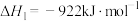
Ⅱ.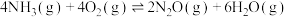
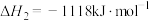
Ⅲ.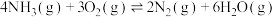

已知:298K时,相关物质的焓的数据如图。
___________  。
。
(2)将一定比例的 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性与温度的关系如图所示。
的选择性与温度的关系如图所示。 适宜的温度为 210℃左右。
适宜的温度为 210℃左右。
②随着温度的升高, 的选择性下降的原因可能为
的选择性下降的原因可能为___________ 。
(3)在一定温度下,氨气溶于水的过程及其平衡常数为:
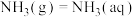

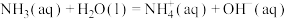

其中p为 的平衡压强,
的平衡压强, 为
为 在水溶液中的平衡浓度。设氨气在水中的溶解度
在水溶液中的平衡浓度。设氨气在水中的溶解度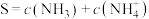 ,则用p、
,则用p、 和
和 表示S的代数式为
表示S的代数式为___________ 。
(4)由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一。
人工合成淀粉(节选途径见图)中的重要反应之一。
已知: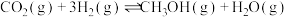 的
的 -49.5kJ/mol
-49.5kJ/mol
反应②:

反应③: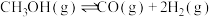
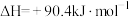
Ⅰ.反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。___________  。
。
Ⅱ.某研究小组采用上述催化剂,向密闭容器中通入
 和
和
 ,只发生反应①和反应②,在不同条件下达到平衡,在
,只发生反应①和反应②,在不同条件下达到平衡,在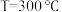 下甲醇的物质的量分数
下甲醇的物质的量分数 随压强
随压强 的变化、在
的变化、在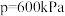 下
下 随温度
随温度 的变化,如下图所示。
的变化,如下图所示。 点对应的温度和压强分别为200℃、600
点对应的温度和压强分别为200℃、600 。
。
ii. 点
点 的分压为
的分压为___________  ,此时容器中
,此时容器中 为
为 ,
, 为
为 ,反应①的压强平衡常数
,反应①的压强平衡常数
___________  (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
iii.图中 点的
点的 高于
高于 点的原因是
点的原因是___________ 。
 与
与 作用时可发生如下3个反应:
作用时可发生如下3个反应:Ⅰ.

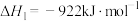
Ⅱ.
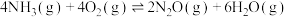
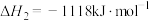
Ⅲ.
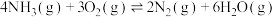

已知:298K时,相关物质的焓的数据如图。


 。
。(2)将一定比例的
 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性与温度的关系如图所示。
的选择性与温度的关系如图所示。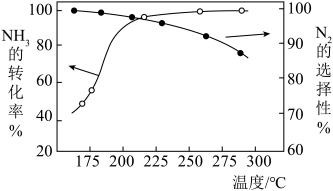
 适宜的温度为 210℃左右。
适宜的温度为 210℃左右。②随着温度的升高,
 的选择性下降的原因可能为
的选择性下降的原因可能为(3)在一定温度下,氨气溶于水的过程及其平衡常数为:
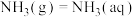

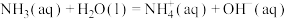

其中p为
 的平衡压强,
的平衡压强, 为
为 在水溶液中的平衡浓度。设氨气在水中的溶解度
在水溶液中的平衡浓度。设氨气在水中的溶解度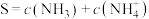 ,则用p、
,则用p、 和
和 表示S的代数式为
表示S的代数式为(4)由
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一。
人工合成淀粉(节选途径见图)中的重要反应之一。已知:
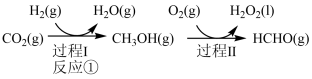
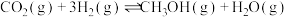 的
的 -49.5kJ/mol
-49.5kJ/mol反应②:


反应③:
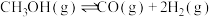
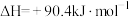
Ⅰ.反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。
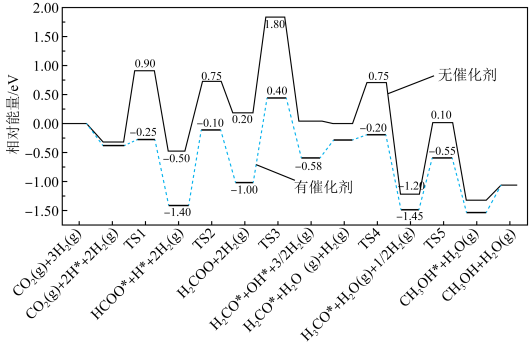
 。
。Ⅱ.某研究小组采用上述催化剂,向密闭容器中通入

 和
和
 ,只发生反应①和反应②,在不同条件下达到平衡,在
,只发生反应①和反应②,在不同条件下达到平衡,在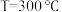 下甲醇的物质的量分数
下甲醇的物质的量分数 随压强
随压强 的变化、在
的变化、在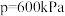 下
下 随温度
随温度 的变化,如下图所示。
的变化,如下图所示。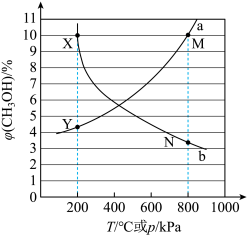
 点对应的温度和压强分别为200℃、600
点对应的温度和压强分别为200℃、600 。
。ii.
 点
点 的分压为
的分压为 ,此时容器中
,此时容器中 为
为 ,
, 为
为 ,反应①的压强平衡常数
,反应①的压强平衡常数
 (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。iii.图中
 点的
点的 高于
高于 点的原因是
点的原因是
您最近一年使用:0次
名校
3 . 实验室以含锌废液(主要成分为ZnSO4,含少量的Fe2+、Mn2+)为原料制备ZnCO3·2Zn(OH)2的实验流程如下:
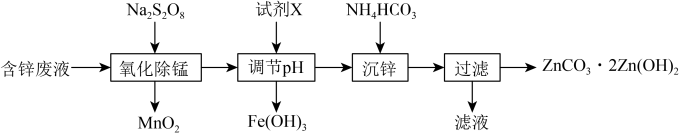
| A.溶液中的Fe2+可以用KSCN溶液检验 |
B.氧化除锰后的溶液中存在:Na+、Zn2+、Fe2+、SO |
| C.调节pH时试剂X可以选用Zn、ZnO、ZnCO3等物质 |
D.沉锌时的离子方程式为3Zn2++6HCO = ZnCO3·2Zn(OH)2↓+5CO2↑+H2O = ZnCO3·2Zn(OH)2↓+5CO2↑+H2O |
您最近一年使用:0次
4 . 现有如图所示的转化关系,已知:A为高级脂肪酸甘油酯。回答下列问题:___________ ,D的结构简式为___________ 。
(2)①的化学方程式为________________ ;③的反应类型为________ 反应。
(3)完全燃烧等物质的量的B和某烷烃消耗等量的氧气,则该烷烃的名称为___________ 。
(4)m g某天然油脂完全水解需要18gNaOH,则m g该油脂的物质的量为___________ mol。
(5)一定量的CH3COOH和O2混合后完全反应生成CO2、CO和H2O(g)。产物分别经过浓硫酸和碱石灰,浓硫酸增重10.8g,碱石灰增重13.2g。则n(CH3COOH)︰n(O2)=___________ 。

(2)①的化学方程式为
(3)完全燃烧等物质的量的B和某烷烃消耗等量的氧气,则该烷烃的名称为
(4)m g某天然油脂完全水解需要18gNaOH,则m g该油脂的物质的量为
(5)一定量的CH3COOH和O2混合后完全反应生成CO2、CO和H2O(g)。产物分别经过浓硫酸和碱石灰,浓硫酸增重10.8g,碱石灰增重13.2g。则n(CH3COOH)︰n(O2)=
您最近一年使用:0次
名校
5 . 关于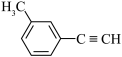 的说法正确的是
的说法正确的是
| A.分子中有6个原子共线 | B.分子中共平面的原子数目最多为14 |
| C.分子中的苯环由单双键交替组成 | D.该有机物的一氯代物有两种 |
您最近一年使用:0次
名校
6 . 下列选项中除杂试剂或操作正确的是
选项 | 物质(杂质) | 除杂试剂或操作 |
A | 甲烷(丙烯) | 酸性高锰酸钾溶液 |
B | 乙酸乙酯(乙醇) | 浓硫酸、乙酸、加热 |
C | 二氧化硫(乙烯) | 溴水 |
D | 蛋白质溶液(NaCl) | 渗析 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-20更新
|
977次组卷
|
3卷引用:江西省南昌十九中2021-2022学年高一下学期第三次月考化学试卷
名校
7 . 环境科学研究发现, 也是一种温室效应气体,与
也是一种温室效应气体,与 相比,虽然
相比,虽然 在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。
在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。 的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为
的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为__________ ;在相同温度和压强下,1mol  和1mol CO经过相同反应时间测得如下实验数据:
和1mol CO经过相同反应时间测得如下实验数据:
试分析在相同温度时,催化剂2催化下 的转化率更高的原因是
的转化率更高的原因是___________ 。
(2)在容积均为1L的密闭容器A(起始500℃,恒温)、B(起始500℃,绝热)两个容器中分别加入0.1mol 、0.4mol CO和相同催化剂。实验测得A、B容器中
、0.4mol CO和相同催化剂。实验测得A、B容器中 的转化率随时间的变化关系如图所示:
的转化率随时间的变化关系如图所示: 的转化率随时间的变化关系是图中的
的转化率随时间的变化关系是图中的___________ 曲线(填“a”或“b”)。
②要缩短b曲线对应容器达到平衡的时间,但不改变 的平衡转化率,在催化剂一定的情况下可采取的措施是
的平衡转化率,在催化剂一定的情况下可采取的措施是___________ (答出一条即可)。
③500℃该反应的化学平衡常数K=___________ (用最简分数表示)。
④实验测定该反应的反应速率 ,
, ,
, 、
、 分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
___________ (保留两位小数)。
 也是一种温室效应气体,与
也是一种温室效应气体,与 相比,虽然
相比,虽然 在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。
在大气中的含量很低,增温潜势却是二氧化碳的298倍,对全球气候的增温效应在未来将越来越显著,已引起科学家的极大关注。
 的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为
的能量变化如上图所示,则无催化剂条件下该反应的逆反应的活化能为 和1mol CO经过相同反应时间测得如下实验数据:
和1mol CO经过相同反应时间测得如下实验数据:| 实验 | 温度/℃ | 催化剂 |  的转化率/% 的转化率/% |
| 实验1 | 400 | 催化剂1 | 9.5 |
| 400 | 催化剂2 | 10.6 | |
| 实验2 | 500 | 催化剂1 | 12.3 |
| 500 | 催化剂2 | 13.5 |
 的转化率更高的原因是
的转化率更高的原因是(2)在容积均为1L的密闭容器A(起始500℃,恒温)、B(起始500℃,绝热)两个容器中分别加入0.1mol
 、0.4mol CO和相同催化剂。实验测得A、B容器中
、0.4mol CO和相同催化剂。实验测得A、B容器中 的转化率随时间的变化关系如图所示:
的转化率随时间的变化关系如图所示:
 的转化率随时间的变化关系是图中的
的转化率随时间的变化关系是图中的②要缩短b曲线对应容器达到平衡的时间,但不改变
 的平衡转化率,在催化剂一定的情况下可采取的措施是
的平衡转化率,在催化剂一定的情况下可采取的措施是③500℃该反应的化学平衡常数K=
④实验测定该反应的反应速率
 ,
, ,
, 、
、 分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
分别是正、逆反应速率常数,c为物质的量浓度,计算M处的
您最近一年使用:0次
名校
8 . 已知反应: 。在一定压强下,按
。在一定压强下,按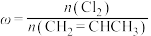 向密闭容器中充入氯气与丙烯。图甲表示平衡时丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时丙烯的体积分数( )与温度(T)、
)与温度(T)、 的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的
的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的
 。在一定压强下,按
。在一定压强下,按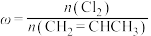 向密闭容器中充入氯气与丙烯。图甲表示平衡时丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时丙烯的体积分数( )与温度(T)、
)与温度(T)、 的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的
的关系,图乙表示反应的平衡常数K与温度T的关系。则下列说法正确的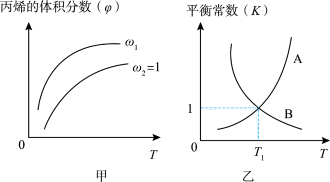
A.图甲中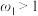 |
| B.图乙中,线A表示正反应的平衡常数 |
| C.若在恒容绝热装置中开始上述反应,达到平衡时装置内的气体压强始终不变 |
D.温度 、 、 , , 的转化率约为33.3% 的转化率约为33.3% |
您最近一年使用:0次
名校
9 . 已知: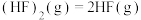 △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
△H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
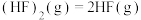 △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
△H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是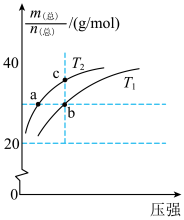
A.反应速率: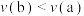 |
B.温度: |
C.当m(总)/n(总)=30g/mol时,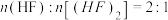 |
| D.欲测定HF的相对分子质量,宜在低温高压下进行 |
您最近一年使用:0次
名校
解题方法
10 . 在恒温恒压下,向密闭容器中充入4mol  和2mol
和2mol  ,发生如下反应:
,发生如下反应: △H<0,2min后,反应达到平衡,生成
△H<0,2min后,反应达到平衡,生成 为1.4mol,同时放出热量Q kJ。则下列分析正确的是
为1.4mol,同时放出热量Q kJ。则下列分析正确的是
 和2mol
和2mol  ,发生如下反应:
,发生如下反应: △H<0,2min后,反应达到平衡,生成
△H<0,2min后,反应达到平衡,生成 为1.4mol,同时放出热量Q kJ。则下列分析正确的是
为1.4mol,同时放出热量Q kJ。则下列分析正确的是A.若反应开始时容器体积为2L,则 |
B.若把条件“恒温恒压”改为“恒压恒容”,则平衡后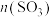 大于1.4mol 大于1.4mol |
C.2min后,向容器中再通入一定量的 气体,重新达到平衡时 气体,重新达到平衡时 的含量变小 的含量变小 |
| D.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于Q kJ |
您最近一年使用:0次



