名校
解题方法
1 . 钠是一种非常活泼、具有广泛应用的金属。请回答:
(1)将一小块金属钠投入水中,发生反应的离子方程式是_______ ;可观察到的实验现象是_______ (填字母序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动 d.有嘶嘶声
(2)钠在空气中的燃烧产物Na2O2可用于呼吸面具或潜水艇中氧气的来源,11.6gCO2和H2O的混合物与足量Na2O2充分反应后,固体质量增加了3.6 g,则生成标准状况下O2的体积_______ L;原混合气体的中CO2和H2O的分子数比为_______ 。
(3)下列实验方案中,不能测定Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是_______
(1)将一小块金属钠投入水中,发生反应的离子方程式是
a.钠沉到水底 b.钠熔成小球 c.小球四处游动 d.有嘶嘶声
(2)钠在空气中的燃烧产物Na2O2可用于呼吸面具或潜水艇中氧气的来源,11.6gCO2和H2O的混合物与足量Na2O2充分反应后,固体质量增加了3.6 g,则生成标准状况下O2的体积
(3)下列实验方案中,不能测定Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是_______
| A.取a g混合物充分加热,质量减少b g |
| B.取a g混合物与足量NaOH溶液充分反应,得到b g溶液 |
| C.取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到b g固体 |
| D.取a g混合物与足量稀硫酸反应,逸出气体经干燥后用碱石灰吸收,质量增加b g |
您最近一年使用:0次
2022-11-29更新
|
538次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2022-2023学年高一上学期期中考试化学试题
名校
2 . 将一定质量的Mg和Al的混合物投入500 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是
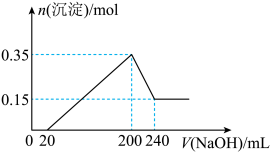

| A.Mg和Al的质量比为3:4 |
| B.生成的H2的体积为10.08 L |
| C.NaOH溶液的物质的量浓度为5 mol/L |
| D.硫酸的物质的量浓度为0.5 mol/L |
您最近一年使用:0次
2022-11-29更新
|
997次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2022-2023学年高一上学期期中考试化学试题
名校
3 . 用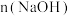 为
为 的
的 浓溶液吸收一定量的氯气,充分反应后溶液中只含有
浓溶液吸收一定量的氯气,充分反应后溶液中只含有 、
、 、
、 三种溶质。下列判断不正确的是
三种溶质。下列判断不正确的是
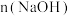 为
为 的
的 浓溶液吸收一定量的氯气,充分反应后溶液中只含有
浓溶液吸收一定量的氯气,充分反应后溶液中只含有 、
、 、
、 三种溶质。下列判断不正确的是
三种溶质。下列判断不正确的是A.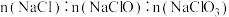 可能为9:4:1 可能为9:4:1 |
B.若反应中转移的电子的物质的量为 ,则 ,则 |
C.被吸收的氯气的物质的量为 |
D. 可能为14:9 可能为14:9 |
您最近一年使用:0次
2022-11-15更新
|
1289次组卷
|
6卷引用:黑龙江省双鸭山市第一中学2022-2023学年高一上学期期中考试化学试题
名校
4 . 葡萄糖酸钙是一种有机钙盐,外观为白色结晶性或颗粒性粉末,无臭,无味,易溶于沸水,微溶于冷水,不溶于乙醇或乙醚等有机溶剂。葡萄糖酸钙临床上用于治疗骨质疏松症。实验室制备葡萄糖酸钙主要步骤如下:
I.葡萄糖酸溶液的制备
称取适量的葡萄糖[CH2OH(CHOH)4CHO],置于三颈烧瓶中,加入足量的溴水,在磁力搅拌器中沸水浴加热、搅拌得到无色透明的葡萄糖酸溶液。当氧化率达 80%以上时(60min),停止反应,把反应液冷却至 60-70℃待用。
Ⅱ.葡萄糖酸钙的制备
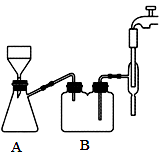
在搅拌下,分批加入足量的碳酸钙至葡萄糖酸溶液中。反应完全后,趁热用下图装置抽滤,得到澄清透明的葡萄糖酸钙溶液。将葡萄糖酸钙溶液转入 100ml 烧杯中冷却至室温,向烧杯中添加适量的无水乙醇,静置 10min 得到悬浊液,抽滤、洗涤、干燥得到白色的葡萄糖酸钙固体。
回答下列问题:
(1)步骤Ⅰ中,滴入溴水后,反应的化学方程式为_______ 。
(2)步骤 Ⅱ 中,判断碳酸钙已经足量的实验现象是_______ 。
(3)步骤Ⅱ抽滤时自来水流的作用是使瓶内与大气形成压强差,与普通过滤操作相比,抽滤的优点是_______ ;装置 B 的作用是_______ 。
(4)洗涤操作洗涤剂最合适的是_______ _(填序号),理由是_______ 。
A.冷水 B. 热水 C.乙醇
Ⅲ.葡萄糖酸钙中钙质量分数的测定
测定步骤:
(i)准确称取葡萄糖酸钙 m g,加入去离子水溶解,定容,配成 250mL 溶液。
(ii)用 c mol/L EDTA(H2Y2-)标准溶液润洗滴定管后,装入 EDTA 标准液,调至零刻度。
(iii)向 250mL 锥形瓶中加入 10mL 水、10mL NH3-NH4Cl 缓冲溶液和 5 mL 硫酸镁溶液。滴加 4 滴铬黑 T(HIn2-)指示剂,摇匀。用 EDTA 标准液滴定至终点。记录消耗的 EDTA 标准液的体积。
滴定过程中发生的反应如下:
Mg2+ + HIn2-(蓝色) MgIn-(酒红色)+ H+
MgIn-(酒红色)+ H+
Mg2+ + H2Y2- MgY2- + 2H+
MgY2- + 2H+
MgIn-(酒红色)+ H2Y2- MgY2- + H+ + HIn2-(蓝色)
MgY2- + H+ + HIn2-(蓝色)
(iv)向上述锥形瓶中加入 25.00 mL 葡萄糖酸钙溶液,摇匀,继续用 EDTA 标准液滴定至终点,记录消耗的 EDTA 标准液的总体积。平行滴定三次,测得步骤 iii 中消耗 EDTA 标准液的平均体积为 V1 L,步骤 iv 中 EDTA 标准液的平均总体积为 V2 L。
已知:配合物的稳定常数类似于化学平衡常数,如反应 Fe3+ + 3SCN- Fe(SCN)3 的平衡常数可以看做是 Fe(SCN)3 的稳定常数 K稳,一般情况下,配合物的稳定常数越大,配合物越稳定,两种离子更容易结合。已知下列化合物稳定常数的大小顺序为 CaY2- > MgY2- > MgIn- > CaIn-,其中CaIn-的稳定常数很小,CaIn-不稳定,易导致滴定终点提前。
Fe(SCN)3 的平衡常数可以看做是 Fe(SCN)3 的稳定常数 K稳,一般情况下,配合物的稳定常数越大,配合物越稳定,两种离子更容易结合。已知下列化合物稳定常数的大小顺序为 CaY2- > MgY2- > MgIn- > CaIn-,其中CaIn-的稳定常数很小,CaIn-不稳定,易导致滴定终点提前。
回答下列问题:
(5)步骤 iii 中加入硫酸镁的作用是_______ 。
(6)滴定终点的颜色变化为_______ 。
(7)步骤 iv 中,加入葡萄糖酸钙后发生反应的离子方程式为_______ ,_______ 。
(8)葡萄糖酸钙中钙的质量分数为_______ 。(用 V1、V2、m、c 的代数式表示)
I.葡萄糖酸溶液的制备
称取适量的葡萄糖[CH2OH(CHOH)4CHO],置于三颈烧瓶中,加入足量的溴水,在磁力搅拌器中沸水浴加热、搅拌得到无色透明的葡萄糖酸溶液。当氧化率达 80%以上时(60min),停止反应,把反应液冷却至 60-70℃待用。
Ⅱ.葡萄糖酸钙的制备
在搅拌下,分批加入足量的碳酸钙至葡萄糖酸溶液中。反应完全后,趁热用下图装置抽滤,得到澄清透明的葡萄糖酸钙溶液。将葡萄糖酸钙溶液转入 100ml 烧杯中冷却至室温,向烧杯中添加适量的无水乙醇,静置 10min 得到悬浊液,抽滤、洗涤、干燥得到白色的葡萄糖酸钙固体。

回答下列问题:
(1)步骤Ⅰ中,滴入溴水后,反应的化学方程式为
(2)步骤 Ⅱ 中,判断碳酸钙已经足量的实验现象是
(3)步骤Ⅱ抽滤时自来水流的作用是使瓶内与大气形成压强差,与普通过滤操作相比,抽滤的优点是
(4)洗涤操作洗涤剂最合适的是
A.冷水 B. 热水 C.乙醇
Ⅲ.葡萄糖酸钙中钙质量分数的测定
测定步骤:
(i)准确称取葡萄糖酸钙 m g,加入去离子水溶解,定容,配成 250mL 溶液。
(ii)用 c mol/L EDTA(H2Y2-)标准溶液润洗滴定管后,装入 EDTA 标准液,调至零刻度。
(iii)向 250mL 锥形瓶中加入 10mL 水、10mL NH3-NH4Cl 缓冲溶液和 5 mL 硫酸镁溶液。滴加 4 滴铬黑 T(HIn2-)指示剂,摇匀。用 EDTA 标准液滴定至终点。记录消耗的 EDTA 标准液的体积。
滴定过程中发生的反应如下:
Mg2+ + HIn2-(蓝色)
 MgIn-(酒红色)+ H+
MgIn-(酒红色)+ H+ Mg2+ + H2Y2-
 MgY2- + 2H+
MgY2- + 2H+ MgIn-(酒红色)+ H2Y2-
 MgY2- + H+ + HIn2-(蓝色)
MgY2- + H+ + HIn2-(蓝色) (iv)向上述锥形瓶中加入 25.00 mL 葡萄糖酸钙溶液,摇匀,继续用 EDTA 标准液滴定至终点,记录消耗的 EDTA 标准液的总体积。平行滴定三次,测得步骤 iii 中消耗 EDTA 标准液的平均体积为 V1 L,步骤 iv 中 EDTA 标准液的平均总体积为 V2 L。
已知:配合物的稳定常数类似于化学平衡常数,如反应 Fe3+ + 3SCN-
 Fe(SCN)3 的平衡常数可以看做是 Fe(SCN)3 的稳定常数 K稳,一般情况下,配合物的稳定常数越大,配合物越稳定,两种离子更容易结合。已知下列化合物稳定常数的大小顺序为 CaY2- > MgY2- > MgIn- > CaIn-,其中CaIn-的稳定常数很小,CaIn-不稳定,易导致滴定终点提前。
Fe(SCN)3 的平衡常数可以看做是 Fe(SCN)3 的稳定常数 K稳,一般情况下,配合物的稳定常数越大,配合物越稳定,两种离子更容易结合。已知下列化合物稳定常数的大小顺序为 CaY2- > MgY2- > MgIn- > CaIn-,其中CaIn-的稳定常数很小,CaIn-不稳定,易导致滴定终点提前。回答下列问题:
(5)步骤 iii 中加入硫酸镁的作用是
(6)滴定终点的颜色变化为
(7)步骤 iv 中,加入葡萄糖酸钙后发生反应的离子方程式为
(8)葡萄糖酸钙中钙的质量分数为
您最近一年使用:0次
5 . 羟基自由基(·OH)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种能将苯酚氧化为 CO2 和 H2O 的原电池-电解池组合装置(如下图所示),该装置能实现发电、环保二位一体。下列说法错误的是
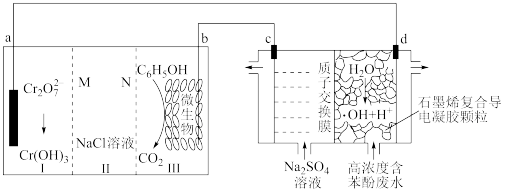

| A.系统工作时,电流由 b 极经 III、II、I 室流向 a 极 |
| B.d 极区苯酚被氧化的化学方程式为 C6H5OH+28·OH = 6 CO2↑+17 H2O |
| C.系统工作时,每转移 28mol e-消耗 1mol 苯酚 |
D.a 电极的电极反应式:7H2O + Cr2O + 6 e-=2 Cr(OH)3 + 8 OH- + 6 e-=2 Cr(OH)3 + 8 OH- |
您最近一年使用:0次
名校
解题方法
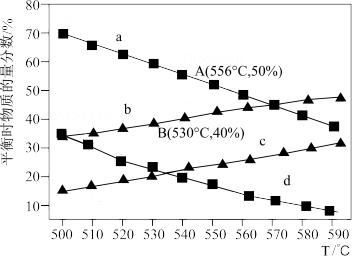
6 . 利用丙烷(C3H8)在无氧条件下制备丙烯(C3H6)的反应方程式为:C3H8(g) C3H6(g)+H2(g) △H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是
C3H6(g)+H2(g) △H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是
 C3H6(g)+H2(g) △H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是
C3H6(g)+H2(g) △H=+124kJ·mol-1。在一体积可变的容器中,不同起始压强下(0.1MPa、0.01MPa)进行上述反应,达到化学平衡时,测得丙烷和丙烯的物质的量分数随温度变化如图所示,则下列说法中正确的是
| A.c曲线表示的是0.01MPa压强下丙烯随温度变化的物质的量分数 |
| B.A点对应的该反应平衡常数Kp=1.25MPa(Kp为以分压表示的平衡常数) |
| C.B点丙烷的平衡转化率为33.3% |
| D.实际生产过程中需通入一定量水蒸气,其目的是稀释原料气,增大丙烯的平衡产率 |
您最近一年使用:0次
2022-09-04更新
|
1510次组卷
|
5卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高二10月月考化学试题
黑龙江省牡丹江市第一高级中学2022-2023学年高二10月月考化学试题重庆市南开中学校2022-2023学年高三上学期第一次质量检测联考化学试题(已下线)2022年北京高考真题变式题1-14(已下线)2022年北京高考真题化学试题变式题(选择题11-14)重庆市南开中学2022-2023学年高三上学期第一次质检化学试题
名校
解题方法
7 . 砷是生命的第七元素,可形成多种重要的化合物。回答下列问题:
(1)基态砷原子N电子层中的成对电子与单电子的数量比为_______ 。As的第一电离能(I1)比Se大的原因是_______ 。
(2)雄黄(As4S4)和雌黄(As2S3)在自然界中共生,是提取砷的主要矿物原料,其结构如下图所示,1mol雄黄与O2反应生成As2O3,转移28mol电子,则另一种产物为_______ 。雌黄中As的杂化方式为_______ 。

(3)亚砷酸(H3AsO3)可以用来治疗白血病,为三元弱酸,试推测 的空间构型为
的空间构型为____ 。其酸性弱于砷酸(H3AsO4)的原因是_______ 。
(4)砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料。晶胞结构如下图所示

已知:砷化镓晶体密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。
①连接面心上6个砷原子构成正八面体,该正八面体的边长为_______ pm(用含 和
和 的代数式表示)。
的代数式表示)。
②Ga和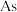 之间的最近距离为
之间的最近距离为_______ nm(用含 和
和 的代数式表示)。
的代数式表示)。
(1)基态砷原子N电子层中的成对电子与单电子的数量比为
(2)雄黄(As4S4)和雌黄(As2S3)在自然界中共生,是提取砷的主要矿物原料,其结构如下图所示,1mol雄黄与O2反应生成As2O3,转移28mol电子,则另一种产物为

(3)亚砷酸(H3AsO3)可以用来治疗白血病,为三元弱酸,试推测
 的空间构型为
的空间构型为(4)砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料。晶胞结构如下图所示

已知:砷化镓晶体密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。①连接面心上6个砷原子构成正八面体,该正八面体的边长为
 和
和 的代数式表示)。
的代数式表示)。②Ga和
 之间的最近距离为
之间的最近距离为 和
和 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
8 . 铬酸铅俗称铬黄,是一种难溶于水的黄色固体,也是一种重要的黄色颜料,常用作橡胶、油墨、水彩、色纸等的着色剂。工业上用草酸泥渣(主要含草酸铅、硫酸铅)和铬矿渣(主要成分为 ,含有少量的
,含有少量的 )为原料制备铬酸铅,实现资源的回收再利用,其流程如下:
)为原料制备铬酸铅,实现资源的回收再利用,其流程如下:
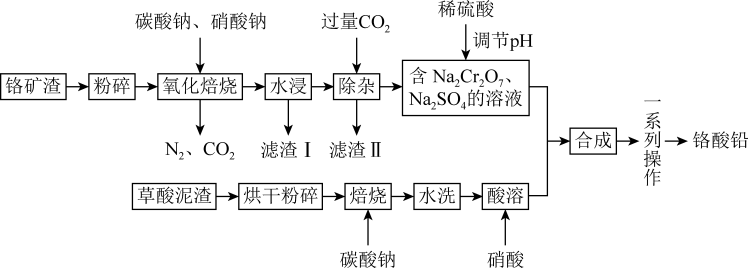
回答下列问题:
(1)将铬矿渣“粉碎"”的目的是_______ ;草酸泥渣“焙烧”后“水洗”的作用是_______ 。
(2)“滤渣Ⅱ”的主要成分是_______ (填化学式)。
(3)“氧化焙烧”时, 被氧化的反应的化学方程式为
被氧化的反应的化学方程式为_______ 。
(4)“一系列操作”包括_______ 、粉碎。
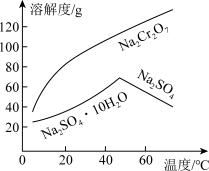
(5)为了使产品更纯,需将“含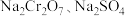 的溶液”分离提纯,依据如图所示的溶解度信息,“含
的溶液”分离提纯,依据如图所示的溶解度信息,“含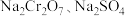 的溶液”分离提纯的操作是
的溶液”分离提纯的操作是_______ 。分离提纯后得到的固体的化学式为_______ 。
(6)“焙烧”时加入碳酸钠是为了将硫酸铅转化为氧化铅 ,同时放出二氧化碳,该转化过程的化学方程式为
,同时放出二氧化碳,该转化过程的化学方程式为_______ 。
 ,含有少量的
,含有少量的 )为原料制备铬酸铅,实现资源的回收再利用,其流程如下:
)为原料制备铬酸铅,实现资源的回收再利用,其流程如下:
回答下列问题:
(1)将铬矿渣“粉碎"”的目的是
(2)“滤渣Ⅱ”的主要成分是
(3)“氧化焙烧”时,
 被氧化的反应的化学方程式为
被氧化的反应的化学方程式为(4)“一系列操作”包括
(5)为了使产品更纯,需将“含
 的溶液”分离提纯,依据如图所示的溶解度信息,“含
的溶液”分离提纯,依据如图所示的溶解度信息,“含 的溶液”分离提纯的操作是
的溶液”分离提纯的操作是
(6)“焙烧”时加入碳酸钠是为了将硫酸铅转化为氧化铅
 ,同时放出二氧化碳,该转化过程的化学方程式为
,同时放出二氧化碳,该转化过程的化学方程式为
您最近一年使用:0次
9 . 聚乳酸(PLA)是最具潜力的可降解高分子材料之一,对其进行基团修饰可进行材料的改性,从而拓展PLA的应用范围。PLA和某改性的PLA的合成路线如图。
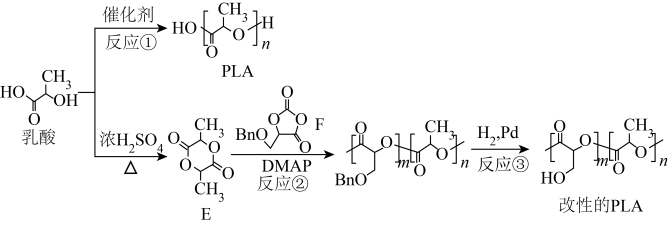
注:Bn是苯甲基(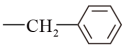 )
)
下列说法正确 的有几个
(1)反应①是缩聚反应
(2)在合成中Bn的作用是保护羟基,防止羟基参与聚合反应
(3)改性的PLA中,m∶n越大,其在水中的溶解性越好
(4)反应②中,参与聚合的F和E的物质的量之比是m∶n

注:Bn是苯甲基(
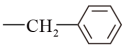 )
)下列说法
(1)反应①是缩聚反应
(2)在合成中Bn的作用是保护羟基,防止羟基参与聚合反应
(3)改性的PLA中,m∶n越大,其在水中的溶解性越好
(4)反应②中,参与聚合的F和E的物质的量之比是m∶n
| A.4个 | B.3个 | C.2个 | D.1个 |
您最近一年使用:0次
2022-05-08更新
|
1035次组卷
|
3卷引用:黑龙江省大庆实验中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
10 . 如图所示,在注射器里吸入20mL NO,然后吸入5mL水。若再吸入30mL空气(按O2体积占1/5计算),夹住弹簧夹,观察现象(不考虑摩擦力)。已知常温常压下,气体摩尔体积为24.5 L·mol-1,则下列叙述不正确的是
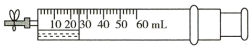

| A.最终剩余气体体积约为36mL |
| B.可观察到注射器的活塞缓缓向右移动 |
| C.可观察到注射器内气体由无色变成红棕色,最后变成无色 |
| D.若反应前后液体体积不变,所得硝酸溶液的浓度约为0.07mol/L |
您最近一年使用:0次
2022-05-03更新
|
1814次组卷
|
6卷引用:黑龙江省佳木斯市第十二中学2022-2023学年高三上学期期中考试化学试题



