解题方法
1 . Fe、Cu都是人类早期使用的金属,某校化学研究性学习小组的同学通过实验研究Fe、Cu及其化合物的相关性质。回答下列问题:
(1)甲同学取两束细铜丝用砂纸打磨后在酒精灯上加热至红热,再分别伸入盛有 、
、 的集气瓶中。则甲同学在两个集气瓶中观察到的现象是
的集气瓶中。则甲同学在两个集气瓶中观察到的现象是__________ 。

(2)乙同学为验证Fe在冷的浓硝酸中发生钝化但能和热的浓硝酸发生反应,设计了如图所示的实验装置,结果发现装置1中无明显现象,装置2中________ (填实验现象);为使装置2能控制反应的进行,请对装置2提出改进意见:_________ 。
(3)丙同学在Fe和热的浓硝酸反应后的溶液中加入一块Cu片,Cu片逐渐溶解,反应一段时间后Cu片不再溶解。
①丙同学依据反应现象得出Cu片溶解的原因是Cu和 发生了反应,则他依据的反应现象是
发生了反应,则他依据的反应现象是______ 。
②丁同学认为丙同学的结论不完全正确,理由是___________ 。
(4)请设计实验证明加入Cu片并反应完全后的溶液中含有 但不含
但不含 。写出具体的实验方案和实验现象:
。写出具体的实验方案和实验现象:_____________ 。
(1)甲同学取两束细铜丝用砂纸打磨后在酒精灯上加热至红热,再分别伸入盛有
 、
、 的集气瓶中。则甲同学在两个集气瓶中观察到的现象是
的集气瓶中。则甲同学在两个集气瓶中观察到的现象是
(2)乙同学为验证Fe在冷的浓硝酸中发生钝化但能和热的浓硝酸发生反应,设计了如图所示的实验装置,结果发现装置1中无明显现象,装置2中
(3)丙同学在Fe和热的浓硝酸反应后的溶液中加入一块Cu片,Cu片逐渐溶解,反应一段时间后Cu片不再溶解。
①丙同学依据反应现象得出Cu片溶解的原因是Cu和
 发生了反应,则他依据的反应现象是
发生了反应,则他依据的反应现象是②丁同学认为丙同学的结论不完全正确,理由是
(4)请设计实验证明加入Cu片并反应完全后的溶液中含有
 但不含
但不含 。写出具体的实验方案和实验现象:
。写出具体的实验方案和实验现象:
您最近一年使用:0次
2 . 已知红热的铁能与水蒸气反应生成氢气。现用如图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集、检验生成的氢气。请回答下列问题。

(1)写出铁在高温下与水蒸气反应的化学方程式:_________________________ 。
(2)干燥管C中盛放的药品是__________________ ;干燥管的____________ (填“m”或“n”)端与g导管相连接。
(3)在D处画出用试管收集氢气的装置图(所需其他仪器自行选择)。______
(4)怎样用简单的方法检验收集到的气体是氢气?
简述实验操作步骤和现象:______________________________ 。
(5)若收集到标准状况下的H2 22.4L,则参加反应的铁粉的质量为____________ g。
(6)当固体质量增加32g时,生成H2的质量为________________ g。

(1)写出铁在高温下与水蒸气反应的化学方程式:
(2)干燥管C中盛放的药品是
(3)在D处画出用试管收集氢气的装置图(所需其他仪器自行选择)。
(4)怎样用简单的方法检验收集到的气体是氢气?
简述实验操作步骤和现象:
(5)若收集到标准状况下的H2 22.4L,则参加反应的铁粉的质量为
(6)当固体质量增加32g时,生成H2的质量为
您最近一年使用:0次
3 . 氨气与适量氯气混合反应可生成NH4Cl(岩脑砂的主要成分)和一种无污染的气体。某学习小组利用下列装置模拟该反应,请回答相关问题。
A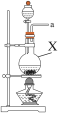 B
B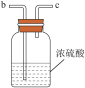
C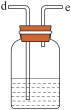 D
D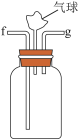
(1)该实验中所需的氯气是用浓盐酸与MnO2反应制取。装置A中仪器X的名称为________________ 。
(2)要得到干燥纯净的氯气,A、B、C装置中导管的连接顺序为a→________________ → ________________ → ________________ → ________________ 。
(3)利用D装置,将适量氨气与氯气充分混合,氨气应从__________ 通入,反应的化学方程式为 ___________ ;可能观察到的现象是________________ 。
(4)现取岩脑砂进行NH4Cl含量的测定。准确称取一定质量的岩脑砂,与足量的氧化铜混合,如图所示进行实验。已知:2NH4Cl+3CuO 3Cu+N2↑+2HCl↑+3H2O
3Cu+N2↑+2HCl↑+3H2O
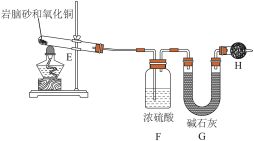
①为顺利完成有关物理量的测定,请完善下列表格。
②如果不用H装置,测出NH4Cl的含量将_____ (填“偏高”“偏低”或“无影响”)。
A
 B
B
C
 D
D
(1)该实验中所需的氯气是用浓盐酸与MnO2反应制取。装置A中仪器X的名称为
(2)要得到干燥纯净的氯气,A、B、C装置中导管的连接顺序为a→
(3)利用D装置,将适量氨气与氯气充分混合,氨气应从
(4)现取岩脑砂进行NH4Cl含量的测定。准确称取一定质量的岩脑砂,与足量的氧化铜混合,如图所示进行实验。已知:2NH4Cl+3CuO
 3Cu+N2↑+2HCl↑+3H2O
3Cu+N2↑+2HCl↑+3H2O
①为顺利完成有关物理量的测定,请完善下列表格。
| 测量时间点 | 反应前 | 反应后 |
| 测量内容 | 当观察到 时停止加热,冷却,称量H装置的总质量 |
②如果不用H装置,测出NH4Cl的含量将
您最近一年使用:0次
4 . 某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验。

实验中某同学将a g铜片和12 mL 18 mol·L-1的浓硫酸放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的H2SO4和Cu剩余。
请回答:
(1)请写出Cu与浓硫酸反应的化学方程式:_____________________________ 。
(2)装置E中试管D内盛品红溶液,当C中气体收集满后,D中有可能观察到的现象是______________________ 。
实验装置E中D有可能造成环境污染,试用最简单方法加以解决(实验用品自选)______________ 。
装置B的作用是储存多余的气体。当D处有明显现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是____________________ 。B中应放置的液体是________ (填字母)。
A 饱和Na2SO3溶液 B 酸性KMnO4溶液 C 浓溴水 D 饱和NaHSO3溶液
(3)问题讨论:为什么有一定量的余酸还未能使Cu完全溶解。你认为原因是______________________ 。
足量下列药品能够用来证明反应结束后的烧瓶中的确有余酸的是________ (填字母)。
A Fe B BaCl2溶液 C Ag D Na2CO3溶液
(4)实验中该同学向A中反应后溶液中通入一种气体单质,使铜片全部溶解且仅生成硫酸铜溶液,请问该气体单质是__________ (填名称),反应的化学方程式是__________________________________ 。

实验中某同学将a g铜片和12 mL 18 mol·L-1的浓硫酸放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的H2SO4和Cu剩余。
请回答:
(1)请写出Cu与浓硫酸反应的化学方程式:
(2)装置E中试管D内盛品红溶液,当C中气体收集满后,D中有可能观察到的现象是
实验装置E中D有可能造成环境污染,试用最简单方法加以解决(实验用品自选)
装置B的作用是储存多余的气体。当D处有明显现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是
A 饱和Na2SO3溶液 B 酸性KMnO4溶液 C 浓溴水 D 饱和NaHSO3溶液
(3)问题讨论:为什么有一定量的余酸还未能使Cu完全溶解。你认为原因是
足量下列药品能够用来证明反应结束后的烧瓶中的确有余酸的是
A Fe B BaCl2溶液 C Ag D Na2CO3溶液
(4)实验中该同学向A中反应后溶液中通入一种气体单质,使铜片全部溶解且仅生成硫酸铜溶液,请问该气体单质是
您最近一年使用:0次
2019-05-23更新
|
803次组卷
|
4卷引用:鲁教版高中化学必修1第三章《自然界中的元素》测试卷1
5 . 某校学生实验小组为了证明铜与稀硝酸反应产生一氧化氮,用如图所示装置进行实验(加热装置和夹持装置均已略去,气密性已检验,F是用于鼓入空气的双连打气球)。
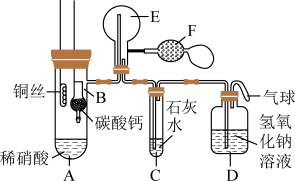
实验操作及现象为:
(1)操作Ⅰ中产生气体的离子反应方程式为__ ;
(2)操作Ⅰ的目的是__ ;
(3)C中白色沉淀的化学式是__ ,操作Ⅱ中当C产生白色沉淀时立刻将B上提的原因是__ ;
(4)操作Ⅲ中装置A产生无色气体的化学方程式是__ ;
(5)烧瓶E内气体颜色逐渐加深的原因是__ ;
(6)操作Ⅴ现象产生的原因是(结合化学方程式说明)__ ;
(7)D装置的作用是__ 。

实验操作及现象为:
| 操作 | 现象 |
| I,将B装置下移,使碳酸钙与稀硝酸接触 | 产生气体 |
| Ⅱ.当C处产生白色沉淀,立刻将B装置上提 | |
| III.将A中铜丝放入稀硝酸中,给装置A微加热 | 装置A中产生无色气体,装置E中开始时出现浅红棕色气体 |
| IV.用F向E中鼓入空气 | 烧瓶E内气体颜色逐渐加深 |
| V.一段时间后 | C中白色沉淀溶解 |
(2)操作Ⅰ的目的是
(3)C中白色沉淀的化学式是
(4)操作Ⅲ中装置A产生无色气体的化学方程式是
(5)烧瓶E内气体颜色逐渐加深的原因是
(6)操作Ⅴ现象产生的原因是(结合化学方程式说明)
(7)D装置的作用是
您最近一年使用:0次
6 . 过氧化钠是一种淡黄色固体,能与水反应,常用在呼吸面具和潜水艇里作为氧气的来源,还可用作熔矿剂,使某些不溶于酸的矿物分解。用脱脂棉包住约0.2 g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来。
请回答:(1)由实验现象所得出的有关过氧化钠与水反应的结论是:
a.有氧气生成;b.__________ 。
(2)某研究性学习小组拟用如图所示装置进行实验,以证明上述结论。
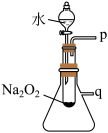
①用以验证结论a的实验方法是:__________ ;
②用以验证结论b的实验方法是:______________ 。
请回答:(1)由实验现象所得出的有关过氧化钠与水反应的结论是:
a.有氧气生成;b.
(2)某研究性学习小组拟用如图所示装置进行实验,以证明上述结论。

①用以验证结论a的实验方法是:
②用以验证结论b的实验方法是:
您最近一年使用:0次
2020-01-28更新
|
78次组卷
|
2卷引用:人教版高中化学必修1第三章《金属及其化合物》测试卷1
19-20高一·全国·单元测试
解题方法
7 . 下列实验的现象或表述正确的是
| A.向等浓度的碳酸钠和碳酸氢钠溶液中滴加酚酞,碳酸氢钠溶液的红色更深 |
| B.检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴即可 |
| C.制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁 |
| D.向饱和FeCl3溶液中滴入少量NaOH溶液,煮沸后即得红棕色Fe(OH)3胶体 |
您最近一年使用:0次
名校
解题方法
8 . 某小组取一定质量的FeSO4固体,利用下图装置进行实验。
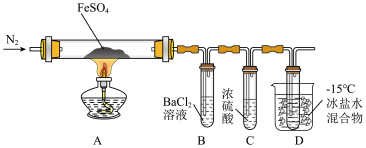
已知:SO2熔点-72℃,沸点-10℃;SO3熔点16.8℃,沸点44.8 ℃。
(1)实验③反应的离子方程式是_________________________ 。
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有________ 气体,依据是________________________________ 。
(3)实验④反应的离子方程式是__________________________ 。
(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。你认为是否正确,并说明原因:____________ (用必要的文字和化学方程式解释)。

| 实验 | 实验过程 | 实验现象 |
| ① | 通入一段时间N2,加热 | A中固体变为红棕色 B中有白色沉淀,D试 管中有无色液体 |
| ② | 用带有火星的木条靠近 装置D的导管口 | 木条复燃 |
| ③ | 充分反应,停止加热, 冷却后,取A中固体, 加盐酸 | 固体溶解,溶液呈黄色 |
| ④ | 将③所得溶液滴入D 试管中 | 溶液变为浅绿色 |
(1)实验③反应的离子方程式是
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有
(3)实验④反应的离子方程式是
(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。你认为是否正确,并说明原因:
您最近一年使用:0次
2020-02-17更新
|
408次组卷
|
2卷引用:重庆市南开中学高一下学期化学人教版第1章《非金属及其化合物》单元测试
9 . 按如图所示装置进行实验,填写有关现象及化学方程式。
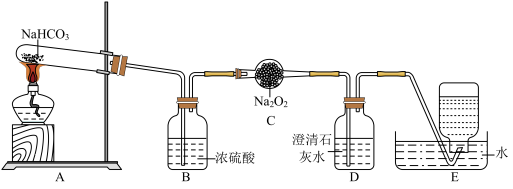
(1)A中现象是________________________________ 。
(2)B中浓硫酸的作用是__________________________ 。
(3)C中发生反应的化学方程式为____________________________________ 。
(4)D中的现象是______________________________ 。
(5)E中收集的气体是____________ (填名称)。

(1)A中现象是
(2)B中浓硫酸的作用是
(3)C中发生反应的化学方程式为
(4)D中的现象是
(5)E中收集的气体是
您最近一年使用:0次
2020-01-29更新
|
379次组卷
|
11卷引用:人教版高中化学必修一第三章《金属及其化合物》测试卷1
人教版高中化学必修一第三章《金属及其化合物》测试卷1苏教版高中化学必修1专题2《从海水中获得的化学物质》测试卷(已下线)2.1.2 钠的几种化合物 焰色试验(精练)——2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)(已下线)2.1.2 钠的几种化合物 焰色试验(精练)-2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)安徽省定远县育才学校2020-2021学年高一上学期11月质量检测化学试题湖北省孝感市普通高中2021-2022学年高一上学期期中联合考试化学试题甘肃省秦安县第一中学2021-2022学年高一上学期期中考试化学试题(已下线)第07讲 碳酸钠和碳酸氢钠-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)2.1.2 钠的氧化物与焰色试验-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)甘肃省嘉峪关市等3地2022-2023学年高一上学期12月期中考试化学试题湖南省株洲市株洲世纪星高级中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
10 . 用如图所示的装置做铝热反应实验,回答下列问题:
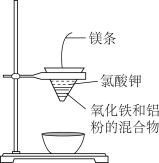
(1)写出该反应的化学方程式:___ ,在该反应中___ 是氧化剂,___ 是还原剂,该反应称为___ 反应。
(2)选出该实验的实验现象(把序号填写在横线上):___ 。
①镁条剧烈燃烧;②放出大量的热,并发出耀眼的光芒,火星四射;③纸漏斗的下部被烧穿;④有红热状态的液珠落入蒸发皿内的细沙上,液珠冷却后变为黑色固体。
(3)写出下列操作或物质的作用:内层纸漏斗底部剪一个孔:___ ;蒸发皿盛沙:___ ;镁条:___ ;氯酸钾:___ 。

(1)写出该反应的化学方程式:
(2)选出该实验的实验现象(把序号填写在横线上):
①镁条剧烈燃烧;②放出大量的热,并发出耀眼的光芒,火星四射;③纸漏斗的下部被烧穿;④有红热状态的液珠落入蒸发皿内的细沙上,液珠冷却后变为黑色固体。
(3)写出下列操作或物质的作用:内层纸漏斗底部剪一个孔:
您最近一年使用:0次



