名校
1 . 设 表示阿伏加德罗常数值,下列叙述正确的是
表示阿伏加德罗常数值,下列叙述正确的是
 表示阿伏加德罗常数值,下列叙述正确的是
表示阿伏加德罗常数值,下列叙述正确的是A.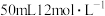 浓盐酸与足量 浓盐酸与足量 共热,转移的电子数目为 共热,转移的电子数目为 |
B.标准状况下,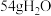 中含有分子数为 中含有分子数为 个 个 |
C.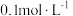 的硫酸铝溶液所含的硫酸根离子的数目就是 的硫酸铝溶液所含的硫酸根离子的数目就是 |
D.在溶有 的胶体中,含有 的胶体中,含有 个 个 胶粒 胶粒 |
您最近一年使用:0次
2024-02-18更新
|
48次组卷
|
2卷引用:湖北省部分县市区省级示范高中温德克英协作体2023-2024学年高二上学期期末综合性调研考试化学试题
2 . 在2.8gFe中加入100mL3mol/L HCl,Fe完全溶解。 代表阿伏加德罗常数的值,下列说法错误的是
代表阿伏加德罗常数的值,下列说法错误的是
 代表阿伏加德罗常数的值,下列说法错误的是
代表阿伏加德罗常数的值,下列说法错误的是A.HCl溶液中 数为 数为 | B.反应转移的电子数为 |
C. 含有的中子数为 含有的中子数为 | D.反应生成标准状况下的气体2.24L |
您最近一年使用:0次
名校
解题方法
3 . 有一块铁的“氧化物”样品,用140mL5.0mol•L-1盐酸恰好将之完全溶解,所得溶液还能吸收0.56LCl2(标况下),恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为
| A.Fe4O5 | B.Fe3O4 | C.Fe5O7 | D.Fe2O3 |
您最近一年使用:0次
2024-02-14更新
|
52次组卷
|
3卷引用:河南省南阳市邓州市第六高级中学校2023-2024学年高二下学期开学测试化学试题
名校
4 . 已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下: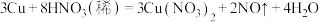 。
。
(1)用单桥法表示电子转移______ 。
(2)被氧化的元素是______ ,被还原的元素是_______ ,发生氧化反应的物质是______ 。
(3)若消耗 还原剂,则被还原的氧化剂是
还原剂,则被还原的氧化剂是______  ,
, 表现
表现_______ 性。
(4)铁钉在氯气中被锈蚀成棕黄色物质 ,而在盐酸中生成浅绿色溶液(
,而在盐酸中生成浅绿色溶液( );向浓盐酸中滴加
);向浓盐酸中滴加 溶液产生黄绿色气体(
溶液产生黄绿色气体( )。则在
)。则在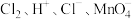 中,具有氧化性的是
中,具有氧化性的是_____ 、_______ 氧化性最强。
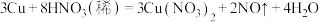 。
。(1)用单桥法表示电子转移
(2)被氧化的元素是
(3)若消耗
 还原剂,则被还原的氧化剂是
还原剂,则被还原的氧化剂是 ,
, 表现
表现(4)铁钉在氯气中被锈蚀成棕黄色物质
 ,而在盐酸中生成浅绿色溶液(
,而在盐酸中生成浅绿色溶液( );向浓盐酸中滴加
);向浓盐酸中滴加 溶液产生黄绿色气体(
溶液产生黄绿色气体( )。则在
)。则在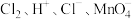 中,具有氧化性的是
中,具有氧化性的是
您最近一年使用:0次
名校
5 . 在 被水吸收的反应中,化学方程式为
被水吸收的反应中,化学方程式为 ,氧化剂和还原剂的物质的量之比为
,氧化剂和还原剂的物质的量之比为
 被水吸收的反应中,化学方程式为
被水吸收的反应中,化学方程式为 ,氧化剂和还原剂的物质的量之比为
,氧化剂和还原剂的物质的量之比为A. | B. | C. | D. |
您最近一年使用:0次
解题方法
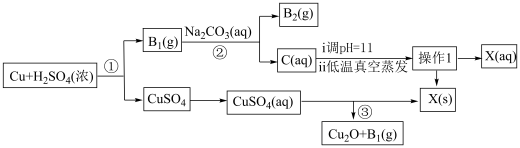
6 . 一种制备 的工艺路线如图所示
的工艺路线如图所示
已知:ⅰ.常温下, 的电离平衡常数
的电离平衡常数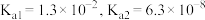
ⅱ.反应②所得C溶液 在
在 之间
之间
ⅲ.反应③需及时补加 以保持反应在
以保持反应在 条件下进行。
条件下进行。
(1)反应①中氧化剂与还原剂物质的量之比为___________ ,溶液C的溶质为___________ (填化学式)。
(2)低温真空蒸发主要目的是___________ ,操作1的名称为___________ 。
(3)写出流程中可以循环利用的物质___________ (填化学式)。
(4)写出反应③的化学反应方程式___________ 。
(5)若 产量不变,参与反应③的X与
产量不变,参与反应③的X与 物质的量之比
物质的量之比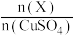 增大时,需补加
增大时,需补加 的量
的量___________ (填“减少”或“增多”或“不变”)。
 的工艺路线如图所示
的工艺路线如图所示
已知:ⅰ.常温下,
 的电离平衡常数
的电离平衡常数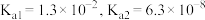
ⅱ.反应②所得C溶液
 在
在 之间
之间ⅲ.反应③需及时补加
 以保持反应在
以保持反应在 条件下进行。
条件下进行。(1)反应①中氧化剂与还原剂物质的量之比为
(2)低温真空蒸发主要目的是
(3)写出流程中可以循环利用的物质
(4)写出反应③的化学反应方程式
(5)若
 产量不变,参与反应③的X与
产量不变,参与反应③的X与 物质的量之比
物质的量之比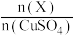 增大时,需补加
增大时,需补加 的量
的量
您最近一年使用:0次
7 . 卤族元素的化合物在生活、医药、化工中有着重要的用途。
Ⅰ.过氧化氢氧化法制备碘酸钾(KIO3)的方法如图:
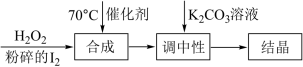
(1)合成步骤的加热方法为______ ,发生反应的化学方程式为____________________ 。
(2)当合成温度高于70℃,碘酸钾产率会降低,写出可能的两种原因:____________________ 。
Ⅱ.ClO2和Cl2都可以用于自来水消毒杀菌,可以通过下列方法制取:
(3)该反应的氧化产物为______ ,若反应过程中有4 mol HCl参与反应,则电子转移的数目为______ 。
Ⅲ.目前从海水中提溴(Br2)大致有“浓缩”、“氧化”、“提取”等步骤。
(4)向浓缩的海水中通入Cl2,将海水中的 氧化为Br2,再用热空气将Br2从溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3和CO2,吸收反应的离子方程式为
氧化为Br2,再用热空气将Br2从溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3和CO2,吸收反应的离子方程式为____________________ 。
Ⅰ.过氧化氢氧化法制备碘酸钾(KIO3)的方法如图:

(1)合成步骤的加热方法为
(2)当合成温度高于70℃,碘酸钾产率会降低,写出可能的两种原因:
Ⅱ.ClO2和Cl2都可以用于自来水消毒杀菌,可以通过下列方法制取:

(3)该反应的氧化产物为
Ⅲ.目前从海水中提溴(Br2)大致有“浓缩”、“氧化”、“提取”等步骤。
(4)向浓缩的海水中通入Cl2,将海水中的
 氧化为Br2,再用热空气将Br2从溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3和CO2,吸收反应的离子方程式为
氧化为Br2,再用热空气将Br2从溶液中吹出,并由浓Na2CO3溶液吸收,转变为NaBr、NaBrO3和CO2,吸收反应的离子方程式为
您最近一年使用:0次
名校
8 . 下列反应中,氧化剂与还原剂化学计量数为1:2的是
| A.Fe+2HCl=FeCl2+H2↑ |
| B.2HCl+Ca(ClO)2=2HClO+CaCl2 |
| C.I2+2NaClO3=2NaIO3+Cl2↑ |
D.4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O MnCl2+Cl2↑+2H2O |
您最近一年使用:0次
解题方法
9 . 锰酸锂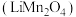 作为一种新型锂电池正极材料受到广泛关注。工业上利用
作为一种新型锂电池正极材料受到广泛关注。工业上利用 溶液多途径制备锰酸锂的流程如下,回答下列问题:
溶液多途径制备锰酸锂的流程如下,回答下列问题:

已知:①硫酸的结构为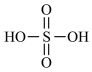
②干冰的晶胞结构见图。
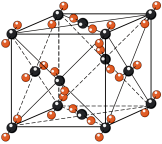
(1)将干冰晶胞沿体对角线投影,●代表 分子,则
分子,则 的投影图为______(选填序号)
的投影图为______(选填序号)
(2)工艺1中, 中S元素的化合价为
中S元素的化合价为 ,画出
,画出 的结构式
的结构式______ 。
(3)工艺2中,发生电解反应的离子方程式为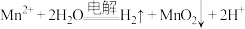 。随着电解反应进行,为保持电解液成分和浓度稳定,应不断加入
。随着电解反应进行,为保持电解液成分和浓度稳定,应不断加入______ (填化学式)。
(4)工艺3中,“沉锰、过滤”得到 和
和 ;若“控温、氧化”时溶液的pH显著减小,此时
;若“控温、氧化”时溶液的pH显著减小,此时 发生反应的化学方程式为
发生反应的化学方程式为______ 。
(5)为控制碳排放,用NaOH溶液吸收焙烧窑中释放的 并转化为正盐,理论上消耗的
并转化为正盐,理论上消耗的 和NaOH的物质的量之比为
和NaOH的物质的量之比为______ 。
 作为一种新型锂电池正极材料受到广泛关注。工业上利用
作为一种新型锂电池正极材料受到广泛关注。工业上利用 溶液多途径制备锰酸锂的流程如下,回答下列问题:
溶液多途径制备锰酸锂的流程如下,回答下列问题:
已知:①硫酸的结构为

②干冰的晶胞结构见图。

(1)将干冰晶胞沿体对角线投影,●代表
 分子,则
分子,则 的投影图为______(选填序号)
的投影图为______(选填序号)A.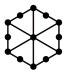 | B.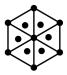 |
C.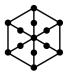 | D.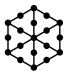 |
(2)工艺1中,
 中S元素的化合价为
中S元素的化合价为 ,画出
,画出 的结构式
的结构式(3)工艺2中,发生电解反应的离子方程式为
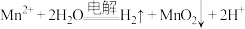 。随着电解反应进行,为保持电解液成分和浓度稳定,应不断加入
。随着电解反应进行,为保持电解液成分和浓度稳定,应不断加入(4)工艺3中,“沉锰、过滤”得到
 和
和 ;若“控温、氧化”时溶液的pH显著减小,此时
;若“控温、氧化”时溶液的pH显著减小,此时 发生反应的化学方程式为
发生反应的化学方程式为(5)为控制碳排放,用NaOH溶液吸收焙烧窑中释放的
 并转化为正盐,理论上消耗的
并转化为正盐,理论上消耗的 和NaOH的物质的量之比为
和NaOH的物质的量之比为
您最近一年使用:0次
名校
解题方法
10 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
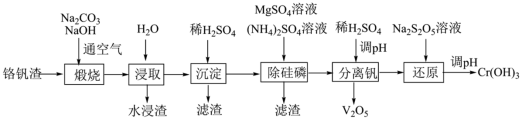
已知:最高价铬酸根在酸性介质中以 存在,在碱性介质中以
存在,在碱性介质中以 存在。
存在。
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为_______ (填化学式)。
(2)“沉淀”步骤中主要生成的滤渣为_______ (填化学式)。
(3)“除硅磷”步骤中,使硅、磷分别以 和
和 的形式沉淀,该步需要控制溶液的
的形式沉淀,该步需要控制溶液的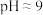 的原因为
的原因为_______ 。
(4)“分离钒”步骤中,将溶液pH调到1.8左右得到 沉淀,
沉淀, 在
在 时溶解为
时溶解为 的离子方程式为
的离子方程式为_______ 。
(5)“还原”步骤中加入焦亚硫酸钠 溶液,反应中氧化剂和还原剂的物质的量之比为
溶液,反应中氧化剂和还原剂的物质的量之比为_______ ; 的性质与
的性质与 相似,写出
相似,写出 与
与 溶液反应的离子方程式
溶液反应的离子方程式_______ 。

已知:最高价铬酸根在酸性介质中以
 存在,在碱性介质中以
存在,在碱性介质中以 存在。
存在。(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(2)“沉淀”步骤中主要生成的滤渣为
(3)“除硅磷”步骤中,使硅、磷分别以
 和
和 的形式沉淀,该步需要控制溶液的
的形式沉淀,该步需要控制溶液的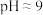 的原因为
的原因为(4)“分离钒”步骤中,将溶液pH调到1.8左右得到
 沉淀,
沉淀, 在
在 时溶解为
时溶解为 的离子方程式为
的离子方程式为(5)“还原”步骤中加入焦亚硫酸钠
 溶液,反应中氧化剂和还原剂的物质的量之比为
溶液,反应中氧化剂和还原剂的物质的量之比为 的性质与
的性质与 相似,写出
相似,写出 与
与 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次



